Clear Sky Science · sv
Konstruera programmerbar CAR och antigenparning via drogstyrd ljusaktivering
Lära immunceller att jaga smartare
Många har hört talas om CAR T‑celler, en typ av individualiserad cancerbehandling som omprogrammerar en patients egna immunceller för att attackera tumörer. Dessa terapier fungerar väl för vissa blodcancerformer men har haft svårt mot solida tumörer, som i bröst, prostata eller lungor. Denna studie beskriver ett nytt sätt att både skärpa och begränsa CAR T‑celler så att de bättre kan hitta mångfaldiga tumörceller samtidigt som frisk vävnad skonas.
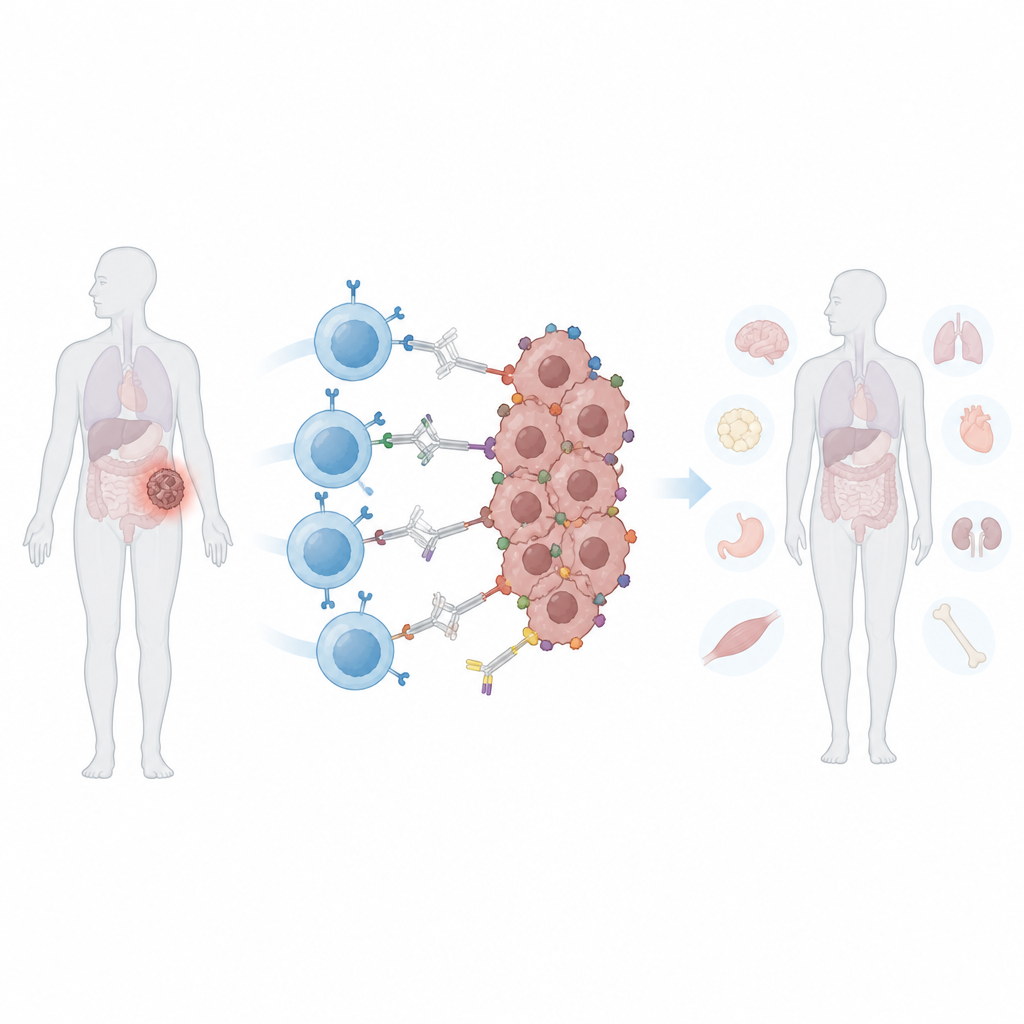
Utmaningen med formbytande tumörer
Standard‑CAR T‑celler är byggda för att känna igen en specifik molekylär “flagga” på cancerceller. Solida tumörer undgår ofta denna attack på två sätt. För det första kan de förlora eller sänka uttrycket av den flaggan, en process som kallas antigenflykt, vilket tillåter vissa celler att överleva och återskapa tumören. För det andra kan olika celler inom samma tumör visa olika flaggor, ett problem som kallas heterogenitet. Att utöka CAR T‑cellernas igenkänning till fler flaggor kan hjälpa, men det ökar också risken att de attackerar normala vävnader som delar dessa markörer. När konventionella CAR T‑celler har getts intravenöst är de ständigt aktiva, vilket gör det svårt för läkare att skruva upp eller ner deras aktivitet om biverkningar uppstår.
En universalplugg för att sikta på många tumörtyper
Forskarna skapade en ”programmerbar” CAR som inte binder tumörceller direkt. Istället känner den igen ett säkert, starkt färgat protein kallat fykoerytrin, som ofta används i livsmedel och laboratorietester. De konstruerade ett litet människodervat bindningsdomän, kallat en PEbody, på CAR:en så att den fäster vid vilken antikropp som helst som bär denna proteintagg. Genom att välja vilken PE‑märkt antikropp som ges skulle läkare i princip kunna rikta om samma sats av CAR T‑celler till olika cancermarkörer, sekventiellt eller flera samtidigt. I laboratorietester dödade dessa PEbody‑CAR T‑celler effektivt leukemi‑ och flera solida tumörcellinjer när matchande märkta antikroppar tillfördes, och de kunde omlokaliseras till nya markörer när den första försvann.
En säkerhetsbrytare med ljus och läkemedel
För ökad säkerhet lade teamet till ett lagerat kontrollsystem som låter dem slå på CAR‑uttrycket bara där och när det behövs. De använde en tvådelad genetisk strömbrytare som först svarar på ett vanligt läkemedel, tamoxifen, och sedan på blått ljus. Endast T‑celler som ser båda signalerna aktiverar en rekombinasenzym som permanent slår på CAR‑genen. Denna ”drogstyrda ljusaktivering” begränsar kraftfull CAR‑aktivitet till belysta tumörområden. I cellodling steg CAR‑nivåer och tumördödande markant i T‑celler exponerade för både tamoxifen och ljus, medan celler i mörker eller utan läkemedel förblev tysta. I möss drev samma system stark genaktivering endast i tumörer på den sida av kroppen som fick ljus, med försumbar aktivitet på den skuggade sidan.
Träningscenter inne i tumören
Som ett steg vidare separerade forskarna tumörsensing från tumördödande. De använde en andra konstruerad receptor, kallad synNotch, som slår på PEbody‑CAR endast efter att en T‑cell möter en särskild markör, en trunkerad version av CD19, placerad på tumörceller. Den markören finns inte naturligt utan induceras lokalt av samma drog‑och‑ljussystem. Endast tumörceller som får ljussignalen börjar visa denna träningsmarkör. När synNotch‑T‑celler anländer fungerar de markerade cellerna som ”träningscenter”, aktiverar många T‑celler och utrustar dem med PEbody‑CARs. När de väl är tränade kan dessa T‑celler sedan attackera den bredare tumörmassan med hjälp av PE‑märkta antikroppar mot vanliga tumörmarkörer såsom PD‑L1 eller PSMA, även på celler som aldrig uttryckte träningsmarkören.
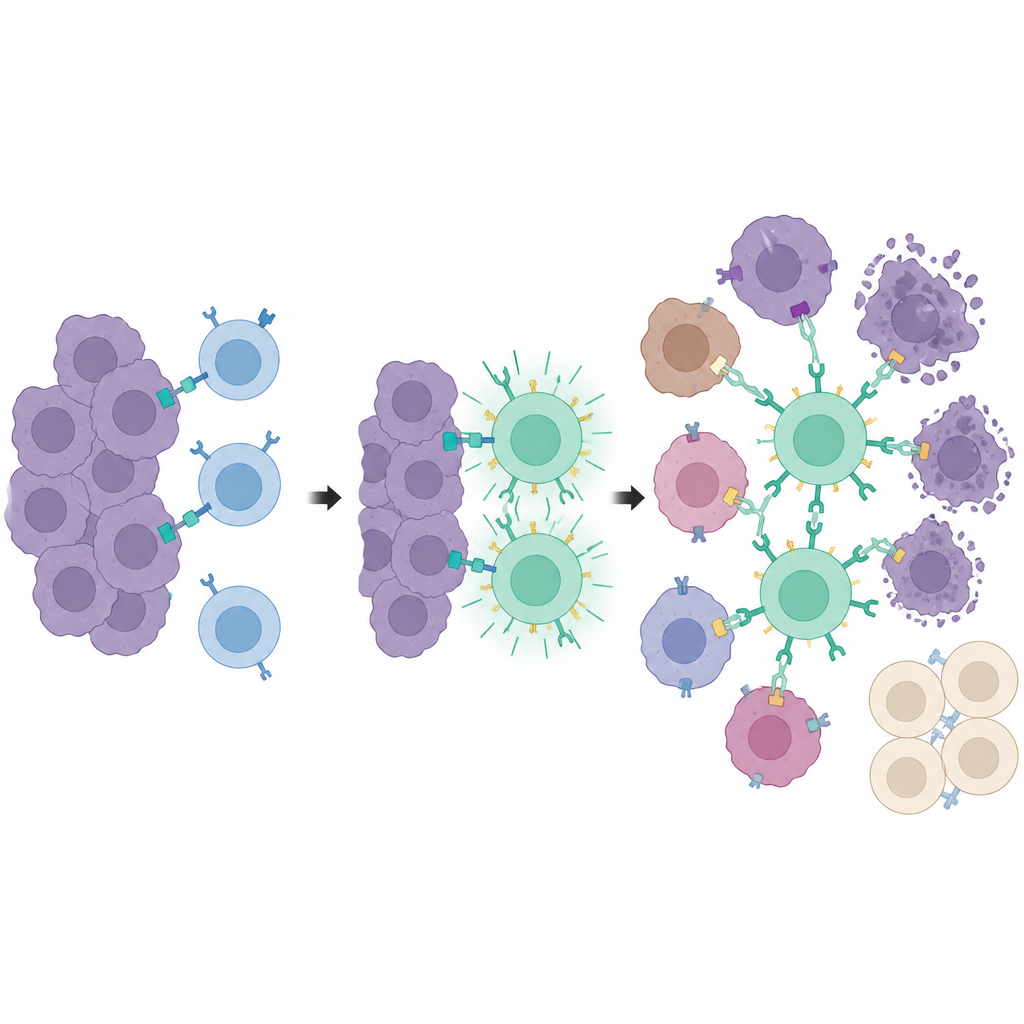
Lokalt angrepp med sparade avlägsna vävnader
I flera musmodeller för bröst‑ och prostatacancer ledde kombinationen av drog, ljus och synNotch‑systemet till stark tumörkontroll på belysta platser. Tumörer som fick tamoxifen och ljus, följt av programmerbara T‑celler och PE‑märkta antikroppar, krympte eller växte mycket långsammare än obelysta tumörer i samma djur. Viktigt är att T‑cellerna cirkulerade i hela kroppen men endast var fullt aktiverade inom de ljus‑primade tumörerna, vilket begränsade skador på andra organ som bar samma ytmolekyler. Jämfört med en konventionell CAR T‑behandling riktad mot PSMA‑markören uppnådde den nya strategin liknande tumörkontroll med mindre viktminskning, lägre inflammatoriska signaler och minskade tecken på leverskada.
Vad detta kan innebära för framtidens cancervård
För en allmän läsare är huvudidén att forskarna har byggt ett slags universellt, omskrivbart CAR T‑system med ett inbyggt lokalt säkerhetslås. Valet av märkta antikroppar bestämmer vilka tumöregenskaper som ska riktas, så läkare skulle kunna anpassa behandlingen allteftersom en cancer utvecklas utan att bygga om T‑cellerna från grunden. Samtidigt hjälper drog‑och‑ljus‑ samt träningscenterdesignen att säkerställa att full T‑cellsattackkraft frigörs endast inne i tumören, inte i friska vävnader som delar samma markörer. Mycket arbete återstår innan detta närmar sig patientbehandling, men studien skisserar en flexibel ritning för säkrare, mer anpassningsbara cellterapier mot komplexa solida tumörer.
Citering: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
Nyckelord: CAR T‑celler, solida tumörer, optogenetik, antigenflykt, syntetisk immunterapi