Clear Sky Science · it
Ingegnerizzare l’abbinamento programmabile tra CAR e antigene tramite attivazione farmacologica e luminosa
Insegnare alle cellule immunitarie a cacciare con più intelligenza
Molti hanno sentito parlare delle cellule CAR T, una forma di terapia personalizzata contro il cancro che riprogramma le cellule immunitarie del paziente per attaccare i tumori. Queste terapie funzionano bene per alcuni tumori del sangue, ma hanno incontrato difficoltà contro i tumori solidi come quelli al seno, alla prostata o al polmone. Questo studio descrive un nuovo modo per affinare e al tempo stesso contenere le cellule CAR T, così che possano riconoscere meglio la varietà delle cellule tumorali risparmiando i tessuti sani.
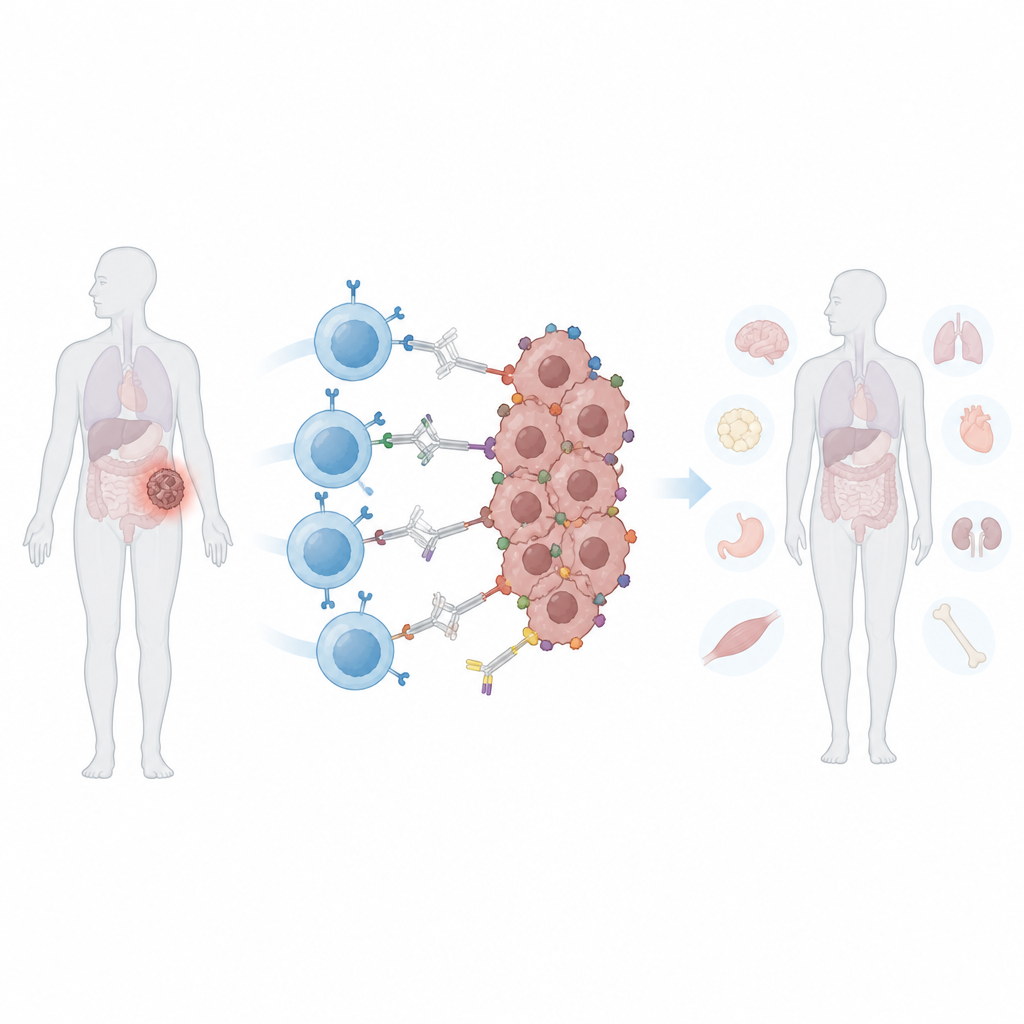
La sfida dei tumori che cambiano forma
Le CAR T convenzionali sono progettate per riconoscere una specifica “bandiera” molecolare sulle cellule cancerose. I tumori solidi spesso eludono questo attacco in due modi. Innanzitutto, possono perdere o ridurre quella bandiera, un processo chiamato fuga antigenica, permettendo ad alcune cellule di sopravvivere e far ricrescere il tumore. In secondo luogo, cellule diverse all’interno dello stesso tumore possono mostrare bandiere diverse, un problema noto come eterogeneità. Ampliare le CAR T per riconoscere più bandiere può aiutare, ma aumenta anche il rischio che attacchino tessuti normali che condividono quegli stessi marcatori. Una volta infuse, le CAR T convenzionali sono sempre attive, rendendo difficile per i medici modulare la loro attività se compaiono effetti collaterali.
Una presa universale per mirare molti tipi di tumore
I ricercatori hanno creato una CAR “programmabile” che non si lega direttamente alle cellule tumorali. Invece riconosce una proteina sicura e fortemente colorata chiamata ficoeritrina, comunemente usata negli alimenti e nei test di laboratorio. Hanno ingegnerizzato un piccolo dominio legante di origine umana, chiamato PEbody, sulla CAR in modo che si agganci a qualsiasi anticorpo porti questa etichetta proteica. Scegliendo quale anticorpo con tag PE infondere, i medici potrebbero in teoria reindirizzare lo stesso lotto di CAR T verso diversi marcatori tumorali, uno dopo l’altro o anche più simultaneamente. Nei test in vitro, queste CAR T con PEbody hanno ucciso efficacemente linee cellulari di leucemia e più tumori solidi quando venivano fornite con gli anticorpi etichettati corrispondenti, e potevano essere reindirizzate verso nuovi marcatori quando il primo veniva perso.
Un interruttore di sicurezza a luce e farmaco
Per migliorare la sicurezza, il team ha aggiunto un sistema di controllo a più livelli che permette di attivare l’espressione della CAR solo dove e quando necessario. Hanno usato un interruttore genetico a due componenti che risponde prima a un farmaco comune, il tamoxifene, e poi alla luce blu. Solo le cellule T che vedono entrambi i segnali attivano un enzima recombinasi che accende permanentemente il gene della CAR. Questa “attivazione luminosa controllata dal farmaco” limita l’attività potente delle CAR alle regioni tumorali illuminate. in colture cellulari, i livelli di CAR e la capacità di uccidere il tumore aumentavano nettamente nelle T esposte sia al tamoxifene che alla luce, mentre le cellule al buio o senza il farmaco restavano quiescenti. Nei topi, lo stesso sistema ha indotto una forte attivazione genica solo nei tumori dal lato del corpo che riceveva la luce, con attività trascurabile sul lato in ombra.
Centri di addestramento all’interno del tumore
Facendo un passo oltre, i ricercatori hanno separato il riconoscimento del tumore dall’attività citotossica. Hanno usato un secondo recettore ingegnerizzato, chiamato synNotch, che accende la CAR con PEbody solo dopo che una cellula T incontra un marcatore speciale, una versione troncata della CD19, posizionata sulle cellule tumorali. Quel marcatore non è naturalmente presente ma viene indotto localmente dallo stesso sistema a base di farmaco e luce. Solo le cellule tumorali che ricevono il segnale luminoso iniziano a esporre questo marcatore di addestramento. Quando le T synNotch arrivano, quelle cellule marcate fungono da “centri di addestramento”, attivando molte T ed equipaggiandole con le CAR PEbody. Una volta addestrate, queste T possono poi attaccare l’intera massa tumorale usando anticorpi con tag PE diretti contro marcatori comuni come PD-L1 o PSMA, anche su cellule che non hanno mai espresso il marcatore di addestramento.
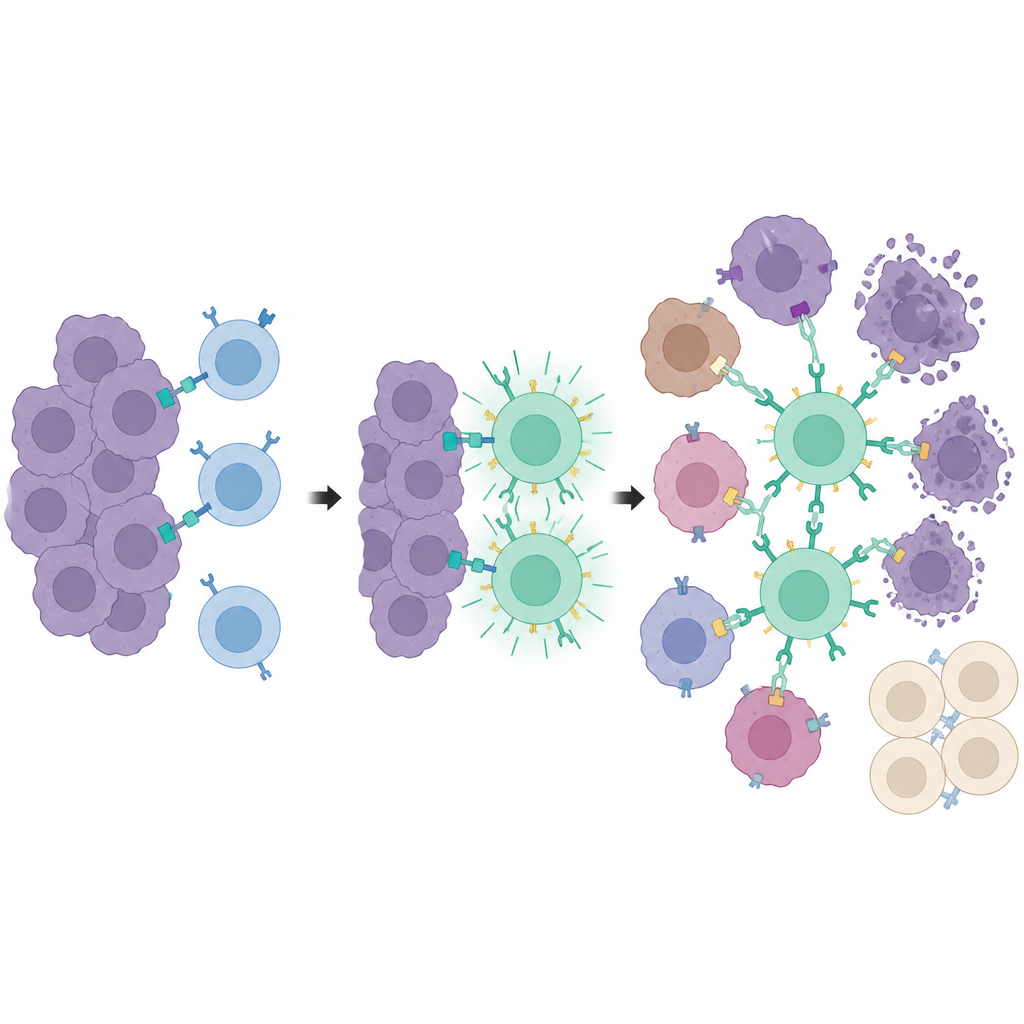
Attacco locale con tessuti distanti risparmiati
In diversi modelli murini di tumore al seno e alla prostata, il sistema combinato di farmaco, luce e synNotch ha portato a un forte controllo tumorale nei siti illuminati. I tumori che hanno ricevuto tamoxifene e luce, seguiti dalle T programmabili e dagli anticorpi con tag PE, si sono ridotti o sono cresciuti molto più lentamente rispetto ai tumori non illuminati nello stesso animale. È importante che le cellule T circolassero in tutto il corpo ma fossero pienamente attivate solo nei tumori primati dalla luce, limitando i danni ad altri organi che portavano gli stessi marcatori superficiali. Rispetto a una terapia CAR T convenzionale diretta contro il marcatore PSMA, la nuova strategia ha ottenuto un controllo tumorale simile con minore perdita di peso, segnali infiammatori ridotti e minori segni di danno epatico.
Cosa potrebbe significare per la cura del cancro in futuro
Per il lettore non specialista, l’idea chiave è che i ricercatori hanno costruito una sorta di sistema CAR T universale e riscrivibile con un blocco di sicurezza locale incorporato. La scelta degli anticorpi etichettati decide quali caratteristiche del tumore mirare, quindi i medici potrebbero adattare la terapia man mano che il cancro evolve senza dover ricostruire le cellule T da zero. Allo stesso tempo, il design basato su farmaco e luce e sui centri di addestramento aiuta a garantire che la piena potenza d’attacco delle T venga scatenata soltanto all’interno del tumore, non nei tessuti sani che condividono gli stessi marcatori. Sebbene resti ancora molto lavoro prima che questo approccio raggiunga i pazienti, lo studio delinea un progetto flessibile per terapie cellulari più sicure e adattabili contro tumori solidi complessi.
Citazione: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
Parole chiave: Cellule CAR T, tumori solidi, optogenetica, fuga antigenica, immunoterapia sintetica