Clear Sky Science · he
הנדסת התאמת CAR הניתנת לתכנות וזיהוי אנטיגן דרך הפעלה באור הנשלט על-ידי תרופה
להכשיר תאי חיסון לצייד חכם יותר
רבים שמעו על תאי CAR T, סוג של טיפול סרטני מותאם אישית שמתכנת מחדש את תאי החיסון של המטופל כדי לתקוף גידולים. טיפולים אלה מצליחים היטב בחלק מסוגי סרטן הדם, אך התקשו נגד גידולים מוצקים כמו שד, ערמונית או ריאה. המחקר מתאר גישה חדשה שמחדדת ומגבילה את פעילות תאי CAR T כך שיוכלו לזהות טוב יותר תאי גידול מגוונים ובו‑זמנית לשמור על רקמות בריאות.
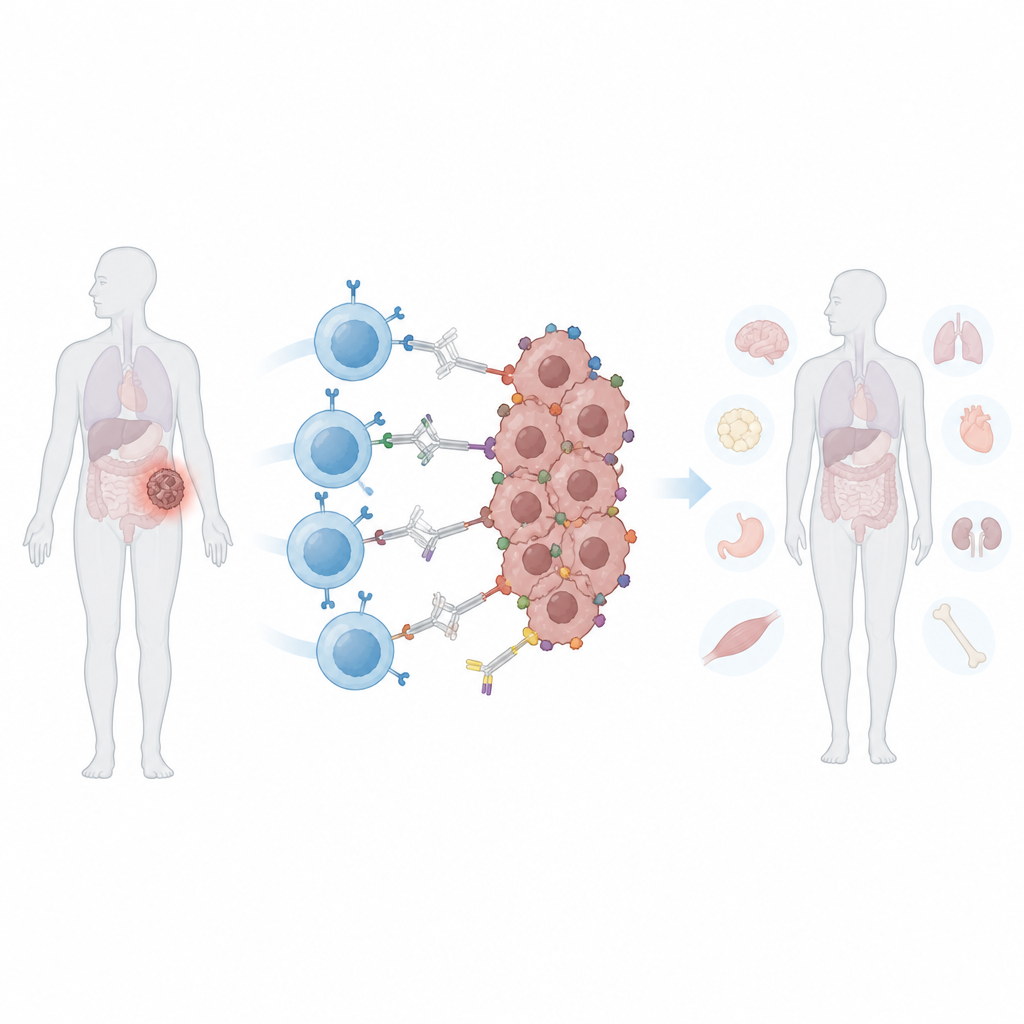
האתגר של גידולים שמשתנים צורה
תאי CAR T סטנדרטיים בנויים לזהות דגל מולקולרי ספציפי אחד על תאי הסרטן. גידולים מוצקים לעיתים מתחמקים מהתקפה זו בשני אופנים. ראשית, הם עלולים לאבד או להוריד את הביטוי של אותו דגל — תהליך הנקרא בריחת אנטיגן — המאפשר לתאים מסוימים לשרוד ולהשיב את הגידול. שנית, תאים שונים באותו גידול עשויים להציג דגלים שונים, בעיה המכונה הטרוגניות. הרחבת זיהוי ה‑CAR למספר דגלים יכולה לעזור, אך גם מעלה את הסיכון שהתאים יתנגשו ברקמות נורמליות החולקות סמנים אלה. לאחר הזרקת תאי CAR T קונבנציונליים, הם פועלים תמיד, מה שמקשה על הרופאים לכוונן את פעילותם אם מופיעים תופעות לוואי.
תקע אוניברסלי למיקוד במגוון סוגי גידול
החוקרים יצרו CAR "ניתן לתכנות" שאינו נקשר ישירות לתאי הגידול. במקום זאת, הוא מזהה חלבון בטוח ובוהק בשם פיקואיריתרין (phycoerythrin), המשמש לעתים במאכלים ובבדיקות מעבדה. הם הניסו תחום קשירה קטן ממקור אנושי, שנקרא PEbody, על ה‑CAR כך שהוא נצמד לכל נוגדן הנושא את תג החלבון הזה. על‑ידי בחירת הנוגדן המסומן ב‑PE להזרקה, ניתן לכאורה להפנות את אותה קבוצת תאי CAR T לסמנים סרטניים שונים, אחד אחרי השני או מספר במקביל. בניסויים במעבדה, תאי PEbody CAR T השמידו ביעילות תאי לוקמיה וקווי תאים של מספר גידולים מוצקים כאשר סופקו הנוגדנים המתאימים, והם יכלו להיות ממוקדים מחדש לסמן חדש כאשר הסמן הראשון אבד.
מתג בטיחות בעזרת אור ותרופה
להגברת הבטיחות, הצוות הוסיף מערכת בקרה מורכבת שמאפשרת להפעיל ביטוי CAR רק במקום ובזמן שרוצים. הם השתמשו במתג גנטי דו‑חלקי המגיב תחילה לתרופה נפוצה, טמוקסיפן, ואחר כך לאור כחול. רק תאי T שרואים את שני האותות מפעילים אנזים רקומבינאז שמדלג באופן קבוע על גן ה‑CAR ומדליק אותו. "הפעלה באור הנשלטת על‑ידי תרופה" זו מגבילה את פעילות ה‑CAR החזקה לאזורים מוארים בגידול. בתרבית תאים, רמות ה‑CAR וההריגה הגידולית עלו באופן חד בתאים שנחשפו גם לטמוקסיפן וגם לאור, בעוד שתאים בחושך או ללא התרופה נשארו שקטים. בעכברים, אותה מערכת הובילה להפעלה גנטית חזקה רק בגידולים בצד הגוף שקבלו אור, עם פעילות מזערית בצד שמוצל.
מרכזי אימון בתוך הגידול
החוקרים עשו צעד נוסף והפרידו בין חישה של הגידול להריגה שלו. הם השתמשו בקולטן מהונדס שני, שנקרא synNotch, שמדליק את ה‑PEbody CAR רק לאחר ש‑T מגיע לתא גידול הנושא סמן מיוחד — גרסה מקוצרת של CD19 — המושבתת על תאי הגידול. סמן זה עצמו אינו קיים בטבע אלא מובן מקומית על‑ידי אותה מערכת תרופה‑ואור. רק תאים סרטניים שמקבלים את אות האור מתחילים להציג את סמן ה"הכשרה" הזה. כאשר תאי synNotch מגיעים, אותם תאים מסומנים משמשים כ"מרכזי אימון", מפעילים המון תאי T ומציידים אותם ב‑PEbody CARs. לאחר ההכשרה, תאים אלה יכולים לתקוף את מסת הגידול הרחבה יותר באמצעות נוגדנים מסומנים ב‑PE נגד סמני גידול נפוצים כמו PD‑L1 או PSMA, אפילו על תאים שמעולם לא הביעו את סמן ההכשרה.
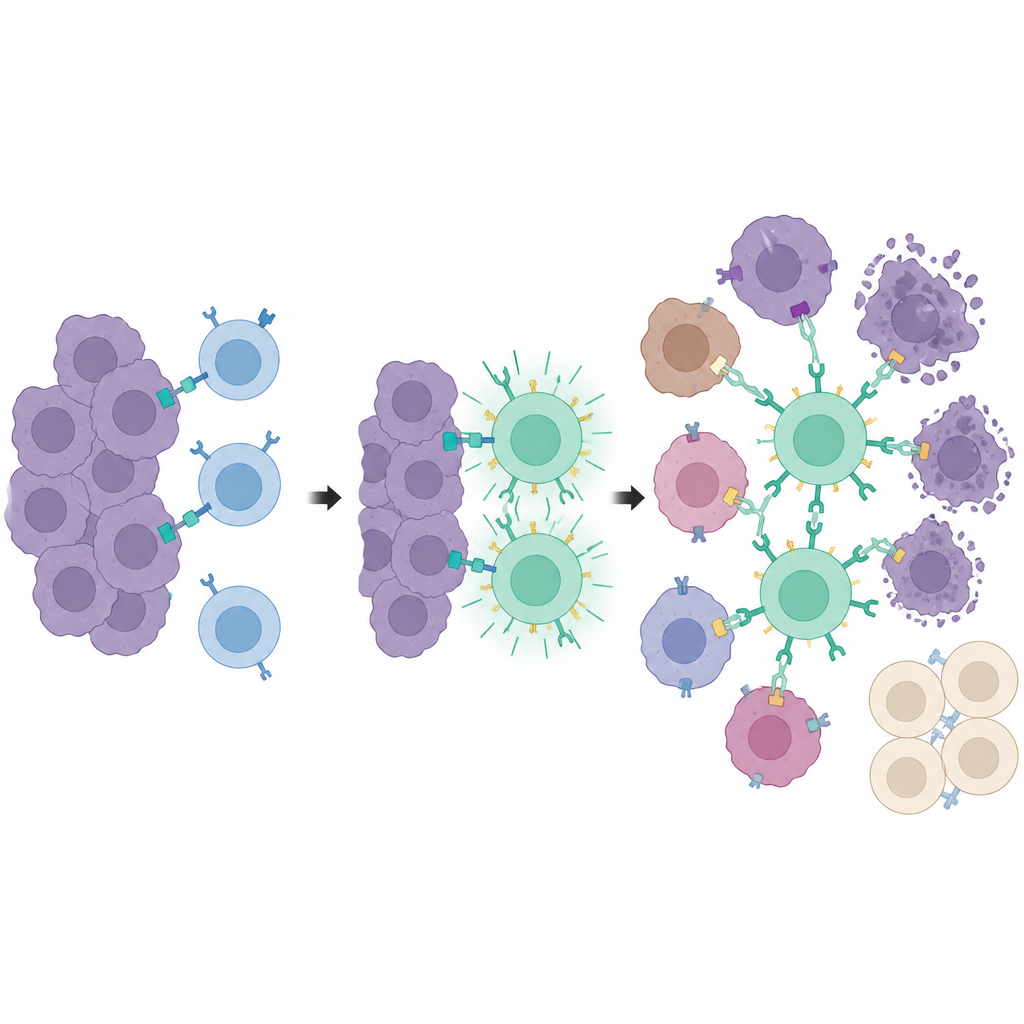
מתקפה מקומית כשרקמות מרוחקות נשמרות
מספר מודלים של עכברים עם גידולי שד וערמונית הראו שהשילוב של תרופה, אור ומערכת synNotch הוביל לשליטה חזקה על הגידול באתרים המוארים. גידולים שקיבלו טמוקסיפן ואור, ואחריהם תאי T ניתנים‑לתכנות ונוגדנים מסומנים ב‑PE, הצטמצמו או גדלו הרבה יותר לאט מאשר גידולים לא מוארים באותו בעל חיים. חשוב מכך, תאי ה‑T נסעו ברחבי הגוף אך הופעלו במלואם רק בתוך הגידולים שהוכנו באור, ובכך הוגבל הנזק לאיברים אחרים שנשאו את אותם סמנים על פני השטח. בהשוואה לטיפול CAR T קונבנציונלי המכוון לנגן PSMA, האסטרטגיה החדשה השיגה שליטה דומה על הגידול תוך פחות אובדן משקל, אותות דלקת נמוכים יותר והפחתה בסימני נזק לכבד.
מה המשמעות של זה לטיפול עתידי בסרטן
לקריאה שאינה מקצועית, הרעיון המרכזי הוא שהחוקרים בנו מעין מערכת CAR T אוניברסלית וקלה לשכתוב עם מנעול בטיחות מקומי מובנה. בחירת הנוגדנים המסומנים קובעת אילו תכונות של הגידול למקד, כך שהרופאים עשויים להתאים את הטיפול ככל שהסרטן משתנה מבלי לבנות מחדש את תאי ה‑T. בו‑זמנית, עיצוב התרופה‑והאור ומרכזי‑האימון מסייע להבטיח שכוח המתקפה המלא של תאי ה‑T משתחרר רק בתוך הגידול, לא ברקמות בריאות החולקות את אותם סמנים. למרות שיש עוד עבודה רבה עד לגישה זו תגיע לחולים, המחקר מציג מתווה גמיש לטיפולי תאים בטוחים וגמישים יותר נגד גידולים מוצקים מורכבים.
ציטוט: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
מילות מפתח: תאי CAR T, גידולים מוצקים, אופטוגנטיקה, בריחת אנטיגן, אימונותרפיה סינתטית