Clear Sky Science · tr
İlaçla kapılı ışık aktivasyonu yoluyla programlanabilir CAR ve antijen eşleştirmesinin mühendisliği
Bağışıklık hücrelerini daha akıllıca avlanmaya öğretmek
Birçok kişi, bir hastanın kendi bağışıklık hücrelerini tümörlere saldıracak şekilde yeniden programlayan kişiselleştirilmiş bir kanser tedavisi türü olan CAR T hücrelerini duymuştur. Bu tedaviler bazı kan kanserlerinde iyi sonuç verirken, meme, prostat veya akciğer gibi katı tümörlere karşı zorlanmıştır. Bu çalışma, CAR T hücrelerini hem keskinleştirmenin hem de sınırlamanın yeni bir yolunu tanımlar; böylece çeşitli tümör hücrelerini daha iyi bulup sağlıklı dokuları koruyabilirler.
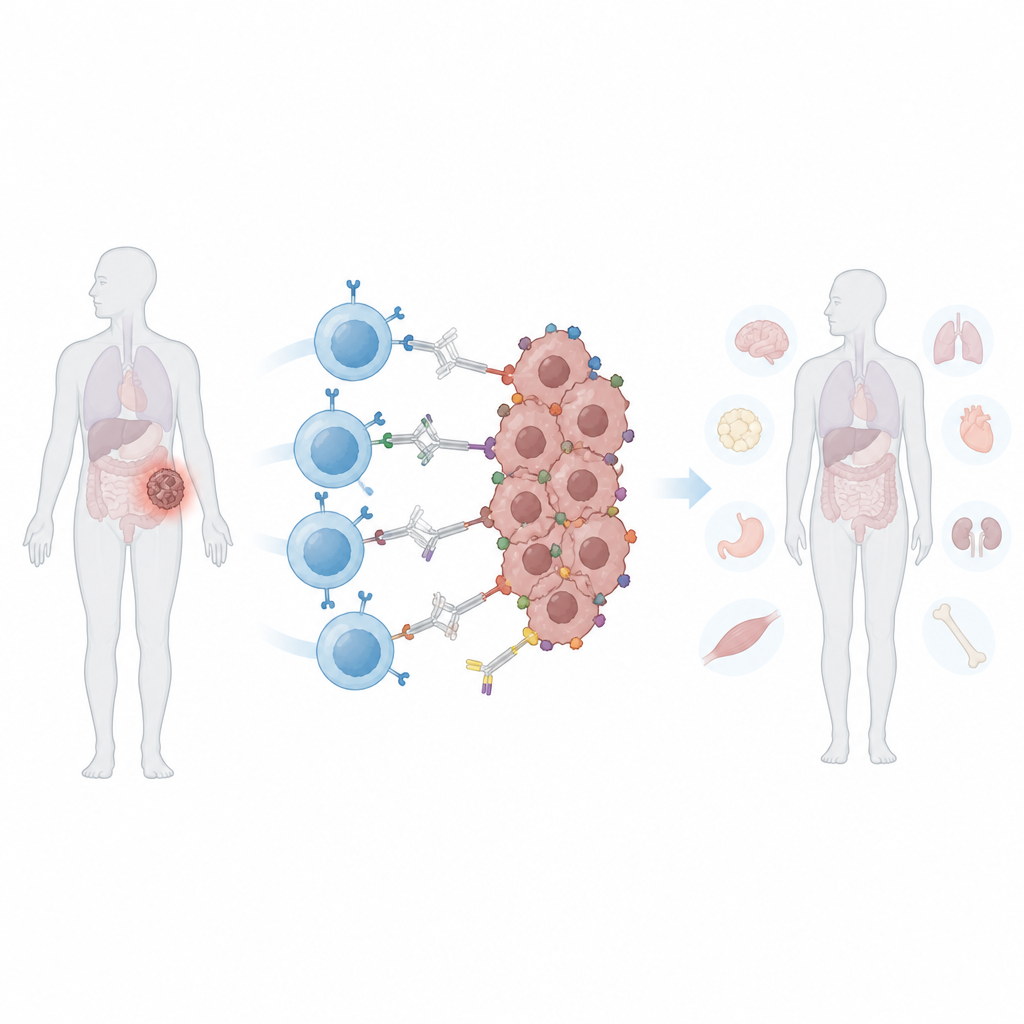
Şekil değiştiren tümörlerin zorluğu
Standart CAR T hücreleri kanser hücrelerindeki tek bir spesifik moleküler “bayrağı” tanımak üzere tasarlanır. Katı tümörler genellikle bu saldırıdan iki yolla kaçınır. Birincisi, bu bayrağı kaybedebilir veya azaltabilirler; buna antijen kaçışı denir ve bazı hücrelerin hayatta kalıp tümörü yeniden büyütmesine izin verir. İkincisi, aynı tümör içindeki farklı hücreler farklı bayraklar gösterebilir; bu probleme heterojenite denir. CAR T hücrelerini daha fazla bayrağı tanıyacak şekilde genişletmek yardımcı olabilir, ancak bu aynı işaretleri paylaşan normal dokulara saldırma riskini de artırır. Geleneksel CAR T hücreleri verildiğinde sürekli aktiftir, bu da yan etkiler ortaya çıkarsa doktorların etkinliklerini açıp kapamasını zorlaştırır.
Birçok tümör tipine hedef oluşturan evrensel fiş
Araştırmacılar, tümör hücrelerine doğrudan bağlanmayan “programlanabilir” bir CAR geliştirdiler. Bunun yerine, gıdalarda ve laboratuvar testlerinde yaygın olarak kullanılan parlak renkli güvenli bir protein olan fizikoretirin (phycoerythrin) adlı bir proteini tanır. CAR üzerine PEbody adı verilen, insan kaynaklı küçük bir bağlanma bölgesi mühendislik ile ekleyip bu protein etiketi taşıyan herhangi bir antikora tutunmasını sağladılar. Hangi PE-etiketli antikorun verileceğini seçerek, aynı CAR T hücresi partisinin sıra ile veya aynı anda birden çok kanser belirtecine yönlendirilebileceği teorik olarak mümkün olur. Laboratuvar testlerinde, uygun etiketli antikorlarla sağlandığında bu PEbody CAR T hücreleri lösemi ve çeşitli katı tümör hücre hatlarını etkin şekilde öldürdü ve ilk hedef kaybolduğunda yeni belirteçlere yeniden hedeflenebildiler.
Bir ışık ve ilaç güvenlik anahtarı
Güvenliği artırmak için ekip, CAR ifadesini yalnızca gerektiği yerde ve zamanda açmalarına izin veren katmanlı bir kontrol sistemi ekledi. İlk önce yaygın bir ilaç olan tamoksifene, ardından mavi ışığa yanıt veren iki parçalı bir genetik anahtar kullandılar. Yalnızca her iki ipucunu da gören T hücreleri, CAR genini kalıcı olarak açan bir rekombinaz enzimini aktive eder. Bu “ilaç kontrollü ışık aktivasyonu” güçlü CAR etkinliğini aydınlatılmış tümör bölgeleriyle sınırlar. Hücre kültüründe, tamoksifen ve ışığa maruz kalan T hücrelerinde CAR seviyeleri ve tümör öldürme belirgin şekilde artarken, karanlıktaki veya ilaçsız hücreler sessiz kaldı. Farelerde aynı sistem, ışık verilen vücut tarafındaki tümörlerde güçlü gen aktivasyonu sürdürürken gölgeli tarafta ihmal edilebilir düzeyde aktivite gösterdi.
Tümör içindeki eğitim merkezleri
Bir adım daha ileri giderek, araştırmacılar tümör algısını tümör öldürmeden ayırdı. Bir T hücresi özel bir belirteçle, tümör hücrelerine konan kısaltılmış bir CD19 versiyonuyla karşılaştıktan sonra PEbody CAR’ı açan synNotch adlı ikinci bir mühendislikli reseptör kullandılar. Bu belirteç kendiliğinden mevcut değildir, ancak aynı ilaç ve ışık sistemiyle yerel olarak indüklenir. Yalnızca ışık sinyali alan tümör hücreleri bu eğitim belirtecini göstermeye başlar. SynNotch T hücreleri geldiğinde, işaretlenmiş bu hücreler “eğitim merkezleri” gibi davranır, birçok T hücresini aktive eder ve onları PEbody CAR’larla donatır. Eğitildikten sonra bu T hücreleri, eğitim belirteci göstermemiş hücrelerde bile PD-L1 veya PSMA gibi yaygın tümör belirteçlerine karşı PE-etiketli antikorlar kullanarak tümörün daha geniş kütlesine saldırabilirler.
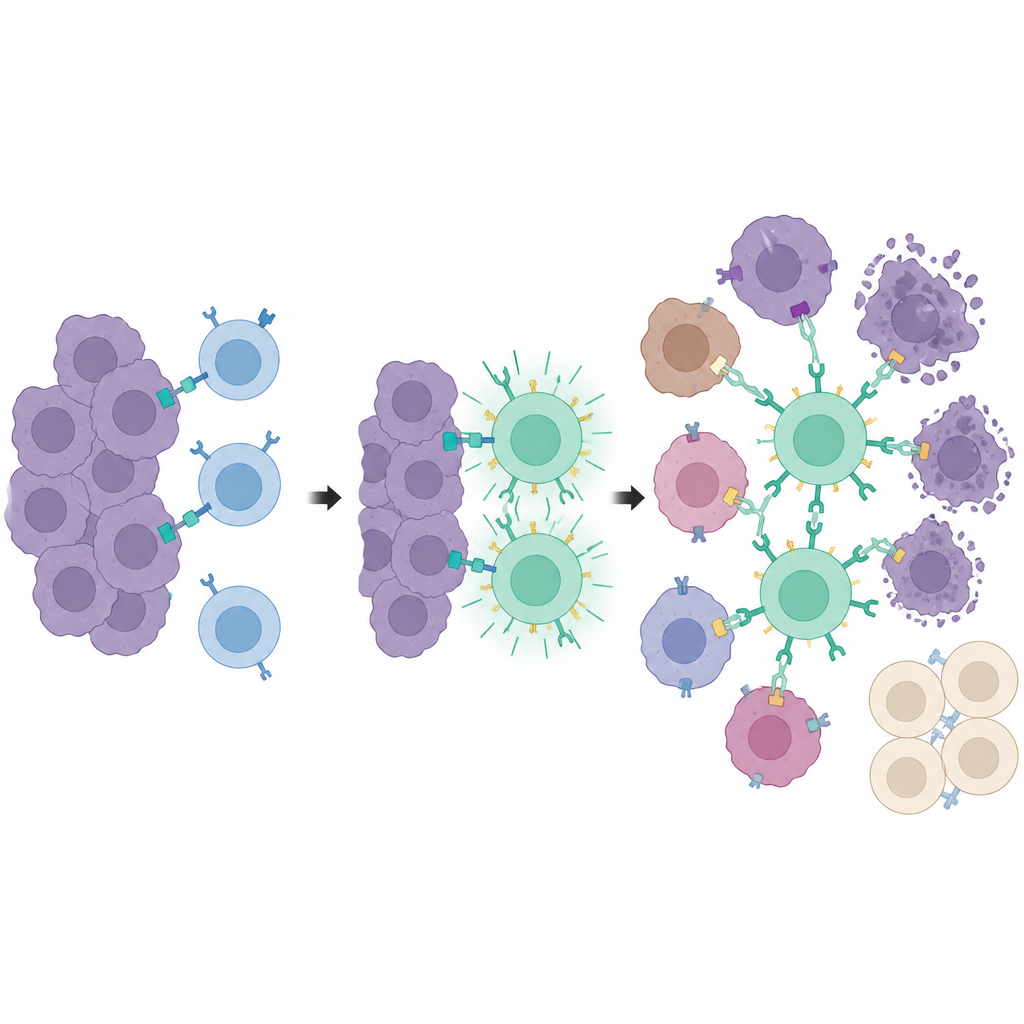
Uzak dokular korunurken yerel saldırı
Meme ve prostat kanserinin birkaç fare modelinde, birleşik ilaç, ışık ve synNotch sistemi aydınlatılmış bölgelerde güçlü tümör kontrolüne yol açtı. Tamoksifen ve ışık alan, ardından programlanabilir T hücreleri ve PE-etiketli antikorlar verilen tümörler, aynı hayvanda aydınlatılmamış tümörlere kıyasla küçüldü veya çok daha yavaş büyüdü. Önemli olarak, T hücreleri vücut boyunca dolaştı ancak yalnızca ışıkla hazırlanmış tümörlerde tam olarak aktive oldu; bu da aynı yüzey belirteçlerini taşıyan diğer organlara zarar verme ihtimalini sınırladı. PSMA belirtecine yöneltilmiş geleneksel bir CAR T tedavisiyle karşılaştırıldığında, yeni strateji benzer tümör kontrolü sağlarken daha az kilo kaybı, daha düşük inflamatuar sinyaller ve azalmış karaciğer hasarı belirtileri gösterdi.
Gelecekteki kanser bakımına olası etkileri
Bir genel okuyucu için ana fikir, araştırmacıların yerleşik bir lokal güvenlik kilidine sahip evrensel, yeniden yazılabilir türde bir CAR T sistemi inşa etmiş olmalarıdır. Etiketli antikorların seçimi hangi tümör özelliklerinin hedefleneceğini belirler; böylece hekimler kanser evrimleştikçe T hücrelerini baştan inşa etmeden tedaviyi uyarlayabilir. Aynı zamanda, ilaç-ışık ve eğitim merkezi tasarımı tam T hücresi saldırı gücünün yalnızca tümör içinde, aynı belirteçleri paylaşan sağlıklı dokularda değil, serbest bırakılmasını sağlamaya yardımcı olur. Bu yaklaşımın hastalara ulaşmasından önce yapılması gereken çok iş olsa da çalışma, karmaşık katı tümörlere karşı daha güvenli, daha uyarlanabilir hücre terapileri için esnek bir taslak sunar.
Atıf: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
Anahtar kelimeler: CAR T hücreleri, katı tümörler, optogenetik, antijen kaçışı, sentetik immünoterapi