Clear Sky Science · fr
Ingénierie d’un appariement programmable CAR–antigène via activation lumineuse contrôlée par médicament
Apprendre aux cellules immunitaires à chasser plus intelligemment
Beaucoup de gens ont entendu parler des cellules CAR T, une forme de traitement personnalisé du cancer qui reprogramme les propres cellules immunitaires du patient pour attaquer les tumeurs. Ces thérapies fonctionnent bien pour certains cancers sanguins mais peinent face aux tumeurs solides comme celles du sein, de la prostate ou du poumon. Cette étude décrit une nouvelle façon d’affiner et de restreindre les CAR T afin qu’elles repèrent mieux des cellules tumorales diverses tout en épargnant les tissus sains.
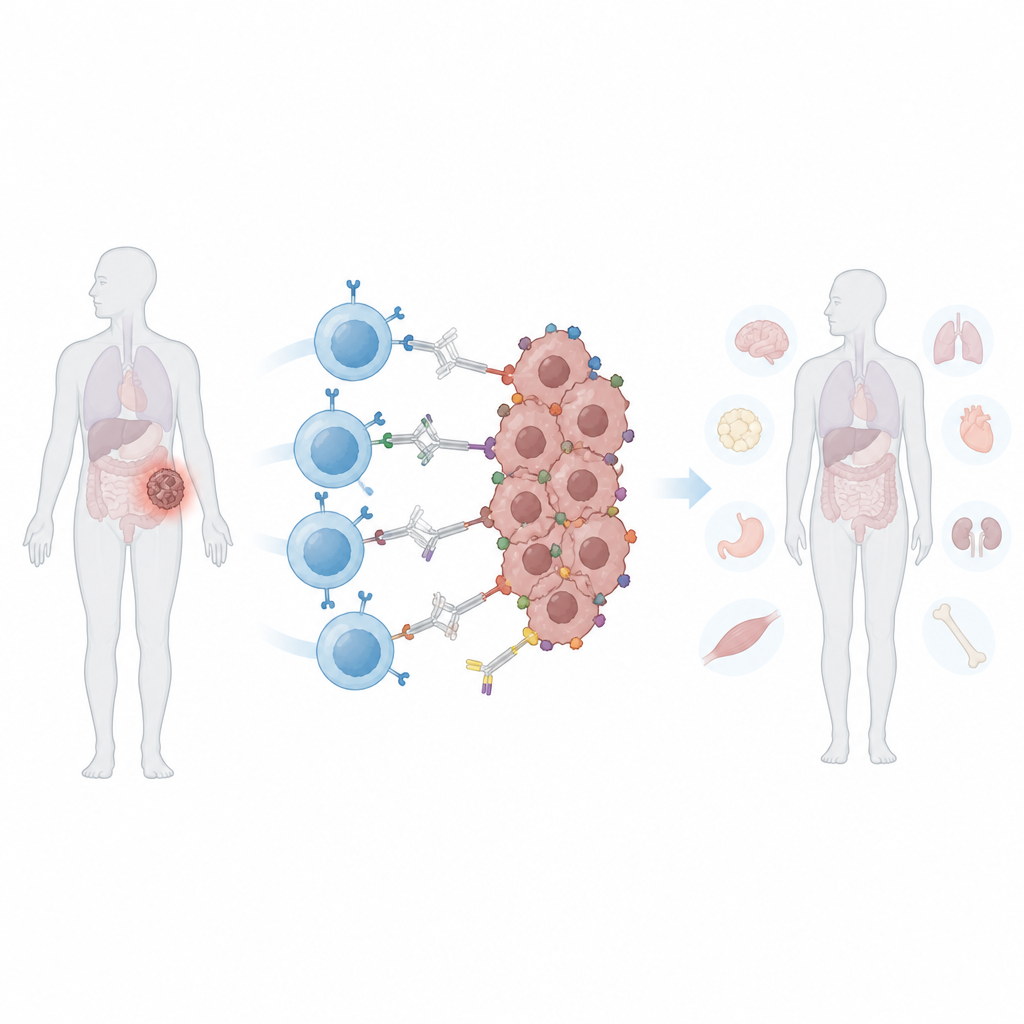
Le défi des tumeurs qui changent de forme
Les CAR T classiques sont conçues pour reconnaître un « drapeau » moléculaire spécifique sur les cellules cancéreuses. Les tumeurs solides échappent souvent à cette attaque de deux manières. D’abord, elles peuvent perdre ou réduire ce drapeau, un processus appelé évasion antigénique, permettant à certaines cellules de survivre et de régénérer la tumeur. Ensuite, différentes cellules au sein d’une même tumeur peuvent afficher des drapeaux différents, un problème connu sous le nom d’hétérogénéité. Élargir la reconnaissance des CAR T à plus de marqueurs peut aider, mais augmente aussi le risque qu’elles attaquent des tissus normaux partageant ces marqueurs. Une fois infusées, les CAR T conventionnelles sont toujours actives, rendant difficile pour les médecins d’ajuster leur activité si des effets secondaires apparaissent.
Une prise universelle pour cibler de nombreux types tumoraux
Les chercheurs ont créé un CAR « programmable » qui ne se lie pas directement aux cellules tumorales. Au lieu de cela, il reconnaît une protéine sûre et très colorée appelée phycoérythrine, couramment utilisée dans l’alimentation et les tests de laboratoire. Ils ont greffé un petit domaine de liaison d’origine humaine, appelé PEbody, sur le CAR afin qu’il s’accroche à tout anticorps portant cette étiquette protéique. En choisissant quel anticorps marqué au PE administrer, les médecins pourraient en principe rediriger le même lot de CAR T vers différents marqueurs tumoraux, successivement ou simultanément. En laboratoire, ces CAR T PEbody ont tué efficacement des lignées de leucémie et de tumeurs solides lorsqu’on leur fournissait des anticorps correspondants marqués, et ils pouvaient être réorientés vers de nouveaux marqueurs lorsque le premier disparaissait.
Un interrupteur de sécurité à la lumière et au médicament
Pour améliorer la sécurité, l’équipe a ajouté un système de contrôle à plusieurs niveaux permettant d’activer l’expression du CAR uniquement là et quand c’est nécessaire. Ils ont utilisé un commutateur génétique en deux parties qui répond d’abord à un médicament courant, le tamoxifène, puis à la lumière bleue. Seules les cellules T exposées aux deux signaux activent une recombinase qui déclenche de façon permanente le gène CAR. Cette « activation lumineuse verrouillée par médicament » confine l’activité puissante du CAR aux régions tumorales illuminées. En culture cellulaire, les niveaux de CAR et la capacité à tuer les tumeurs augmentaient fortement dans les cellules T exposées à la fois au tamoxifène et à la lumière, tandis que les cellules restées dans l’obscurité ou privées du médicament restaient silencieuses. Chez la souris, le même système induisait une activation génique importante uniquement dans les tumeurs du côté du corps éclairé, avec une activité négligeable du côté ombragé.
Centres d’entraînement à l’intérieur de la tumeur
Allant plus loin, les chercheurs ont dissocié la détection tumorale de l’élimination tumorale. Ils ont utilisé un second récepteur modifié, appelé synNotch, qui active le CAR PEbody seulement après qu’une cellule T rencontre un marqueur spécial, une version tronquée de CD19, placée sur les cellules tumorales. Ce marqueur n’est pas naturellement présent mais est induit localement par le même système médicament–lumière. Seules les cellules tumorales recevant le signal lumineux commencent à afficher ce marqueur d’« entraînement ». Lorsque les cellules T synNotch arrivent, ces cellules marquées servent de « centres d’entraînement », activant de nombreuses cellules T et les dotant de CAR PEbody. Une fois entraînées, ces cellules T peuvent alors attaquer la masse tumorale plus large en utilisant des anticorps marqués PE dirigés contre des marqueurs tumoraux courants tels que PD-L1 ou PSMA, même sur des cellules qui n’ont jamais exprimé le marqueur d’entraînement.
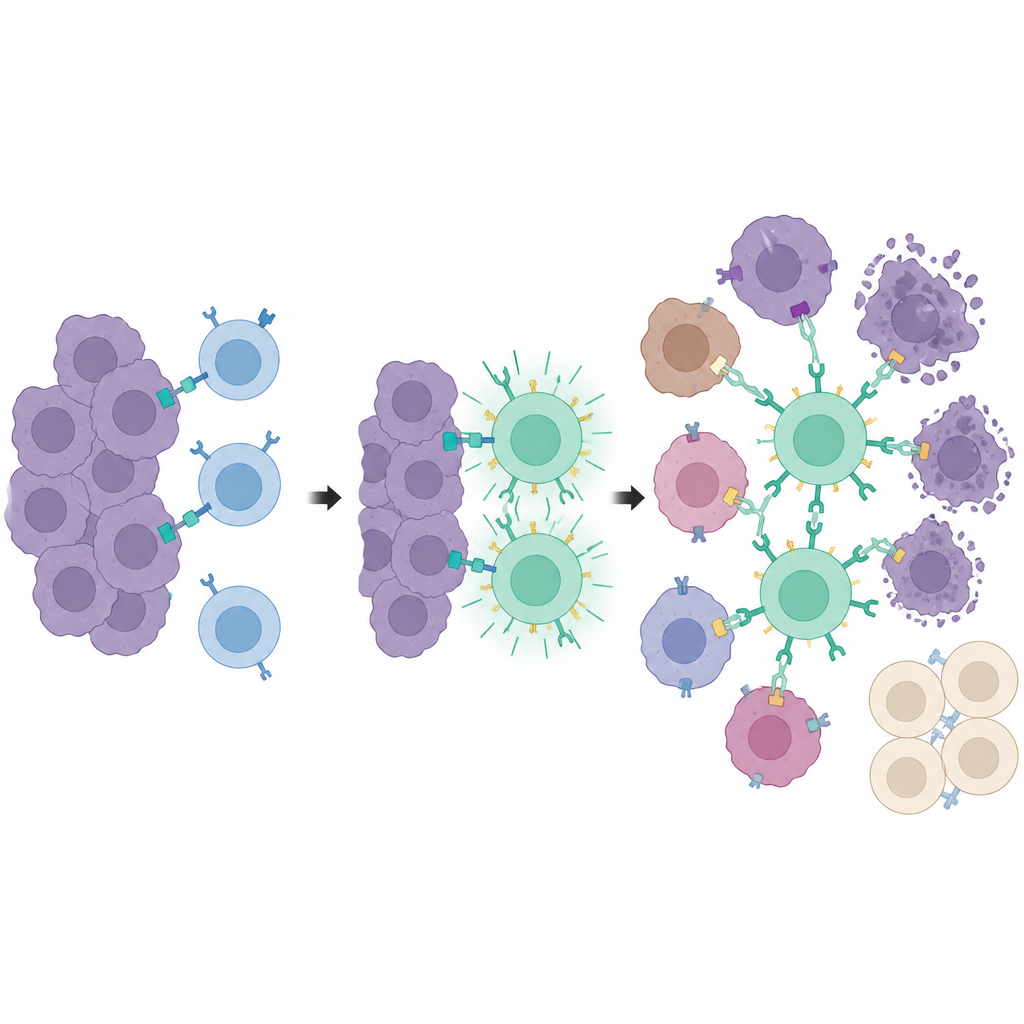
Attaque locale en épargnant les tissus distants
Dans plusieurs modèles murins de cancers du sein et de la prostate, le système combiné médicament, lumière et synNotch a conduit à un contrôle tumoral marqué aux sites illuminés. Les tumeurs ayant reçu tamoxifène et lumière, suivies des cellules T programmables et des anticorps marqués PE, ont diminué ou ont connu une croissance beaucoup plus lente que les tumeurs non éclairées chez le même animal. Il est important de noter que les cellules T circulaient dans tout le corps mais n’étaient pleinement activées que dans les tumeurs amorcées par la lumière, limitant les dommages aux autres organes portant les mêmes marqueurs de surface. Comparée à une thérapie CAR T conventionnelle dirigée contre le marqueur PSMA, la nouvelle stratégie a obtenu un contrôle tumoral comparable avec moins de perte de poids, des signaux inflammatoires plus faibles et des signes réduits de lésions hépatiques.
Ce que cela pourrait signifier pour les soins du cancer à venir
Pour le lecteur non spécialiste, l’idée clé est que les chercheurs ont construit une sorte de système CAR T universel et réinscriptible avec un verrou de sécurité local intégré. Le choix des anticorps marqués détermine quelles caractéristiques tumorales cibler, de sorte que les médecins pourraient adapter le traitement au fur et à mesure de l’évolution d’un cancer sans reconstruire les cellules T depuis zéro. Parallèlement, le design médicament–lumière et les centres d’entraînement contribuent à garantir que la pleine puissance d’attaque des cellules T n’est déclenchée qu’à l’intérieur de la tumeur, et non dans les tissus sains partageant les mêmes marqueurs. Bien qu’il reste beaucoup de travail avant que cette approche n’atteigne les patients, l’étude propose une feuille de route flexible pour des thérapies cellulaires plus sûres et plus adaptables contre des tumeurs solides complexes.
Citation: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
Mots-clés: Cellules CAR T, tumeurs solides, optogénétique, évasion antigénique, immunothérapie synthétique