Clear Sky Science · nl
Programmeerbare CAR en antigeen-koppeling via medicijngestuurde lichtactivatie ontwerpen
Immuuncellen slimmer laten jagen
Veel mensen hebben gehoord van CAR T-cellen, een vorm van gepersonaliseerde kankerbehandeling die de immuuncellen van een patiënt herprogrammeert om tumoren aan te vallen. Deze therapieën werken goed bij sommige bloedkankers, maar hebben moeite met solide tumoren zoals in borst, prostaat of long. Deze studie beschrijft een nieuwe manier om CAR T-cellen zowel scherper als geremter te maken, zodat ze beter diverse tumorcellen kunnen vinden terwijl gezond weefsel gespaard blijft.
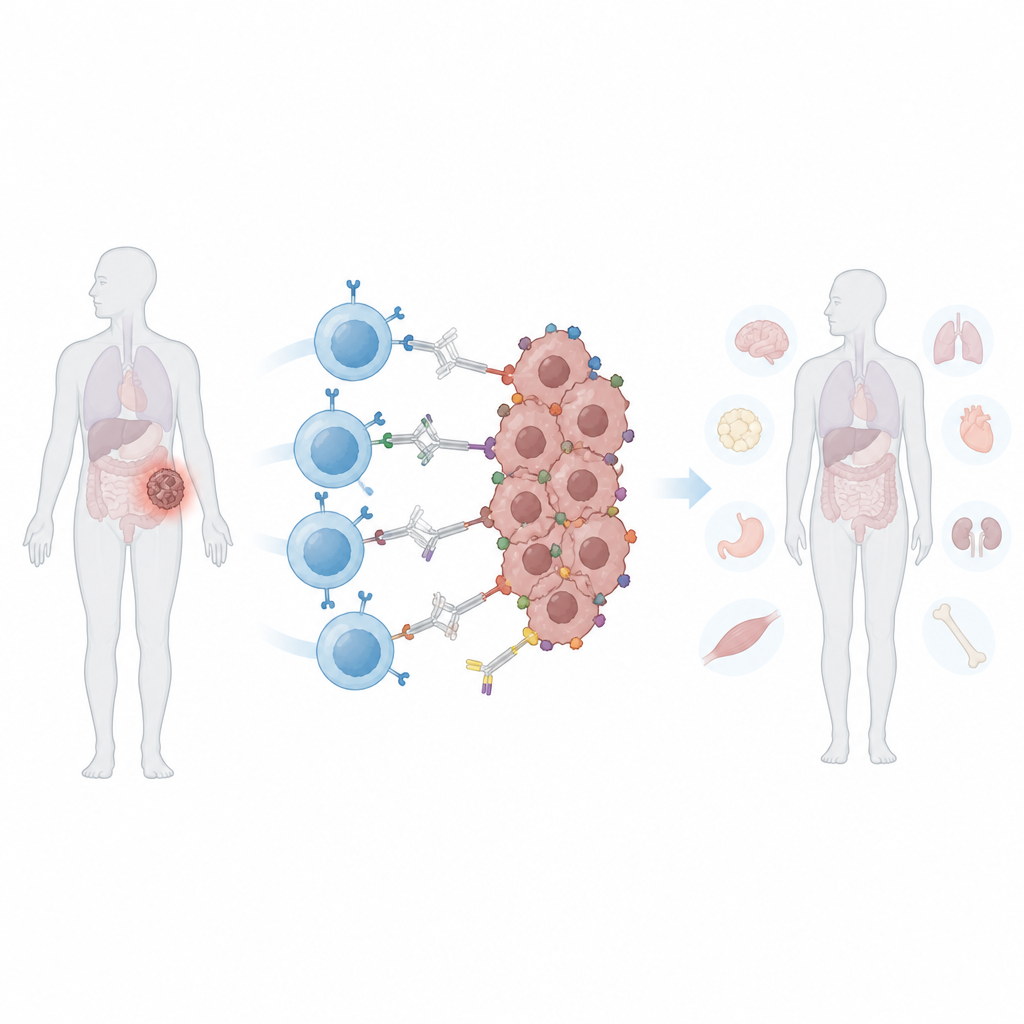
De uitdaging van veranderende tumoren
Conventionele CAR T-cellen zijn ontworpen om één specifiek moleculair “vlaggetje” op kankercellen te herkennen. Solide tumoren ontwijken deze aanval vaak op twee manieren. Ten eerste kunnen ze dat vlaggetje verliezen of minder tot expressie brengen, een proces dat antigeenontsnapping wordt genoemd, waardoor sommige cellen overleven en de tumor kan teruggroeien. Ten tweede tonen verschillende cellen binnen dezelfde tumor verschillende vlaggetjes, een probleem dat heterogeniteit heet. Het uitbreiden van CAR T-cellen om meer vlaggetjes te herkennen kan helpen, maar vergroot ook het risico dat ze normaal weefsel aanvallen dat die merkers deelt. Zodra conventionele CAR T-cellen zijn geïnfusioneerd, staan ze constant aan, waardoor het moeilijk is voor artsen om hun activiteit op of neer te schroeven als bijwerkingen optreden.
Een universele aansluiting voor veel tumorsoorten
De onderzoekers creëerden een “programmeerbare” CAR die niet direct aan tumorcellen bindt. In plaats daarvan herkent hij een veilige, felgekleurde eiwitlabel genaamd fycoerythrine, die vaak in voedingsmiddelen en laboratoriumtests wordt gebruikt. Ze bouwden een klein, mensafgeleid bindingsdomein, een PEbody genoemd, op de CAR zodat het zich hecht aan elk antilichaam dat dit proteïnetag draagt. Door te kiezen welk PE-getagd antilichaam te infuseren, zouden artsen in principe dezelfde partij CAR T-cellen kunnen herleiden naar verschillende kankermarkers, na elkaar of meerdere tegelijk. In laboratoriumtests doodden deze PEbody CAR T-cellen efficiënt leukemie- en verschillende solide tumorlijnen wanneer de overeenkomende getagde antilichamen werden geleverd, en ze konden worden hergericht op nieuwe markers wanneer de eerste verloren ging.
Een veiligheidschakelaar met licht en medicatie
Om de veiligheid te vergroten voegde het team een gelaagd regelsysteem toe waarmee ze CAR-expressie alleen daar en wanneer nodig kunnen inschakelen. Ze gebruikten een tweeledige genetische schakelaar die eerst reageert op een veelgebruikt medicijn, tamoxifen, en vervolgens op blauw licht. Alleen T-cellen die beide signalen zien, activeren een recombinase-enzym dat het CAR-gen permanent aanzet. Deze “medicijn-gated lichtactivatie” beperkt krachtige CAR-activiteit tot verlichte tumorgebieden. In celkweek stegen CAR-niveaus en tumoruitroeiing scherp in T-cellen die zowel tamoxifen als licht kregen, terwijl cellen in het donker of zonder medicatie stil bleven. In muizen zorgde hetzelfde systeem voor sterke genactivatie alleen in tumoren aan de kant van het lichaam die licht kreeg, met verwaarloosbare activiteit aan de beschaduwde kant.
Opleidingscentra binnen de tumor
De onderzoekers gingen een stap verder en scheidden tumorwaarneming van tumoruitroeiing. Ze gebruikten een tweede gemodificeerde receptor, synNotch genaamd, die de PEbody CAR pas inschakelt nadat een T-cel een speciaal merkje ontmoet, een ingekorte versie van CD19, op tumorcellen geplaatst. Dat merkje is zelf niet natuurlijk aanwezig maar wordt lokaal geïnduceerd door hetzelfde medicijn-en-lichtsysteem. Alleen tumorcellen die het lichtsignaal ontvangen, beginnen dit trainingsmerkje te tonen. Wanneer synNotch T-cellen arriveren, fungeren die gemarkeerde cellen als “opleidingscentra”, ze activeren veel T-cellen en rusten ze uit met PEbody CARs. Eenmaal getraind kunnen deze T-cellen vervolgens de bredere tumormassa aanvallen met PE-getagde antilichamen tegen veelvoorkomende tumormerkers zoals PD-L1 of PSMA, zelfs op cellen die nooit het trainingsmerkje hebben geëtaleerd.
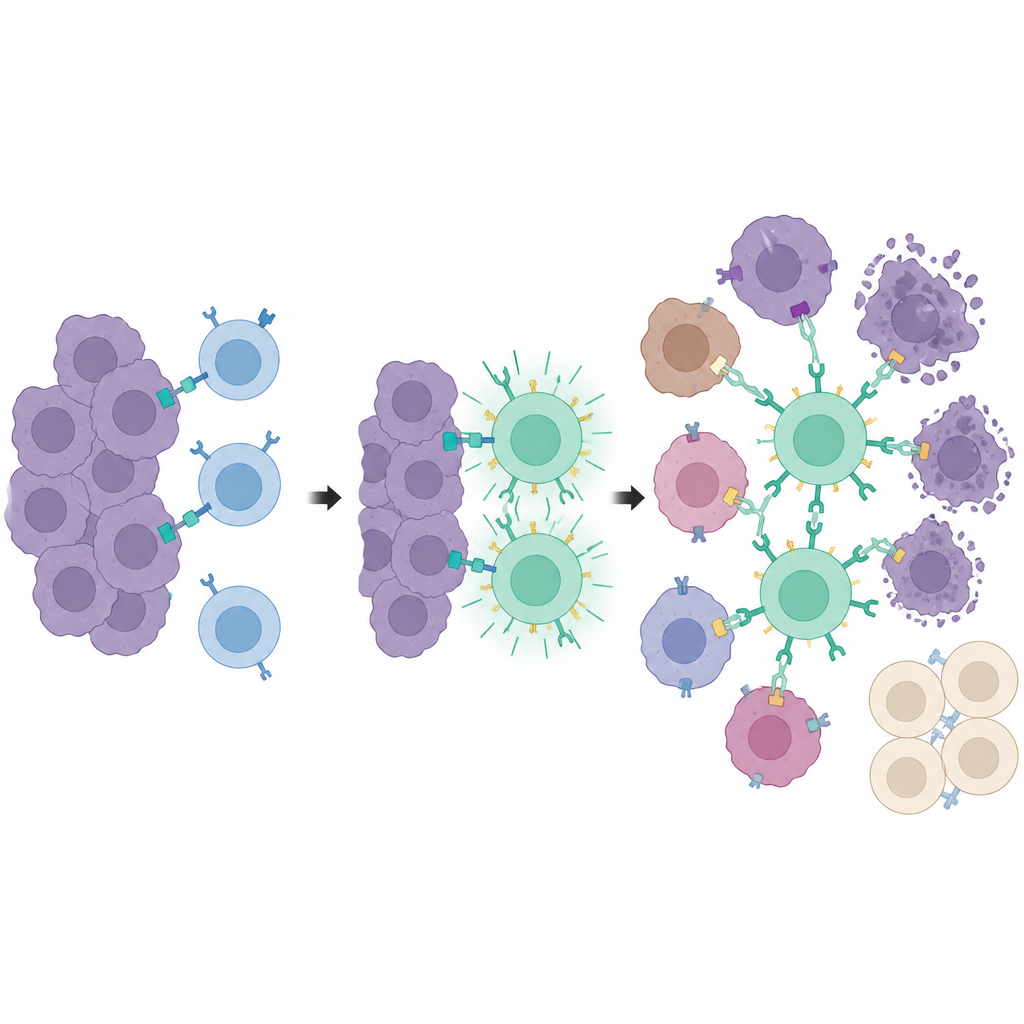
Lokale aanval met gespaarde verre weefsels
In meerdere muismodellen van borstkanker en prostaatkanker leidde het gecombineerde medicijn-, licht- en synNotch-systeem tot sterke tumorcontrole op verlichte locaties. Tumoren die tamoxifen en licht kregen, gevolgd door programmeerbare T-cellen en PE-getagde antilichamen, krimpten of groeiden veel langzamer dan onbelichte tumoren in hetzelfde dier. Belangrijk is dat de T-cellen door het hele lichaam circuleerden maar alleen volledig werden geactiveerd binnen de licht-geprimeerde tumoren, waardoor schade aan andere organen die dezelfde oppervlaktemerkers droegen werd beperkt. Vergeleken met een conventionele CAR T-behandeling gericht op de PSMA-marker, bereikte de nieuwe strategie vergelijkbare tumorcontrole met minder gewichtsverlies, lagere ontstekingssignalen en verminderde tekenen van leverschade.
Wat dit kan betekenen voor toekomstige kankerzorg
Voor een niet-specialistische lezer is de kernidee dat de onderzoekers een soort universeel, herschrijfbaar CAR-T-systeem hebben gebouwd met een ingebouwde lokale veiligheidsvergrendeling. De keuze van getagde antilichamen bepaalt welke tumorkenmerken worden gericht, zodat artsen de behandeling zouden kunnen aanpassen naarmate een kanker evolueert zonder de T-cellen helemaal opnieuw te hoeven bouwen. Tegelijk helpt het medicijn-en-licht- en opleidingscentrumontwerp verzekeren dat de volledige aanvallende kracht van T-cellen alleen binnen de tumor vrijkomt, niet in gezonde weefsels die dezelfde merkers delen. Hoewel er nog veel werk te doen is voordat deze benadering patiënten bereikt, schetst de studie een flexibel stappenplan voor veiligere, beter aanpasbare celtherapieën tegen complexe solide tumoren.
Bronvermelding: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
Trefwoorden: CAR T-cellen, solide tumoren, optogenetica, antigeenontsnapping, synthetische immunotherapie