Clear Sky Science · pl
Inżynieria programowalnego połączenia CAR i antygenu za pomocą aktywacji lekiem i światłem
Nauka komórek odpornościowych sprytniejszego polowania
Wiele osób słyszało o komórkach CAR T, rodzaju spersonalizowanej terapii przeciwnowotworowej, która przeprogramowuje własne komórki odpornościowe pacjenta do atakowania guzów. Terapie te dobrze działają w niektórych nowotworach krwi, ale mają trudności z guzami litymi, takimi jak nowotwory piersi, prostaty czy płuc. W tym badaniu opisano nowy sposób zarówno na wyostrzenie, jak i ograniczenie aktywności komórek CAR T, tak aby lepiej odnajdywały różnorodne komórki nowotworowe, oszczędzając przy tym tkanki zdrowe.
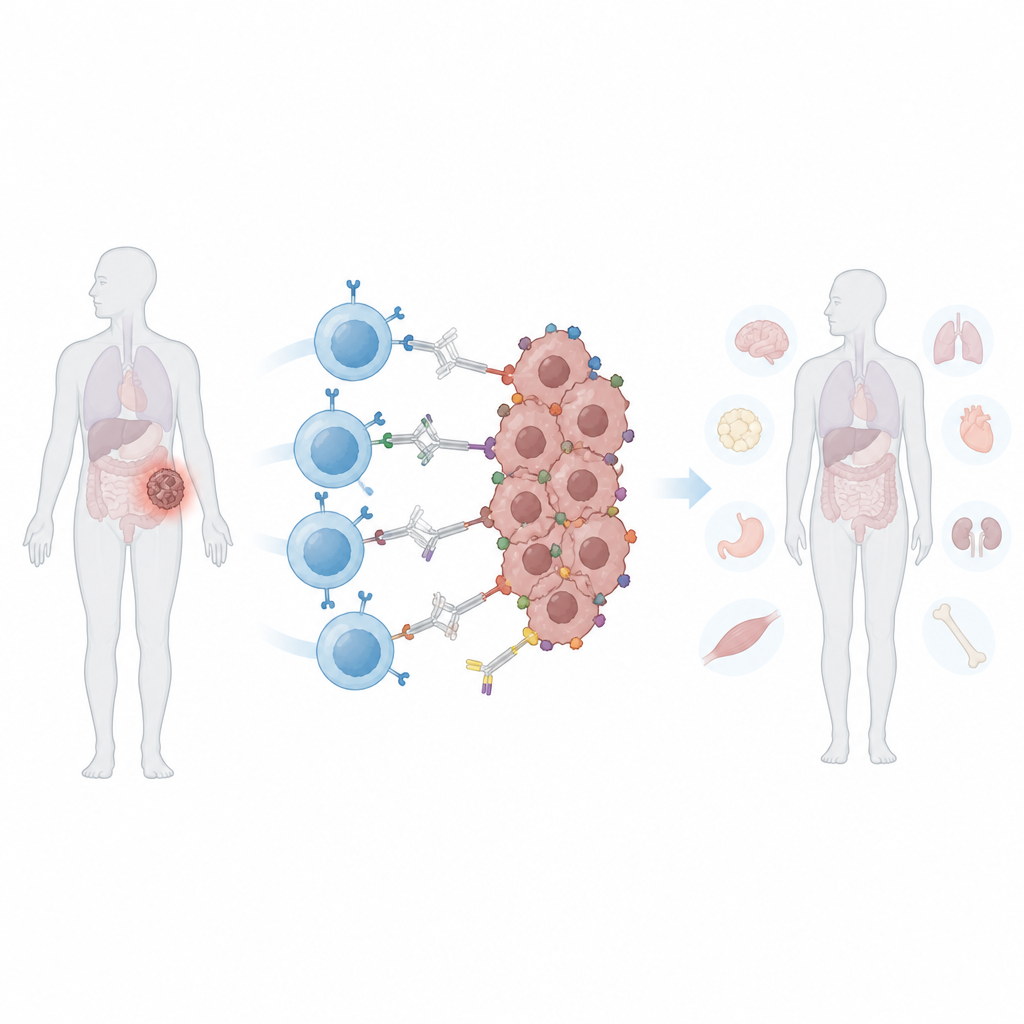
Wyzwanie ze zmieniającymi się kształtami guzów
Standardowe komórki CAR T są zaprojektowane do rozpoznawania jednego specyficznego molekularnego „znaku” na komórkach nowotworowych. Guzy lite często unikają tego ataku na dwa sposoby. Po pierwsze, mogą utracić lub zmniejszyć ekspresję tego znaku, proces nazywany ucieczką przed antygenem, co pozwala niektórym komórkom przetrwać i odtworzyć guz. Po drugie, różne komórki w tym samym guzie mogą prezentować różne znaki, problem znany jako heterogeniczność. Rozszerzenie rozpoznawania przez komórki CAR T na więcej znaków może pomóc, ale zwiększa też ryzyko ataku na normalne tkanki, które dzielą te markery. Po podaniu konwencjonalnych komórek CAR T są one stale aktywne, co utrudnia lekarzom regulację ich działania w przypadku wystąpienia działań niepożądanych.
Uniwersalne gniazdo do celowania w wiele typów guzów
Naukowcy stworzyli „programowalny” CAR, który nie wiąże się bezpośrednio z komórkami nowotworowymi. Zamiast tego rozpoznaje bezpieczne, intensywnie zabarwione białko zwane fykoerytryną, powszechnie stosowane w żywności i testach laboratoryjnych. Zmodyfikowali małą, pochodzącą od człowieka domenę wiążącą, nazwaną PEbody, i umieścili ją na CAR, dzięki czemu przyczepia się ona do każdego przeciwciała niosącego ten znacznik białkowy. Poprzez wybór, które przeciwciało z tagiem PE podać, lekarze mogliby w zasadzie przekierować tę samą partię komórek CAR T na różne markery nowotworowe, jedno po drugim lub kilka jednocześnie. W testach laboratoryjnych te komórki PEbody CAR T skutecznie zabijały linie komórek białaczki i wielu guzów litych, gdy dostarczono odpowiednie znakowane przeciwciała, i mogły zostać ponownie skierowane na nowe markery, gdy pierwszy zniknął.
Wyłącznik bezpieczeństwa oparty na świetle i leku
Aby poprawić bezpieczeństwo, zespół dodał wielowarstwowy system kontroli pozwalający włączać ekspresję CAR tylko tam i wtedy, gdy jest to potrzebne. Użyto dwuczęściowego przełącznika genetycznego, który reaguje najpierw na powszechny lek, tamoksyfen, a następnie na światło niebieskie. Tylko komórki T, które otrzymają oba sygnały, aktywują enzym rekombinazy, który trwale włącza gen CAR. Ta „aktywacja świetlna bramkowana lekiem” ogranicza silną aktywność CAR do naświetlonych obszarów guza. W hodowlach komórkowych poziomy CAR i zabijanie guza wzrastały gwałtownie w komórkach T wystawionych zarówno na tamoksyfen, jak i światło, podczas gdy komórki na ciemno lub bez leku pozostawały ciche. U myszy ten sam system powodował silną aktywację genu tylko w guzach po tej stronie ciała, która otrzymała światło, z minimalną aktywnością po stronie zacienionej.
Centra szkoleniowe wewnątrz guza
Idąc o krok dalej, badacze oddzielili wykrywanie guza od jego niszczenia. Zastosowali drugi zmodyfikowany receptor, nazwany synNotch, który włącza PEbody CAR dopiero po tym, gdy komórka T napotka specjalny znacznik — skróconą wersję CD19 — umieszczony na komórkach nowotworowych. Sam ten znacznik nie występuje naturalnie, lecz jest indukowany lokalnie przez ten sam system leku i światła. Tylko komórki nowotworowe otrzymujące sygnał świetlny zaczynają prezentować ten szkoleniowy marker. Gdy docierają komórki synNotch T, oznaczone komórki działają jako „centra szkoleniowe”, aktywując wiele komórek T i wyposażając je w PEbody CARy. Po przeszkoleniu te komórki T mogą następnie atakować szerszą masę guza przy użyciu przeciwciał z tagiem PE skierowanych przeciw powszechnym markerom nowotworowym, takim jak PD-L1 czy PSMA, nawet na komórkach, które nigdy nie wyrażały markera szkoleniowego.
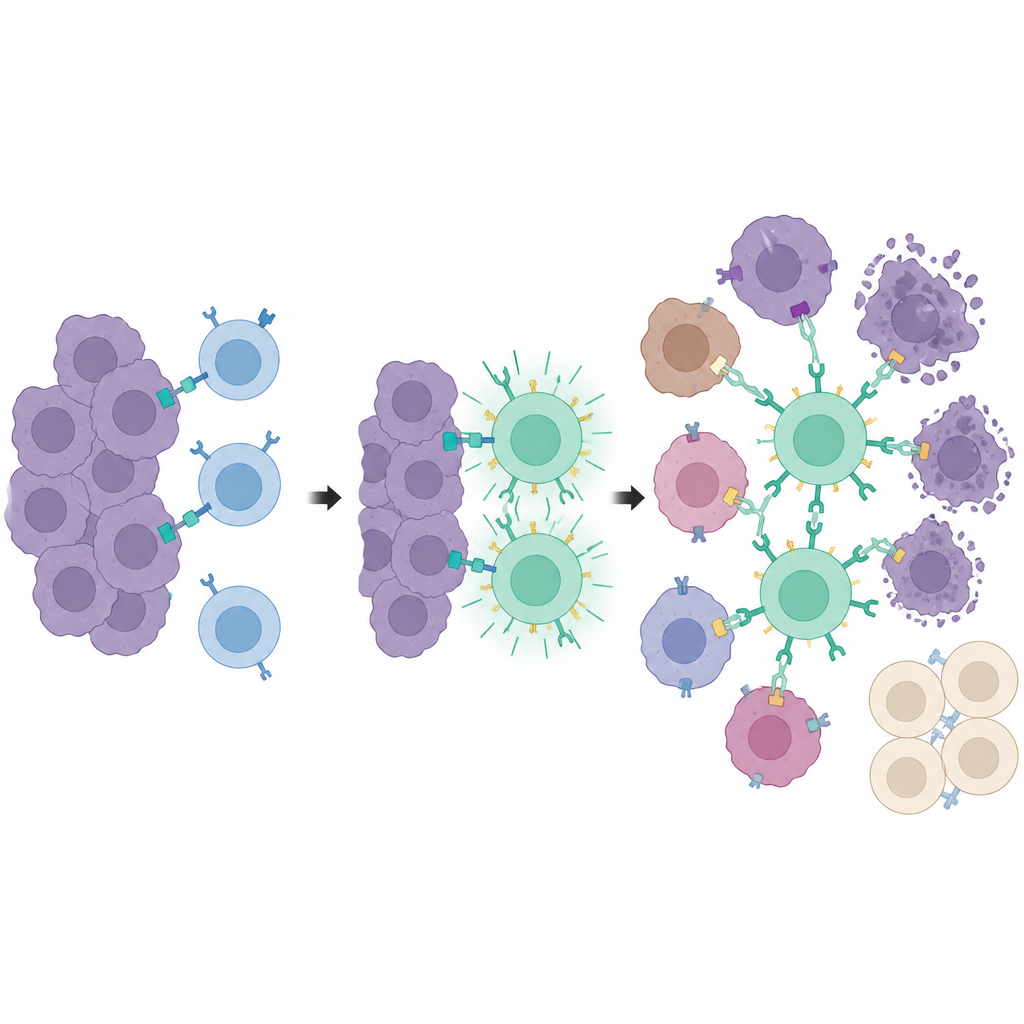
Miejscowy atak przy oszczędzaniu tkanek odległych
W kilku modelach mysich raka piersi i prostaty połączony system leku, światła i synNotch prowadził do silnej kontroli guza w naświetlonych miejscach. Guzy, które otrzymały tamoksyfen i światło, a następnie programowalne komórki T i przeciwciała z tagiem PE, zmniejszały się lub rosły znacznie wolniej niż nieoświetlone guzy w tym samym zwierzęciu. Co ważne, komórki T krążyły po całym organizmie, ale były w pełni aktywowane tylko w naświetlonych, uprzednio przygotowanych guzach, ograniczając uszkodzenia innych narządów noszących te same markery powierzchniowe. W porównaniu z konwencjonalnym leczeniem CAR T skierowanym przeciw markerowi PSMA, nowa strategia osiągnęła podobną kontrolę guza przy mniejszej utracie masy ciała, niższych sygnałach zapalnych i mniejszych oznakach uszkodzenia wątroby.
Co to może znaczyć dla przyszłej opieki onkologicznej
Dla czytelnika nieznającego tematu kluczową ideą jest to, że naukowcy zbudowali rodzaj uniwersalnego, przepisowego systemu CAR T z wbudowanym lokalnym zamkiem bezpieczeństwa. Wybór znakowanych przeciwciał decyduje, jakie cechy guza będą celowane, więc lekarze mogliby dostosowywać leczenie w miarę ewolucji nowotworu bez konieczności przebudowy komórek T od podstaw. Jednocześnie projekt oparty na leku, świetle i centrach szkoleniowych pomaga zapewnić, że pełna siła ataku limfocytów T zostanie uwolniona tylko wewnątrz guza, a nie w zdrowych tkankach dzielących te same markery. Choć przed zastosowaniem u pacjentów wciąż pozostaje wiele pracy, badanie przedstawia elastyczny plan działania dla bezpieczniejszych, bardziej adaptowalnych terapii komórkowych przeciw złożonym guzom litym.
Cytowanie: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
Słowa kluczowe: komórki CAR T, guzy lity, opto-genetyka, ucieczka przed antygenem, syntetyczna immunoterapia