Clear Sky Science · de
Programmierbare CAR- und Antigen-Paarung durch medikamentengesteuerte Lichtaktivierung
Immunsystemzellen schlauer jagen lehren
Viele Menschen haben von CAR‑T‑Zellen gehört, einer Form personalisierter Krebstherapie, bei der die körpereigenen Immunzellen eines Patienten so umprogrammiert werden, dass sie Tumore angreifen. Diese Therapien sind bei einigen Blutkrebsarten sehr erfolgreich, hatten aber bei soliden Tumoren wie Brust-, Prostata‑ oder Lungenkrebs Schwierigkeiten. Diese Studie beschreibt einen neuen Ansatz, CAR‑T‑Zellen sowohl zu schärfen als auch zu begrenzen, damit sie vielfältige Tumorzellen besser finden können und gleichzeitig gesundes Gewebe schonen.
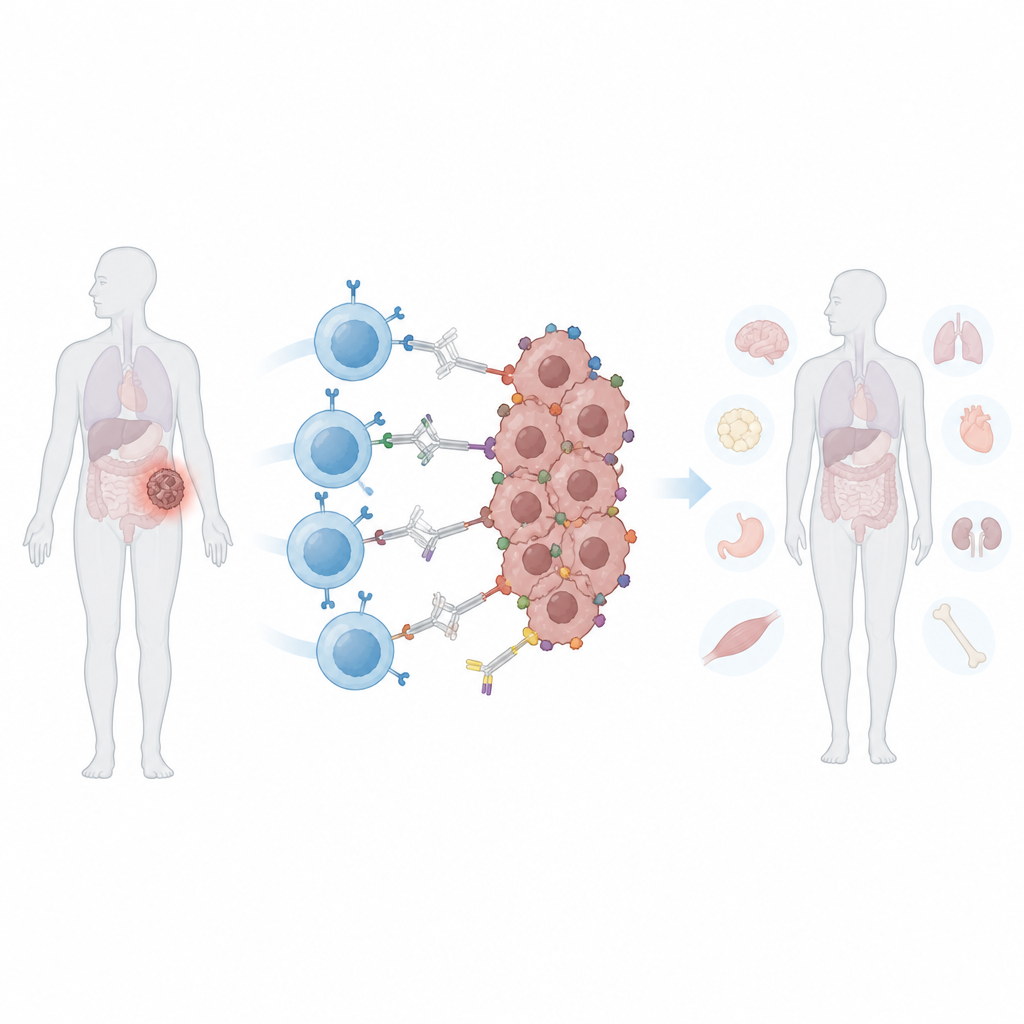
Die Herausforderung formwandelnder Tumore
Konventionelle CAR‑T‑Zellen sind darauf ausgelegt, eine spezifische molekulare „Flagge“ auf Krebszellen zu erkennen. Solide Tumoren entziehen sich dieser Attacke oft auf zwei Arten. Erstens können sie diese Flagge verlieren oder herabregulieren — ein Prozess, der als Antigenentweichung bezeichnet wird und es einigen Zellen erlaubt, zu überleben und den Tumor neu wachsen zu lassen. Zweitens zeigen unterschiedliche Zellen innerhalb desselben Tumors oft unterschiedliche Marker, ein Problem, das als Heterogenität bekannt ist. CAR‑T‑Zellen auf mehrere Marker auszuweiten kann helfen, erhöht aber auch das Risiko, dass sie gesundes Gewebe angreifen, das diese Marker teilt. Einmal infundiert, sind herkömmliche CAR‑T‑Zellen dauerhaft aktiv, was es Ärzten erschwert, ihre Aktivität bei Nebenwirkungen zu modulieren.
Ein universeller Anschluss für viele Tumortypen
Die Forschenden entwickelten einen „programmierbaren“ CAR, der sich nicht direkt an Tumorzellen bindet. Stattdessen erkennt er ein sicheres, leuchtend gefärbtes Protein namens Phycoerythrin, das häufig in Lebensmitteln und Laboranwendungen verwendet wird. Sie bauten eine kleine, aus menschlichem Material abgeleitete Bindedomäne, eine sogenannte PEbody, auf den CAR, sodass dieser an jeden Antikörper andockt, der mit diesem Protein markiert ist. Durch die Wahl des infundierten PE‑markierten Antikörpers könnten Ärzte grundsätzlich denselben CAR‑T‑Zell‑Satz auf unterschiedliche Krebsmarker ausrichten — nacheinander oder gleichzeitig. In Laborversuchen töteten diese PEbody‑CAR‑T‑Zellen effizient Leukämie‑ und mehrere Zelllinien solider Tumoren, wenn passende markierte Antikörper vorlagen, und sie konnten neu ausgerichtet werden, wenn der erste Marker verloren ging.
Ein Sicherheits‑Schalter aus Licht und Medikament
Zur Erhöhung der Sicherheit fügten die Autorinnen und Autoren ein geschichtetes Kontrollsystem hinzu, das CAR‑Expression nur dort und dann einschaltet, wo sie benötigt wird. Sie verwendeten einen zweiteiligen genetischen Schalter, der zuerst auf ein häufiges Medikament, Tamoxifen, reagiert und dann auf blaues Licht. Nur T‑Zellen, die beide Signale sehen, aktivieren eine Rekombinase‑Enzymatik, die das CAR‑Gen dauerhaft einschaltet. Diese „medikamentengegate Lichtaktivierung“ beschränkt die starke CAR‑Aktivität auf beleuchtete Tumorregionen. In Zellkultur stiegen CAR‑Spiegel und Tumorkontrolle stark in T‑Zellen an, die sowohl Tamoxifen als auch Licht ausgesetzt waren, während Zellen im Dunkeln oder ohne Medikament ruhig blieben. In Mäusen führte dasselbe System zu starker Genaktivierung ausschließlich in Tumoren an der beleuchteten Körperseite, mit vernachlässigbarer Aktivität auf der beschatteten Seite.
Trainingszentren im Tumor
Einen Schritt weiter getrennten die Forschenden Tumorerkennung und Tumorzerstörung. Sie nutzten einen zweiten konstruierten Rezeptor, genannt synNotch, der den PEbody‑CAR erst einschaltet, nachdem eine T‑Zelle auf ein spezielles Markermolekül trifft — eine verkürzte Version von CD19 —, das auf Tumorzellen platziert wurde. Dieser Marker ist natürlicherweise nicht vorhanden, sondern wird lokal durch dasselbe Medikament‑und‑Licht‑System induziert. Nur Tumorzellen, die das Lichtsignal erhalten, beginnen diesen Trainingsmarker zu zeigen. Treffen synNotch‑T‑Zellen ein, fungieren diese markierten Zellen als „Trainingszentren“: Sie aktivieren viele T‑Zellen und rüsten diese mit PEbody‑CARs aus. Einmal trainiert, können diese T‑Zellen dann die gesamte Tumormasse angreifen, indem sie PE‑markierte Antikörper gegen verbreitete Tumormarker wie PD‑L1 oder PSMA nutzen — auch gegen Zellen, die nie den Trainingsmarker exprimiert hatten.
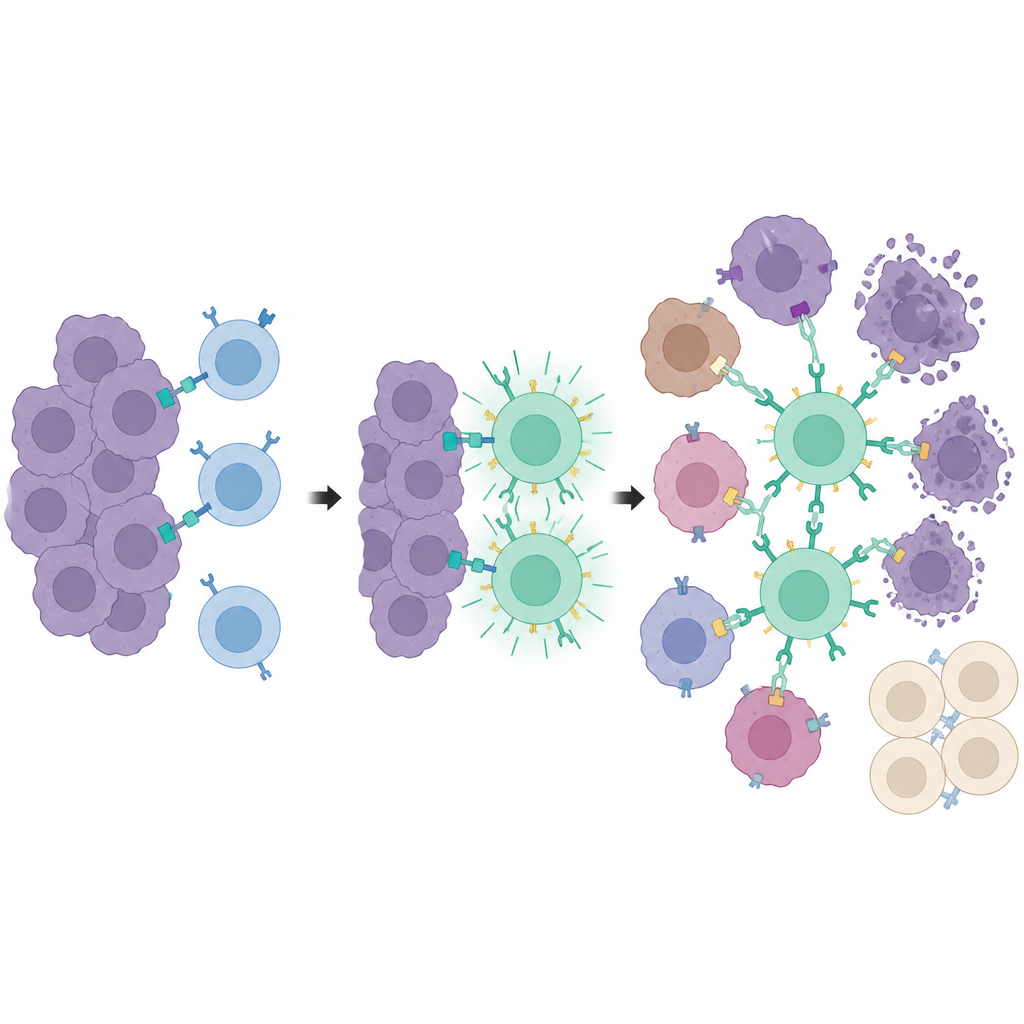
Lokaler Angriff, ferne Gewebe geschont
In mehreren Mausmodellen von Brust‑ und Prostatakrebs führte das kombinierte Medikament‑, Licht‑ und synNotch‑System zu starker Tumorkontrolle an beleuchteten Stellen. Tumoren, die Tamoxifen und Licht erhielten, gefolgt von programmierbaren T‑Zellen und PE‑markierten Antikörpern, schrumpften oder wuchsen deutlich langsamer als unbeleuchtete Tumoren desselben Tieres. Wichtig ist, dass die T‑Zellen zwar im ganzen Körper zirkulierten, aber nur innerhalb der lichtvorbereiteten Tumoren voll aktiviert wurden, wodurch Schäden an anderen Organen mit denselben Oberflächenmarkern begrenzt blieben. Im Vergleich zu einer konventionellen CAR‑T‑Behandlung gegen den PSMA‑Marker erzielte die neue Strategie eine ähnliche Tumorkontrolle bei geringerem Gewichtsverlust, niedrigeren Entzündungswerten und reduzierten Anzeichen von Leberschäden.
Was das für die Zukunft der Krebsbehandlung bedeuten könnte
Für Laien ist die Kernidee, dass die Forschenden eine Art universelles, umschreibbares CAR‑T‑System mit einem eingebauten lokalen Sicherheitsverschluss geschaffen haben. Die Wahl der markierten Antikörper bestimmt, welche Tumoreigenschaften angegriffen werden, sodass Ärzte die Behandlung anpassen könnten, wenn ein Krebs sich entwickelt, ohne die T‑Zellen neu herstellen zu müssen. Gleichzeitig sorgt das Medikament‑und‑Licht‑Design zusammen mit den Trainingszentren dafür, dass die volle Angriffskraft der T‑Zellen nur im Tumor freigesetzt wird, nicht in gesundem Gewebe mit denselben Markern. Zwar bleibt noch viel Arbeit, bevor dieser Ansatz bei Patienten angewendet werden kann, doch die Studie skizziert einen flexiblen Bauplan für sicherere, anpassbarere Zelltherapien gegen komplexe solide Tumoren.
Zitation: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
Schlüsselwörter: CAR-T-Zellen, solide Tumoren, Optogenetik, Antigenentweichung, synthetische Immuntherapie