Clear Sky Science · ja
薬可制御の光活性化によりプログラム可能なCARと抗原の組み合わせを設計する
免疫細胞により賢く狩らせることを教える
多くの人がCAR T細胞を聞いたことがあるでしょう。これは患者自身の免疫細胞を再プログラムして腫瘍を攻撃させる個別化がん治療の一種です。これらの療法は一部の血液癌には有効ですが、乳房、前立腺、肺などの固形腫瘍には苦戦してきました。本研究は、CAR T細胞の標的認識能力を高めつつ抑制する新しい方法を示し、多様な腫瘍細胞をより確実に見つけつつ健常組織を守る手法を提示します。
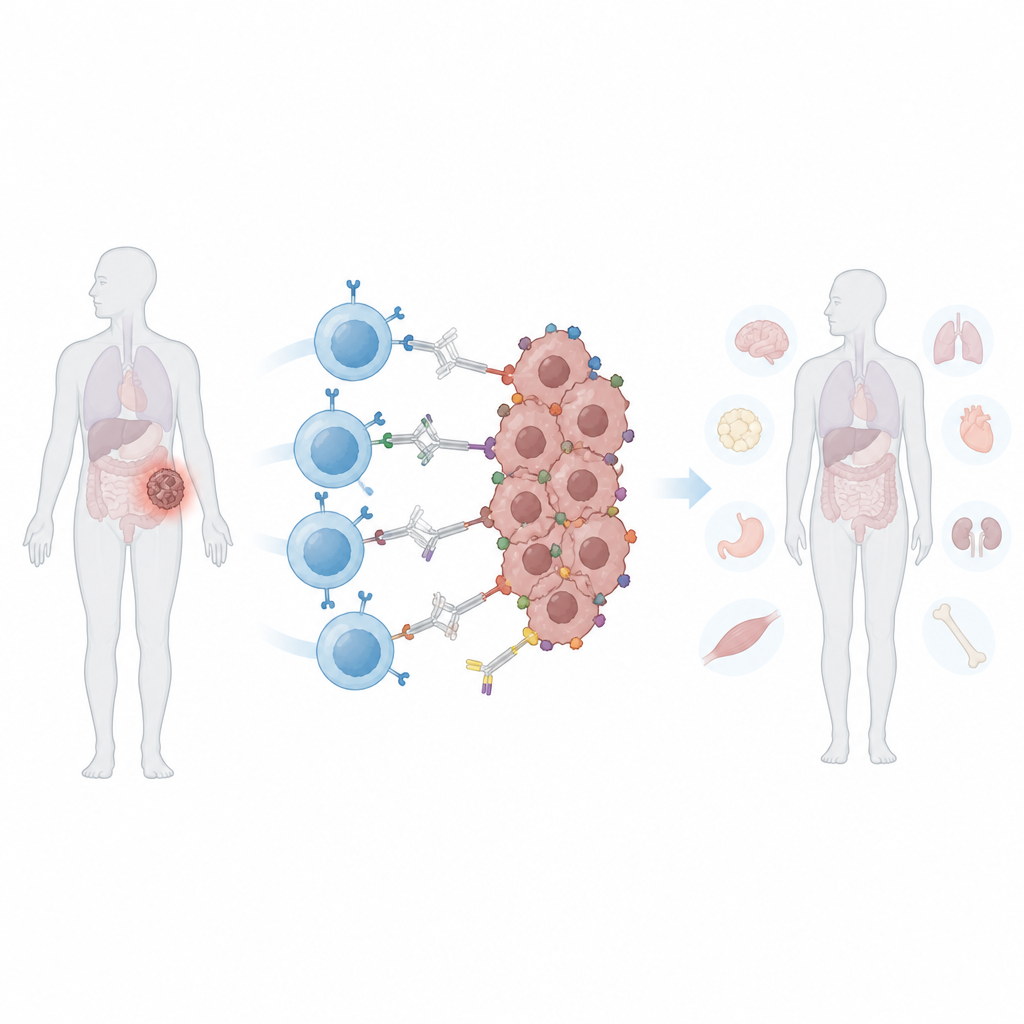
形を変える腫瘍の難しさ
従来のCAR T細胞は癌細胞上の特定の分子的「旗」を認識するように作られています。固形腫瘍はこの攻撃を二つの方法でかわすことが多いです。第一に、その旗を失ったり減少させたりすることで生き残る「抗原回避」が起き、腫瘍の一部の細胞が残って再増殖します。第二に、同じ腫瘍内でも細胞ごとに異なる旗を示すことがあり、これを異質性と呼びます。CAR T細胞により多くの旗を認識させれば助けになりますが、それは同じマーカーを共有する正常組織を攻撃するリスクも高めます。従来型のCAR T細胞は注入後常に活性化状態にあるため、副作用が出たときに医師が容易に活動を上下できないという問題があります。
多くの腫瘍を標的にする汎用プラグ
研究者らは腫瘍細胞に直接結合しない「プログラム可能な」CARを作製しました。代わりに、食品や検査で一般的に使われる明るい色のタンパク質フィコエリスリン(phycoerythrin)を認識します。彼らはPEbodyと呼ばれる小さなヒト由来の結合ドメインをCARに組み込み、このタンパク質タグを持つ任意の抗体に付着できるようにしました。どのPEタグ付き抗体を投与するかを選ぶことで、同じCAR T細胞群を異なるがんマーカーに順次、または同時に向け直すことが理論上可能になります。培養系では、これらのPEbody CAR T細胞は対応するタグ付き抗体を与えると白血病や複数の固形腫瘍細胞株を効率的に殺し、最初の標的が失われたときには新しい標的に再指向され得ました。
光と薬による安全スイッチ
安全性を高めるために、チームはCAR発現を必要な場所・必要な時にだけオンにする多層の制御システムを加えました。彼らはまず一般的な薬剤タモキシフェンに応答し、次いで青色光に応答する二段構えの遺伝子スイッチを用いました。両方の手がかりを受けたT細胞だけがリコンビナーゼ酵素を活性化し、CAR遺伝子を永久にオンに切り替えます。この「薬可制御の光活性化」は強力なCAR活性を照射された腫瘍領域に限定します。細胞培養では、タモキシフェンと光の両方にさらされたT細胞でCAR量と腫瘍殺傷が急増し、暗所や薬剤なしの細胞は静かなままでした。マウスでは、同じシステムが光を受けた体側の腫瘍でのみ強い遺伝子活性化を駆動し、影になった側ではほとんど活動が観察されませんでした。
腫瘍内の訓練センター
さらに一歩進めて、研究者らは腫瘍の検知と腫瘍の殺傷を分離しました。彼らはsynNotchと呼ばれる第二の改変受容体を用い、T細胞が特別なマーカー(切断版CD19)に遭遇した後でのみPEbody CARをオンにします。そのマーカー自体は自然には存在せず、同じ薬と光のシステムで局所的に誘導されます。光信号を受けた腫瘍細胞だけがこの訓練マーカーを表示し、synNotch T細胞が到着するとそれらの標識細胞は「訓練センター」として機能して多数のT細胞を活性化し、PEbody CARを装備させます。一度訓練されたT細胞は、その後PD-L1やPSMAなど一般的な腫瘍マーカーに対するPEタグ付き抗体を用いて、訓練マーカーを決して発現しなかった細胞を含む腫瘍全体を攻撃できます。
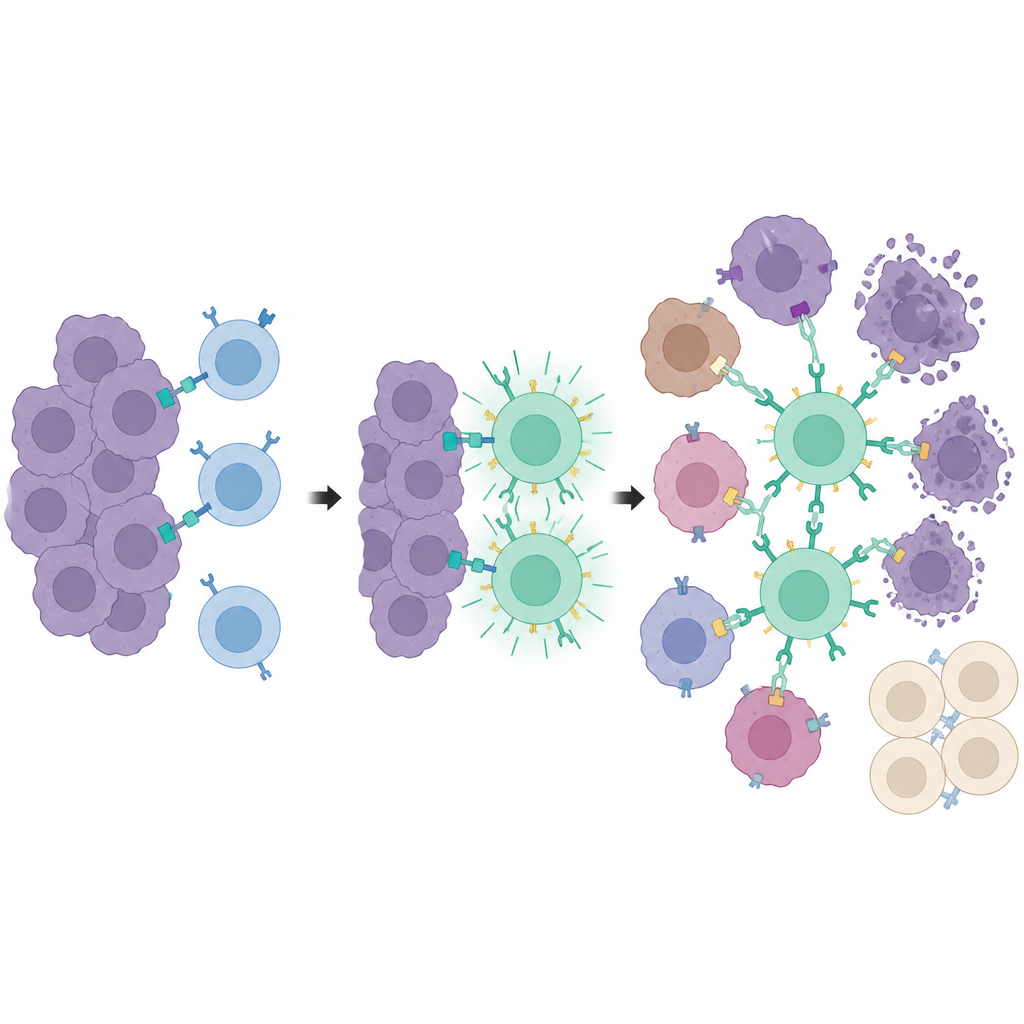
局所攻撃で遠隔組織は保護
乳がんおよび前立腺がんのいくつかのマウスモデルで、薬、光、synNotchを組み合わせたシステムは照射部位で強い腫瘍制御をもたらしました。タモキシフェンと光を受け、その後プログラム可能なT細胞とPEタグ付き抗体が与えられた腫瘍は、同一動物の照射されていない腫瘍より縮小するか増殖が大幅に遅れました。重要なのは、T細胞は体内を巡回したものの完全に活性化されたのは光でプライミングされた腫瘍内だけであり、同じ表面マーカーを持つ他の臓器への損傷を限定したことです。PSMAマーカーを標的とする従来型CAR T療法と比べて、新しい戦略は同等の腫瘍制御を達成しつつ体重減少や炎症シグナルの低下、肝障害の兆候の軽減を示しました。
将来のがん治療に意味すること
一般読者向けに要点を述べると、研究者らは一種の汎用で書き換え可能なCAR Tシステムに局所的な安全ロックを組み込んだということです。どのタグ付き抗体を選ぶかで標的とする腫瘍の特徴を決められるため、医師はがんの進化に合わせてT細胞を最初から作り直すことなく治療を適応させられる可能性があります。同時に、薬と光、そして訓練センターの設計は、T細胞の攻撃力が完全に発揮されるのを腫瘍内部だけに限定し、同じマーカーを共有する健常組織での誤攻撃を防ぐ助けになります。このアプローチが患者に到達するまでにはなお多くの作業が残っていますが、本研究は複雑な固形腫瘍に対するより安全で適応性のある細胞療法の柔軟な設計図を示しています。
引用: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
キーワード: CAR T細胞, 固形腫瘍, オプトジェネティクス, 抗原回避, 合成免疫療法