Clear Sky Science · es
Ingeniería de CAR programables y emparejamiento de antígenos mediante activación con fármacos y luz
Enseñar a las células inmunitarias a cazar con más inteligencia
Mucha gente ha oído hablar de las células CAR T, un tipo de tratamiento oncológico personalizado que reprograma las propias células inmunitarias del paciente para atacar los tumores. Estas terapias funcionan bien en algunos cánceres hematológicos, pero han tenido dificultades contra tumores sólidos, como los de mama, próstata o pulmón. Este estudio describe una nueva forma de afinar y restringir las células CAR T para que puedan encontrar mejor las células tumorales diversas al tiempo que preservan los tejidos sanos.
El desafío de los tumores que cambian de forma
Las células CAR T estándar están diseñadas para reconocer una “bandera” molecular específica en las células cancerosas. Los tumores sólidos a menudo eluden este ataque de dos maneras. Primero, pueden perder o reducir esa bandera, un proceso llamado escape antigénico, lo que permite que algunas células sobrevivan y el tumor vuelva a crecer. Segundo, diferentes células dentro del mismo tumor pueden exhibir banderas distintas, un problema conocido como heterogeneidad. Ampliar el reconocimiento de las CAR T para ver más banderas puede ayudar, pero también aumenta el riesgo de que ataquen tejidos normales que comparten esos marcadores. Una vez infundidas, las CAR T convencionales están siempre activas, lo que dificulta a los médicos modular su actividad si aparecen efectos secundarios.
Un enchufe universal para apuntar a muchos tipos de tumor
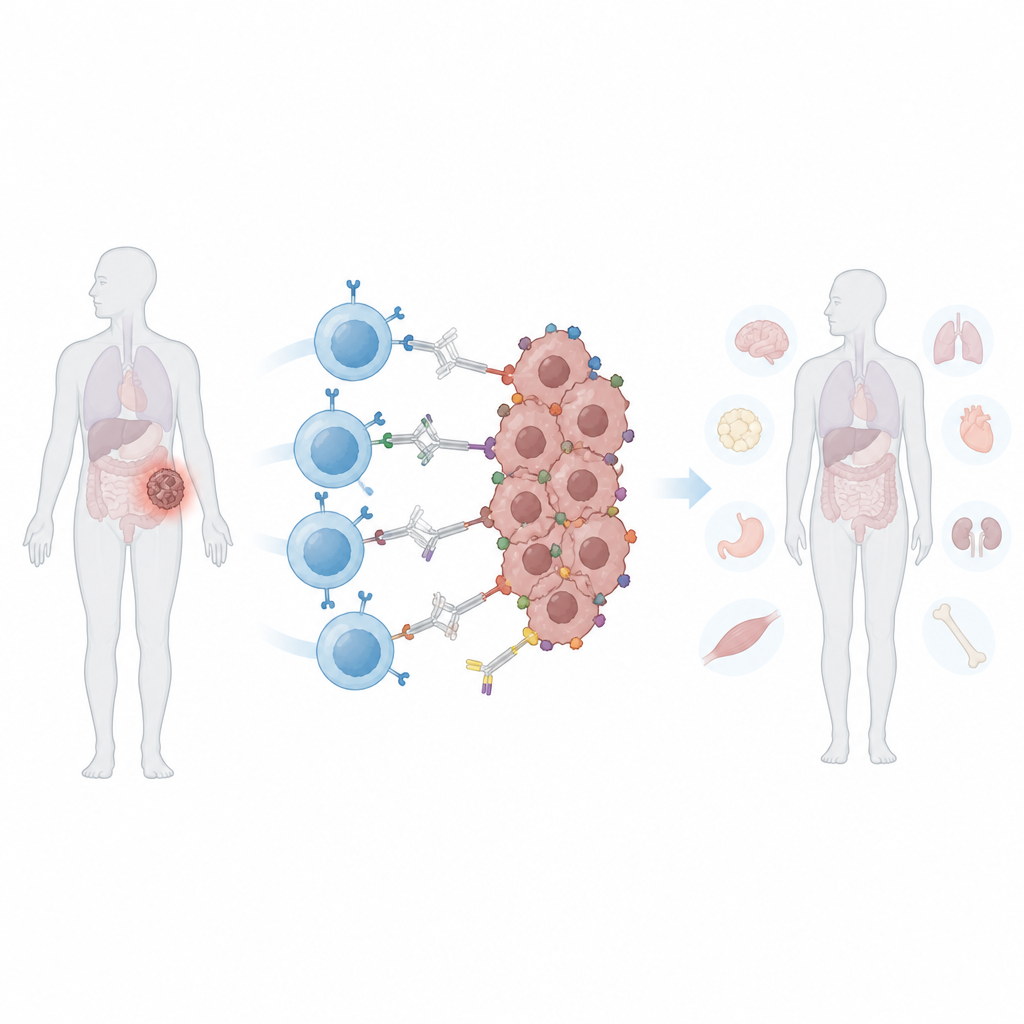
Los investigadores crearon una CAR “programable” que no se une directamente a las células tumorales. En su lugar, reconoce una proteína segura y de color brillante llamada ficoeritrina, empleada habitualmente en alimentos y pruebas de laboratorio. Ingenieríaaron un pequeño dominio de unión derivado de humano, llamado PEbody, en la CAR para que se acople a cualquier anticuerpo que lleve esta etiqueta proteica. Al elegir qué anticuerpo con etiqueta PE infundir, los médicos podrían, en principio, redirigir el mismo lote de células CAR T a diferentes marcadores tumorales, uno tras otro o varios a la vez. En pruebas de laboratorio, estas CAR T con PEbody mataron de forma eficiente líneas celulares de leucemia y de múltiples tumores sólidos cuando se les proporcionaron los anticuerpos etiquetados correspondientes, y pudieron reorientarse a nuevos marcadores cuando el primero se perdió.
Un interruptor de seguridad con luz y fármaco
Para mejorar la seguridad, el equipo añadió un sistema de control por capas que permite activar la expresión de la CAR solo donde y cuando sea necesario. Usaron un interruptor genético en dos pasos que responde primero a un fármaco común, el tamoxifeno, y luego a luz azul. Solo las células T que reciban ambas señales activan una recombinasa que enciende de forma permanente el gen de la CAR. Esta “activación con luz condicionada por fármaco” confina la potente actividad de las CAR a las regiones tumorales iluminadas. En cultivo celular, los niveles de CAR y la capacidad de matar tumores aumentaron bruscamente en las células T expuestas tanto a tamoxifeno como a luz, mientras que las células en oscuridad o sin fármaco permanecieron silenciosas. En ratones, el mismo sistema provocó una fuerte activación génica solo en los tumores del lado del cuerpo que recibió luz, con actividad insignificante en el lado sombreado.
Centros de entrenamiento dentro del tumor
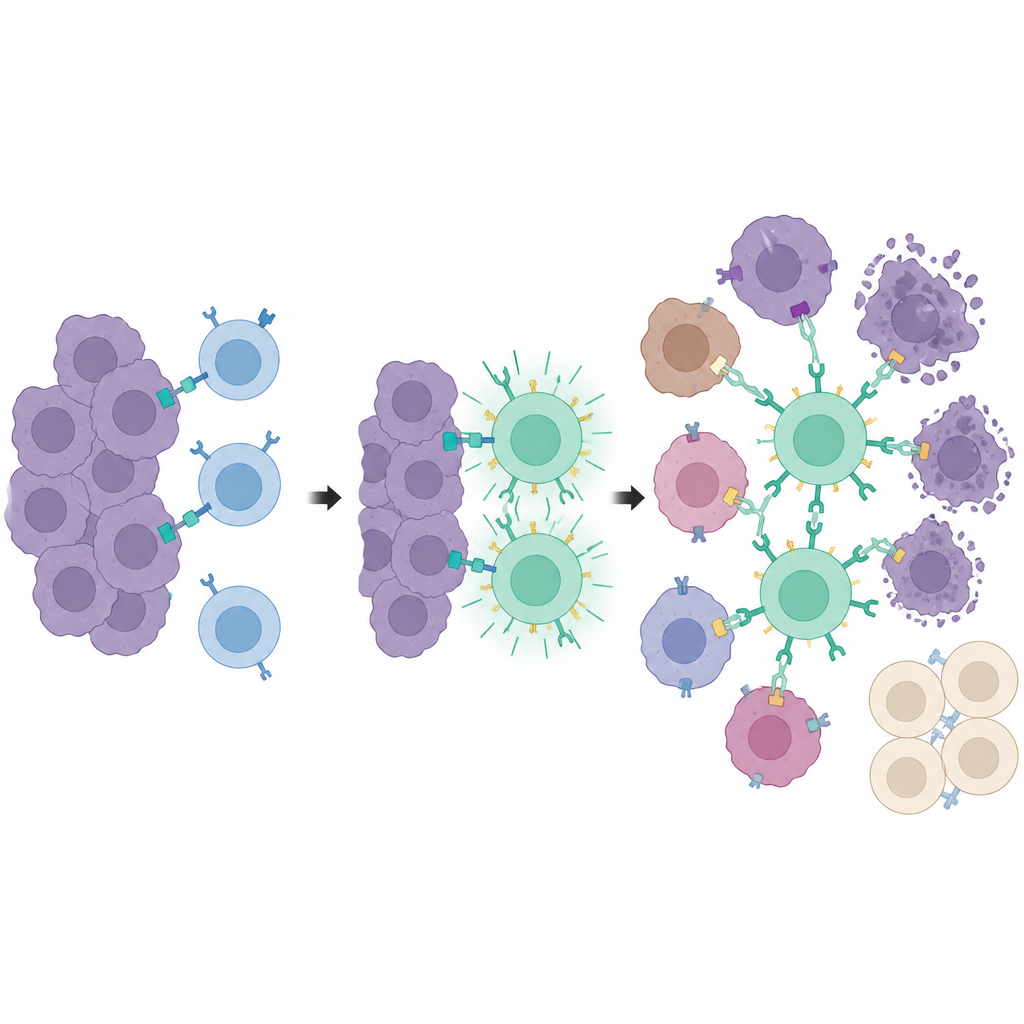
Dando un paso más, los investigadores separaron la detección del tumor de la capacidad de matarlo. Emplearon un segundo receptor diseñado, llamado synNotch, que activa la CAR PEbody solo después de que una célula T encuentre un marcador especial, una versión truncada de CD19, colocada en las células tumorales. Ese marcador en sí no está presente de forma natural, sino que se induce localmente mediante el mismo sistema de fármaco y luz. Solo las células tumorales que reciben la señal luminosa comienzan a exhibir este marcador de entrenamiento. Cuando llegan las células T con synNotch, esas células marcadas actúan como “centros de entrenamiento”, activando muchas células T y dotándolas de CAR PEbody. Una vez entrenadas, estas células T pueden entonces atacar la masa tumoral más amplia usando anticuerpos etiquetados con PE contra marcadores tumorales comunes como PD-L1 o PSMA, incluso en células que nunca expresaron el marcador de entrenamiento.
Ataque localizado con tejidos distantes protegidos
En varios modelos murinos de cáncer de mama y de próstata, el sistema combinado de fármaco, luz y synNotch condujo a un fuerte control tumoral en los sitios iluminados. Los tumores que recibieron tamoxifeno y luz, seguidos por células T programables y anticuerpos con etiqueta PE, se redujeron o crecieron mucho más despacio que los tumores no iluminados en el mismo animal. De forma importante, las células T circularon por todo el cuerpo pero solo se activaron por completo dentro de los tumores cebados con luz, limitando el daño a otros órganos que portaban los mismos marcadores de superficie. En comparación con un tratamiento convencional de CAR T dirigido al marcador PSMA, la nueva estrategia logró un control tumoral similar con menos pérdida de peso, señales inflamatorias más bajas y menores señales de daño hepático.
Lo que esto podría significar para la atención del cáncer en el futuro
Para un lector general, la idea clave es que los investigadores han construido una especie de sistema CAR T universal y reescribible con un seguro local incorporado. La elección de anticuerpos etiquetados decide qué características tumorales atacar, de modo que los médicos podrían adaptar el tratamiento a medida que el cáncer evoluciona sin tener que reconstruir las células T desde cero. Al mismo tiempo, el diseño basado en fármaco-luz y centros de entrenamiento ayuda a garantizar que la máxima potencia de ataque de las células T se libere solo dentro del tumor, no en tejidos sanos que compartan los mismos marcadores. Aunque queda mucho trabajo antes de que este enfoque llegue a los pacientes, el estudio plantea un plano flexible para terapias celulares más seguras y adaptables contra tumores sólidos complejos.
Cita: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
Palabras clave: células CAR T, tumores sólidos, optogenética, escape antigénico, inmunoterapia sintética