Clear Sky Science · ru
Инженерия программируемых CAR и парность антигенов с помощью лекарственно-регулируемой световой активации
Обучение иммунных клеток охотиться умнее
Многие слышали о CAR T-клетках — форме персонализированного лечения рака, при которой собственные иммунные клетки пациента перепрограммируют для атаки опухолей. Эти терапии хорошо работают при некоторых кровных онкологиях, но сталкиваются с трудностями против солидных опухолей, например в молочной железе, предстательной железе или лёгких. В этом исследовании описан новый подход, который одновременно повышает точность и ограничивает активность CAR T-клеток, чтобы они лучше обнаруживали разнообразные опухолевые клетки, при этом щадя здоровые ткани.
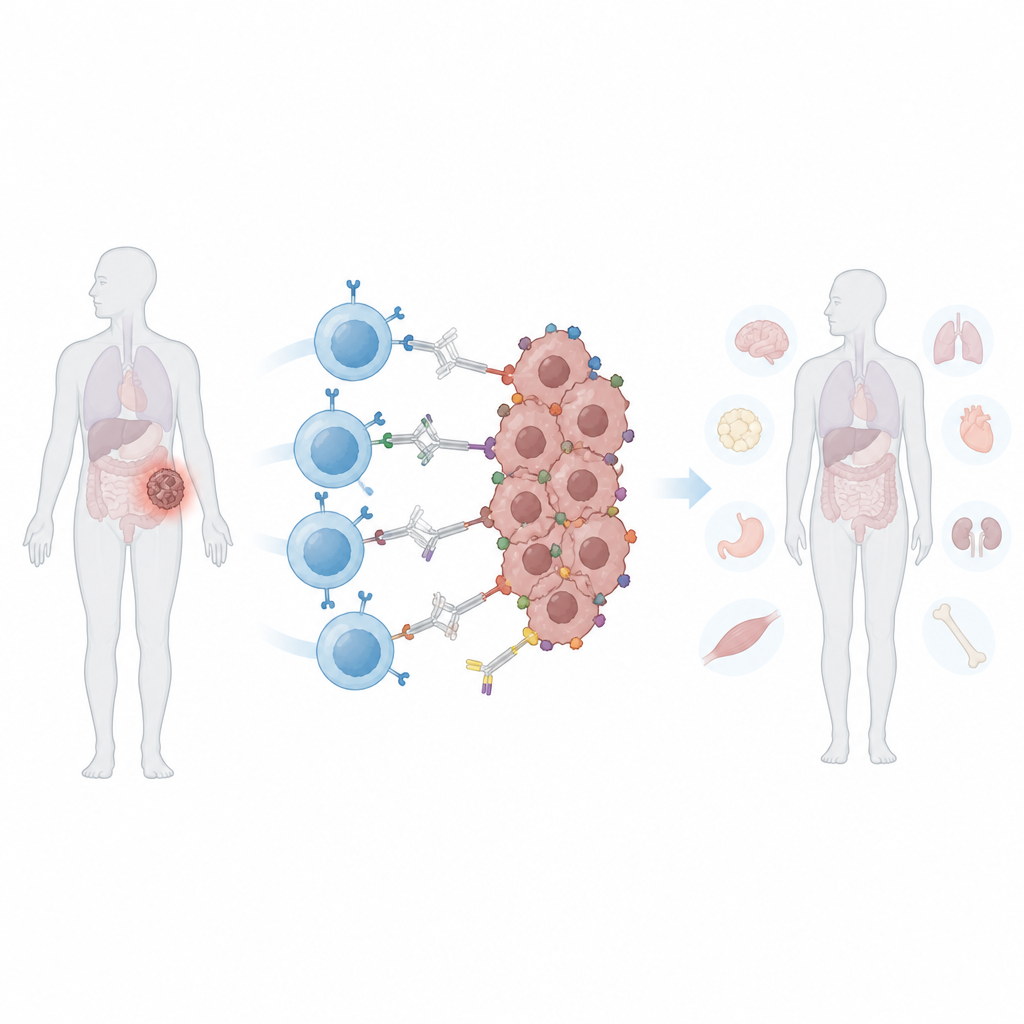
Проблема меняющихся форм опухолей
Стандартные CAR T-клетки созданы для распознавания одного конкретного молекулярного «флага» на раковых клетках. Солидные опухоли часто ускользают от такой атаки двумя способами. Во-первых, они могут терять или снижать экспрессию этого флага — процесс, называемый побегом от антигена, — что позволяет отдельным клеткам выживать и заново разрастать опухоль. Во-вторых, разные клетки внутри одной и той же опухоли могут нести разные флаги, что называется гетерогенностью. Расширение распознавания CAR T-клетками большего числа маркеров может помочь, но одновременно увеличивает риск атаки нормальных тканей, несущих те же маркеры. После инфузии обычные CAR T-клетки постоянно активны, и врачу трудно регулировать их активность при появлении побочных эффектов.
Универсальная «вилка» для нацеливания на разные опухоли
Исследователи создали «программируемый» CAR, который не связывается с опухолевыми клетками напрямую. Вместо этого он распознаёт безопасный, ярко окрашенный белок — фикоэритрин, часто используемый в пищевой промышленности и лабораторных тестах. Они встроили небольшой гуманный связующий домен, называемый PEbody, в CAR, чтобы он прикреплялся к любому антителу, несущему этот белковый тег. Выбирая, какие PE-меченые антитела вводить, врачи теоретически могут перенаправлять одну и ту же партию CAR T-клеток на разные опухолевые маркеры — по очереди или одновременно на несколько. В лабораторных экспериментах эти PEbody CAR T-клетки эффективно убивали клетки лейкемии и нескольких линий солидных опухолей при наличии соответствующих меченых антител и могли перенаправляться на новые мишени, когда первоначальный маркер исчезал.
Световой и лекарственный переключатель безопасности
Чтобы повысить безопасность, команда добавила многоуровневую систему контроля, позволяющую включать экспрессию CAR только там и тогда, где это необходимо. Они использовали двухкомпонентный генетический выключатель, который сначала реагирует на распространённый препарат тамоксифен, а затем на синий свет. Только те Т-клетки, которые получают оба сигнала, активируют рекомбиназу, которая постоянно включает ген CAR. Эта «лекарственно-ограниченная световая активация» ограничивает мощную активность CAR регионами опухоли, куда подан свет. В культурах клеток уровни CAR и способность убивать опухоль резко возрастали в Т-клетках, получивших и тамоксифен, и свет, тогда как клетки в темноте или без препарата оставались неактивными. У мышей та же система вызывала сильную активацию гена только в опухолях на той стороне тела, которая получала свет, при ничтожной активности на затенённой стороне.
Учебные центры внутри опухоли
Двигаясь дальше, исследователи разделили обнаружение опухоли и её уничтожение. Они использовали второй инженерный рецептор, называемый synNotch, который включает PEbody CAR только после того, как Т-клетка встречает специальный маркер — укороченную версию CD19, размещённую на опухолевых клетках. Сам по себе этот маркер естественно не присутствует, но индуцируется локально той же системой «лекарство + свет». Только опухолевые клетки, получившие световой сигнал, начинают демонстрировать этот маркер подготовки. Когда synNotch-Т-клетки прибывают, помеченные клетки действуют как «учебные центры», активируя множество Т-клеток и оснащая их PEbody CAR. После обучения эти Т-клетки могут затем атаковать более широкую массу опухоли, используя PE-меченые антитела против общих опухолевых маркеров, таких как PD-L1 или PSMA, даже на тех клетках, которые никогда не экспрессировали маркер подготовки.
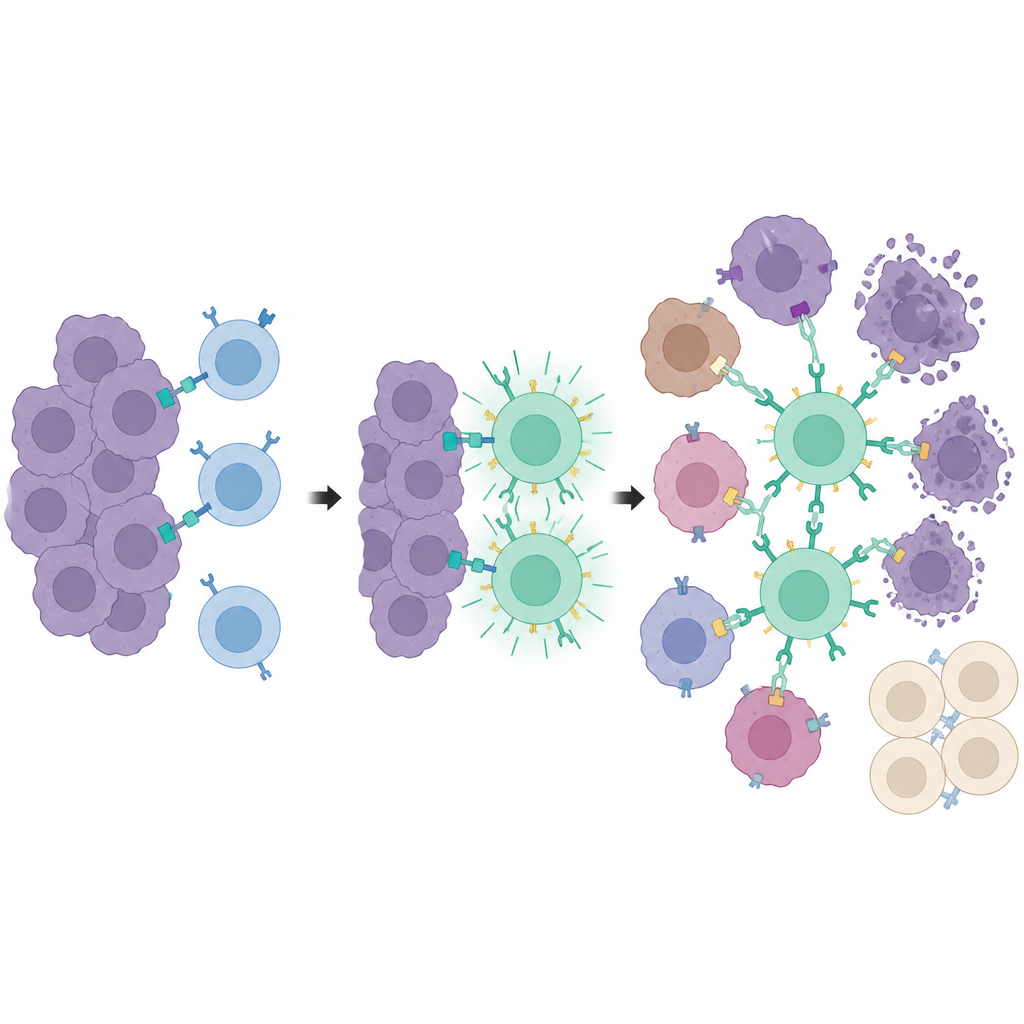
Локальная атака при сохранении здоровья отдалённых тканей
В нескольких моделях мышей с раком молочной и предстательной железы комбинированная система препарата, света и synNotch приводила к сильному контролю опухоли в освещённых участках. Опухоли, получавшие тамоксифен и свет с последующей подачей программируемых Т-клеток и PE-меченых антител, уменьшались или росли значительно медленнее, чем неосвещённые опухоли у того же животного. Важно, что Т-клетки циркулировали по всему организму, но были полностью активированы только внутри светоподготовленных опухолей, что ограничивало повреждение других органов с теми же поверхностными маркерами. По сравнению с традиционной терапией CAR T, направленной на маркер PSMA, новая стратегия обеспечивала сопоставимый контроль опухоли с меньшей потерей массы тела, более низкими воспалительными реакциями и уменьшенными признаками повреждения печени.
Что это может значить для будущей помощи при раке
Для неспециалиста ключевая идея такова: исследователи создали своего рода универсальную, переписываемую систему CAR T с встроенным локальным замком безопасности. Выбор меченых антител определяет, какие особенности опухоли будут нацелены, поэтому врачи могли бы адаптировать лечение по мере эволюции рака, не перестраивая Т-клетки с нуля. Одновременно дизайн «лекарство + свет» и концепция учебных центров помогают обеспечить, чтобы полная сила атаки Т-клеток разворачивалась только внутри опухоли, а не в здоровых тканях с теми же маркерами. Хотя до применения у пациентов ещё далеко, исследование описывает гибкую схему для более безопасных и адаптируемых клеточных терапий против сложных солидных опухолей.
Цитирование: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
Ключевые слова: CAR T клетки, солидные опухоли, оптогенетика, побег от антигена, синтетическая иммунотерапия