Clear Sky Science · ar
تصميم CAR قابل للبرمجة وتزاوج المستضدات عبر تنشيط دوائي محكوم بالضوء
تعليم الخلايا المناعية كيف تصطاد بذكاء أكبر
سمع الكثيرون عن خلايا CAR T، وهو نوع من علاجات السرطان المخصّصة التي تعيد برمجة خلايا الجهاز المناعي لدى المريض ليهاجم الأورام. تنجح هذه العلاجات جيدًا مع بعض سرطانات الدم لكنها واجهت صعوبات ضد الأورام الصلبة مثل سرطانات الثدي والبروستاتا والرئة. تصف هذه الدراسة طريقة جديدة لكل من تعزيز وتقيد خلايا CAR T بحيث تستطيع العثور على خلايا ورمية متنوّعة مع الحفاظ على الأنسجة السليمة.
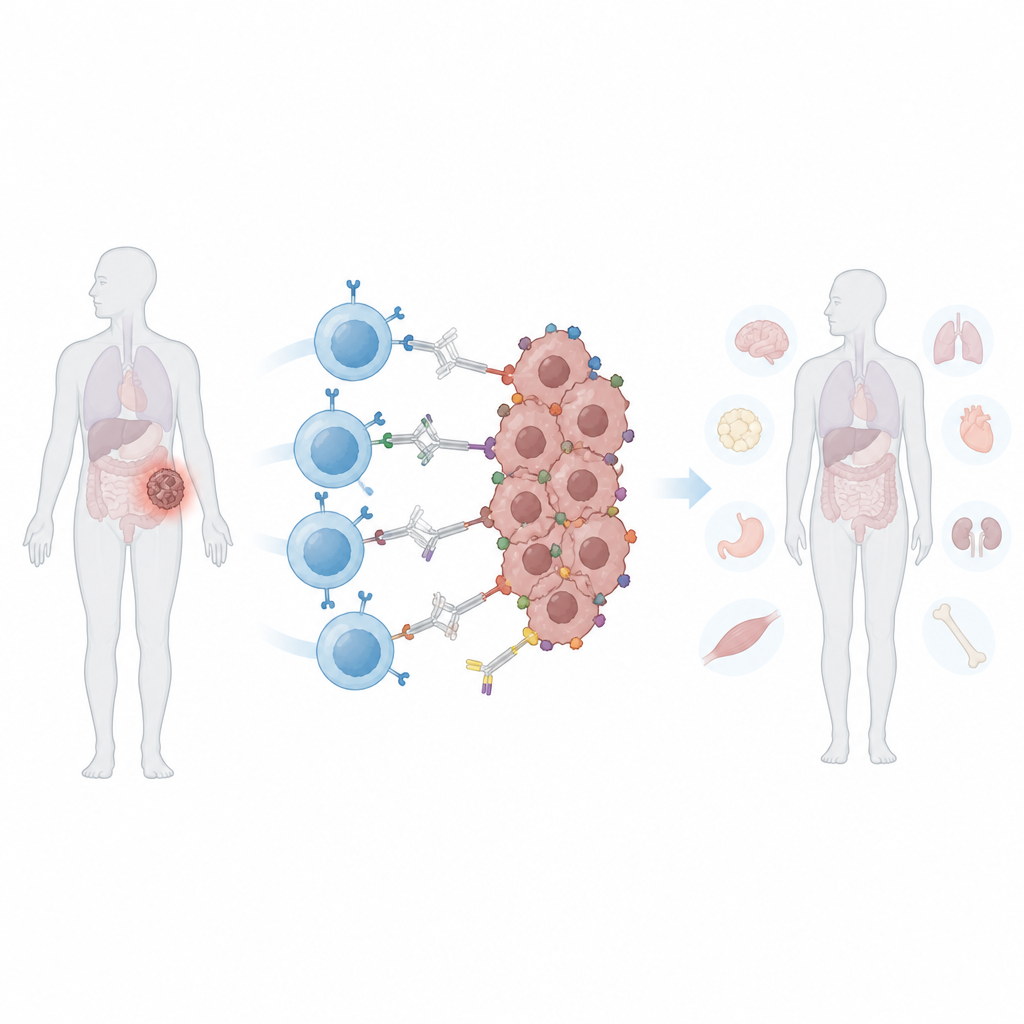
تحدي الأورام متغيرة الشكل
تُبنى خلايا CAR T التقليدية لتتعرف على "علم" جزيئي واحد محدد على الخلايا السرطانية. غالبًا ما تفلت الأورام الصلبة من هذا الهجوم بطريقتين. أولًا، يمكنها فقدان أو خفض ذلك العلم، وهي عملية تُسمى هروب المستضد، مما يسمح لبعض الخلايا بالبقاء وإعادة نمو الورم. ثانيًا، قد تعرض خلايا مختلفة داخل نفس الورم أعلامًا مختلفة، وهي مشكلة تُعرف بعدم التجانس. توسيع نطاق قدرة خلايا CAR T لتتعرف على أعلام أكثر يمكن أن يساعد، لكن ذلك يزيد أيضًا من خطر مهاجمتها للأنسجة الطبيعية التي تشترك في تلك العلامات. وبمجرد حقن خلايا CAR T التقليدية، تظل نشطة دائمًا، مما يصعّب على الأطباء تعديل نشاطها إن ظهرت آثار جانبية.
قابس عالمي لاستهداف أنواع أورام متعددة
أنشأ الباحثون CAR "قابل للبرمجة" لا يرتبط بالخلايا الورمية مباشرة. بدلاً من ذلك، يتعرف على بروتين آمن وملوَّن بشكل ساطع يُدعى فيكوإريثرين (phycoerythrin)، يُستخدم عادة في الأطعمة والاختبارات المخبرية. حرّكوا نطاق ارتباط صغير مشتق من الإنسان، أطلقوا عليه اسم PEbody، على CAR ليلتصق بأي جسم مضاد يحمل وسم هذا البروتين. باختيار أي جسم مضاد معنّن بوسم PE لحقنه، يمكن للأطباء من حيث المبدأ إعادة توجيه نفس دفعة خلايا CAR T إلى علامات سرطانية مختلفة، واحدة تلو الأخرى أو عدة علامات في آن واحد. في تجارب مخبرية، قتلت خلايا PEbody CAR T بشكل فعّال خلايا خطوط سرطان الدم وبعض خطوط الأورام الصلبة عندما وُفّر لها الأجسام المضادة الموسومة المطابقة، وكان بالإمكان إعادة توجيهها إلى علامات جديدة عندما اختفى العلم الأول.
مفتاح أمان بالدواء والضوء
لتحسين الأمان، أضاف الفريق نظام تحكّم متعدد الطبقات يسمح بتشغيل تعبير CAR فقط حيث ومتى يلزم. استخدموا مفتاحًا وراثيًا مكوّنًا من جزأين يستجيب أولاً لدواء شائع، تاموكسيفين، ثم للضوء الأزرق. فقط خلايا T التي تتلقى الإشارتين تُفعّل إنزيمًا معدّلًا (recombinase) يقلب جين CAR بشكل دائم لتشغيله. يقيّد هذا "التشغيل الضوئي المحكوم بالدواء" نشاط CAR القوي لمناطق الأورام المضاءة. في مزروعات خلوية، ارتفعت مستويات CAR وقتل الخلايا الورمية بشدة في الخلايا T المعرضة لكل من التاموكسيفين والضوء، بينما بقيت الخلايا في الظلام أو دون الدواء هادئة. في الفئران، نفس النظام دفع تفعيلًا جينيًا قويًا فقط في الأورام على جهة الجسم التي تَلَقّت الضوء، مع نشاط ضئيل على الجانب المظلل.
مراكز تدريب داخل الورم
تقدمًا أكثر، فصل الباحثون استشعار الورم عن قتل الورم. استخدموا مستقبلًا مهندسًا ثانيًا يُدعى synNotch يُشغّل CAR PEbody فقط بعد أن تصادف خلية T علامة خاصة، نسخة مجزأة من CD19، موضوعة على الخلايا الورمية. هذه العلامة نفسها ليست موجودة طبيعيًا بل تُستحث محليًا بواسطة نفس نظام الدواء والضوء. فقط الخلايا الورمية التي تستلم إشارة الضوء تبدأ في عرض علامة التدريب هذه. عندما تصل خلايا synNotch T، تعمل تلك الخلايا الموسومة كم "مراكز تدريب"، فتُفعّل العديد من خلايا T وتزوّدها بـ CARs PEbody. وبعد التدريب، يمكن لتلك الخلايا T أن تُهاجم الكتلة الورمية الأوسع باستخدام أجسام مضادة معنونة بوسم PE ضد علامات ورمية شائعة مثل PD-L1 أو PSMA، حتى على خلايا لم تُظهر علامة التدريب أبدًا.
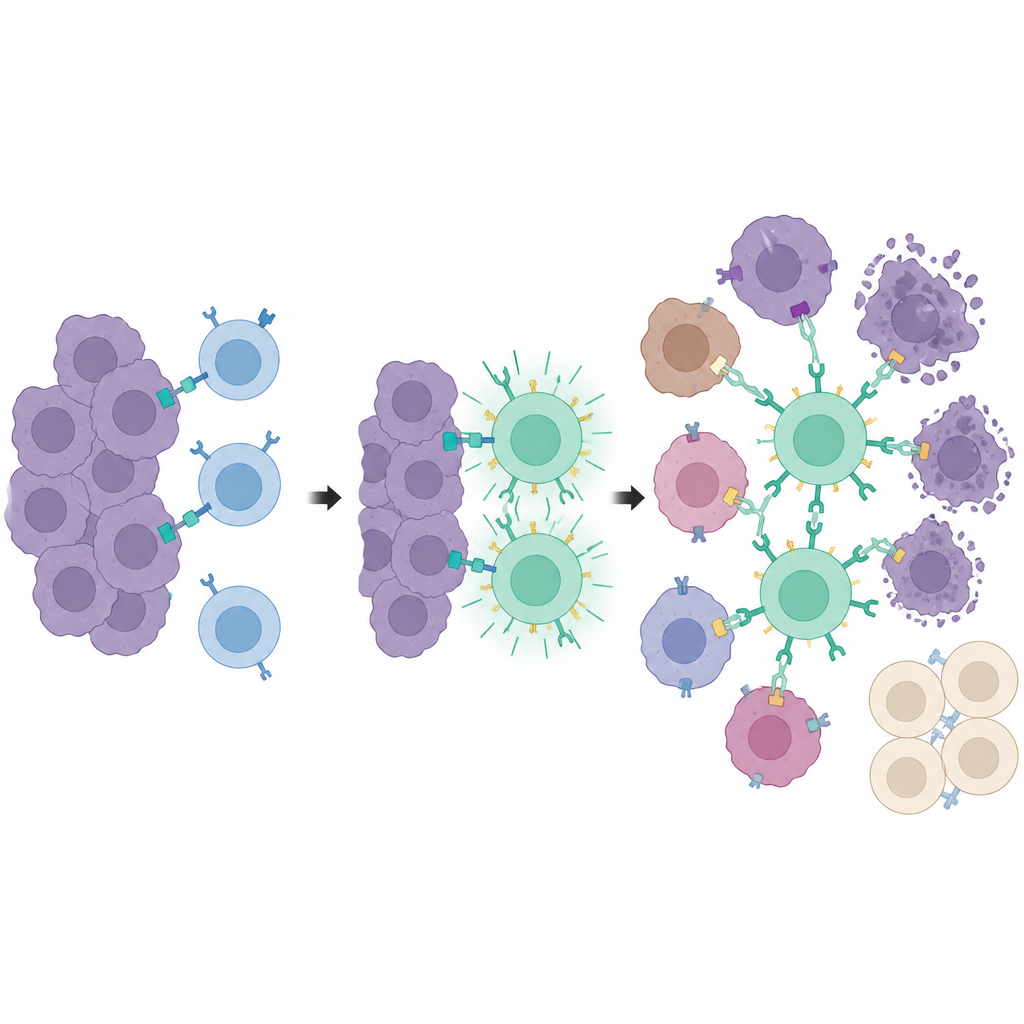
هجوم موضعي مع حفاظ على الأنسجة البعيدة
في عدة نماذج فأرية لسرطان الثدي والبروستاتا، أدى الجمع بين الدواء والضوء ونظام synNotch إلى سيطرة قوية على الأورام في المواقع المضاءة. تقلصت الأورام التي تلقت تاموكسيفين والضوء، تلتها خلايا T القابلة للبرمجة والأجسام المضادة الموسومة بـ PE، أو نمت ببطء أكبر بكثير من الأورام غير المضاءة في نفس الحيوان. والأهم أن خلايا T دارت في الجسم كله لكنها كانت مفعّلة بالكامل فقط داخل الأورام المهيأة بالضوء، مما حدّ من الضرر على أعضاء أخرى تحمل نفس العلامات السطحية. مقارنة بعلاج CAR T تقليدي موجه إلى علامة PSMA، حققت الاستراتيجية الجديدة سيطرة مماثلة على الورم مع فقدان وزن أقل وإشارات التهابية أدنى وعلامات متقلصة لتلف الكبد.
ماذا قد يعني هذا لرعاية السرطان في المستقبل
للقارئ العام، الفكرة الأساسية هي أن الباحثين بنوا نوعًا من نظام CAR T عام وقابل لإعادة الكتابة مع قفل أمان موضعي مدمج. قرار اختيار الأجسام المضادة الموسومة يحدد أي ميزات ورمية يجب استهدافها، بحيث يمكن للأطباء تكييف العلاج مع تطور السرطان دون إعادة بناء الخلايا من الصفر. وفي الوقت نفسه، يساعد تصميم الدواء والضوء ومراكز التدريب على ضمان أن قوة الهجوم الكاملة لخلايا T تُطلَق فقط داخل الورم، لا في الأنسجة السليمة التي تشترك في نفس العلامات. وبينما لا يزال هناك عمل كبير قبل أن يصل هذا النهج إلى المرضى، توضح الدراسة مخططًا مرنًا لعلاجات خلوية أكثر أمانًا وقابلة للتكيف ضد الأورام الصلبة المعقدة.
الاستشهاد: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
الكلمات المفتاحية: خلايا CAR T, أورام صلبة, البصريات الوراثية (optogenetics), هروب المستضد, العلاج المناعي الاصطناعي