Clear Sky Science · pt
Engenharia de emparelhamento programável entre CAR e antígeno via ativação por luz controlada por fármaco
Ensinando células imunes a caçar com mais inteligência
Muitas pessoas já ouviram falar de células CAR T, um tipo de tratamento personalizado contra o câncer que reprograma as próprias células imunes do paciente para atacar tumores. Essas terapias funcionam bem para alguns cânceres sanguíneos, mas têm dificuldades contra tumores sólidos, como os de mama, próstata ou pulmão. Este estudo descreve uma nova forma de ao mesmo tempo aguçar e conter as células CAR T para que possam localizar melhor células tumorais diversas, poupando os tecidos saudáveis.
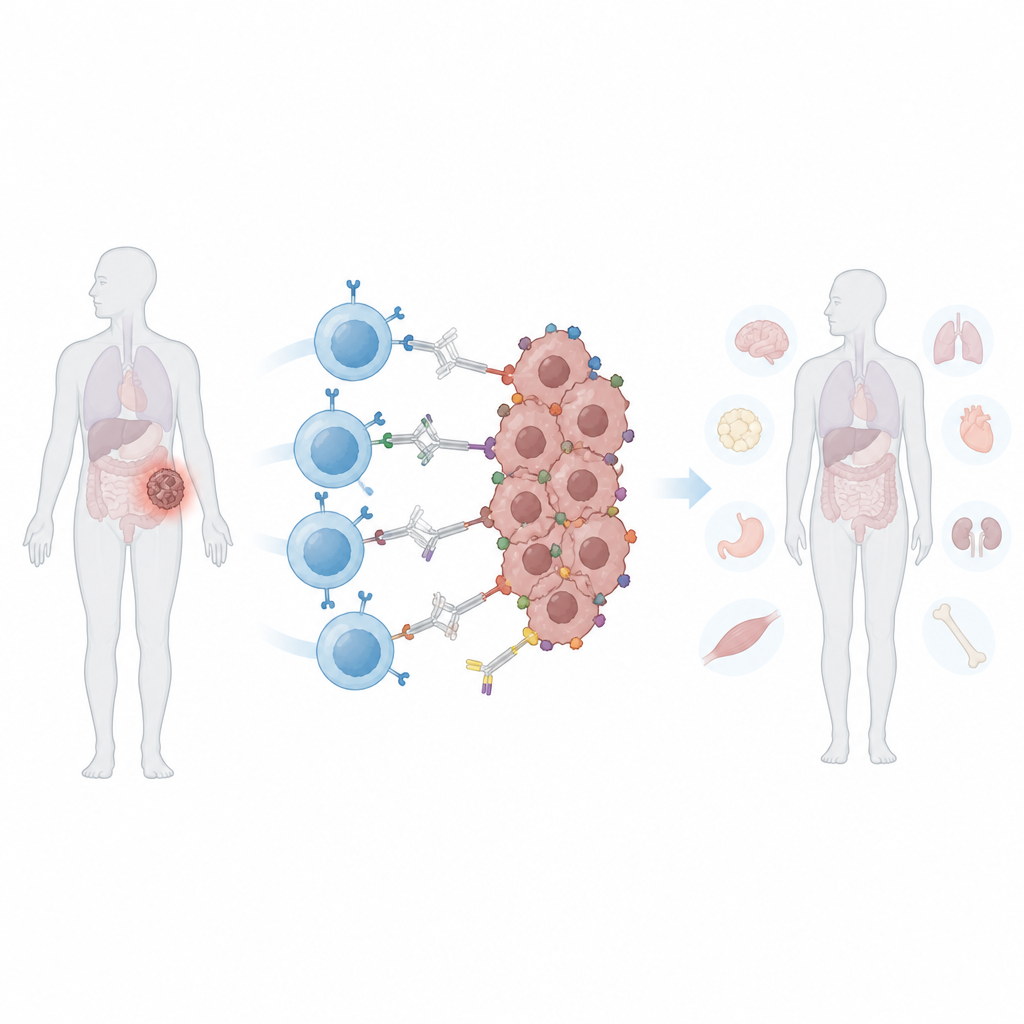
O desafio dos tumores que mudam de forma
As células CAR T convencionais são projetadas para reconhecer uma “bandeira” molecular específica nas células cancerosas. Tumores sólidos frequentemente evitam esse ataque de duas formas. Primeiro, podem perder ou diminuir essa bandeira, um processo chamado escape de antígeno, permitindo que algumas células sobrevivam e o tumor volte a crescer. Segundo, diferentes células dentro do mesmo tumor podem exibir bandeiras diferentes, um problema conhecido como heterogeneidade. Expandir as células CAR T para reconhecer mais bandeiras pode ajudar, mas também aumenta o risco de que ataquem tecidos normais que compartilham esses marcadores. Uma vez infundidas, as CAR T convencionais estão sempre ativas, o que torna difícil para os médicos ajustar sua atividade caso surjam efeitos colaterais.
Um conector universal para mirar em muitos tipos de tumor
Os pesquisadores criaram um CAR “programável” que não se liga diretamente às células tumorais. Em vez disso, ele reconhece uma proteína segura e de cor brilhante chamada ficoeritrina (phycoerythrin), comumente usada em alimentos e testes laboratoriais. Eles engenheiraram um pequeno domínio de ligação de origem humana, chamado PEbody, no CAR para que ele se prenda a qualquer anticorpo que carregue essa etiqueta proteica. Ao escolher qual anticorpo marcado com PE infundir, os médicos poderiam, em princípio, redirecionar o mesmo lote de células CAR T para diferentes marcadores tumorais, um após outro ou vários de uma vez. Em testes de laboratório, essas células PEbody CAR T mataram de forma eficiente linhagens de leucemia e de múltiplos tumores sólidos quando recebiam anticorpos marcados correspondentes, e podiam ser retargetadas para novos marcadores quando o primeiro era perdido.
Um interruptor de segurança por luz e fármaco
Para aumentar a segurança, a equipe adicionou um sistema de controle em camadas que permite ligar a expressão do CAR apenas onde e quando necessário. Eles usaram um interruptor genético em duas partes que responde primeiro a um fármaco comum, o tamoxifeno, e depois à luz azul. Apenas as células T que recebem ambos os sinais ativam uma enzima recombinase que liga permanentemente o gene do CAR. Essa “ativação por luz com trava farmacológica” confina a atividade potente do CAR às regiões tumorais iluminadas. Em cultura celular, os níveis de CAR e a morte tumoral aumentaram fortemente em células T expostas tanto ao tamoxifeno quanto à luz, enquanto células mantidas no escuro ou sem o fármaco permaneceram silenciosas. Em camundongos, o mesmo sistema promoveu forte ativação gênica apenas nos tumores do lado do corpo que recebeu luz, com atividade negligenciável no lado sombreado.
Centros de treinamento dentro do tumor
Indo além, os pesquisadores separaram a detecção do tumor da fase de ataque ao tumor. Eles usaram um segundo receptor engenheirado, chamado synNotch, que liga o CAR PEbody apenas depois que uma célula T encontra um marcador especial — uma versão truncada de CD19 — colocada nas células tumorais. Esse marcador em si não está naturalmente presente, mas é induzido localmente pelo mesmo sistema de fármaco e luz. Apenas as células tumorais que recebem o sinal luminoso começam a exibir esse marcador de treinamento. Quando as células T synNotch chegam, essas células marcadas atuam como “centros de treinamento”, ativando muitas células T e equipando-as com CARs PEbody. Uma vez treinadas, essas células T podem então atacar a massa tumoral mais ampla usando anticorpos marcados com PE contra marcadores tumorais comuns como PD-L1 ou PSMA, mesmo em células que jamais expressaram o marcador de treinamento.
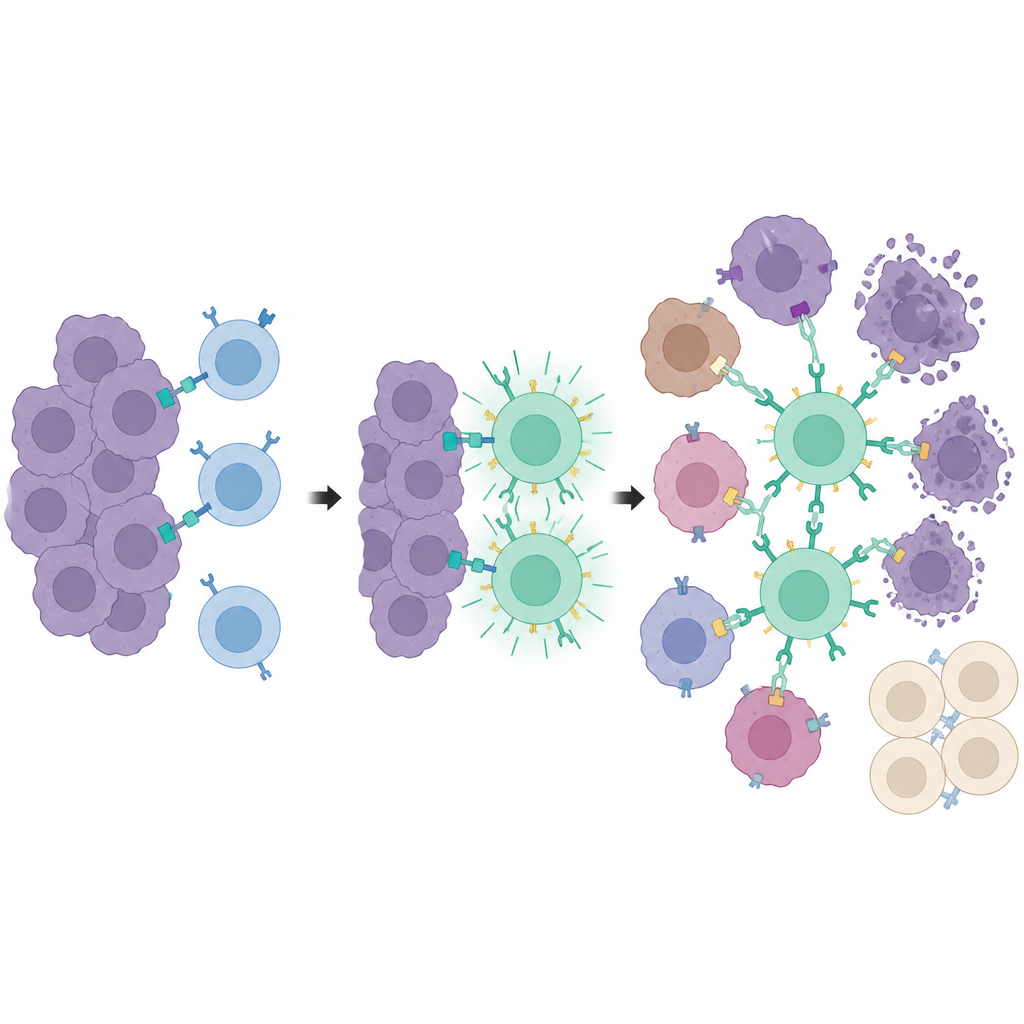
Ataque local com preservação de tecidos distantes
Em vários modelos murinos de câncer de mama e próstata, o sistema combinado de fármaco, luz e synNotch levou a um forte controle tumoral nos locais iluminados. Tumores que receberam tamoxifeno e luz, seguidos pelas células T programáveis e por anticorpos marcados com PE, encolheram ou cresceram muito mais lentamente do que tumores não iluminados no mesmo animal. Importante, as células T circularam por todo o corpo, mas foram totalmente ativadas apenas dentro dos tumores primados pela luz, limitando o dano a outros órgãos que carregavam os mesmos marcadores de superfície. Em comparação com um tratamento CAR T convencional dirigido ao marcador PSMA, a nova estratégia alcançou controle tumoral similar com menos perda de peso, sinais inflamatórios menores e redução de indícios de dano hepático.
O que isso pode significar para cuidados futuros contra o câncer
Para um leitor leigo, a ideia principal é que os pesquisadores construíram uma espécie de sistema CAR T universal e reescritível com uma trava de segurança local embutida. A escolha dos anticorpos marcados decide quais características do tumor serão alvo, de modo que os médicos possam adaptar o tratamento conforme o câncer evolui sem reconstruir as células T do zero. Ao mesmo tempo, o desenho com fármaco-e-luz e os centros de treinamento ajudam a garantir que o poder total de ataque das células T seja desencadeado apenas dentro do tumor, não em tecidos saudáveis que compartilham os mesmos marcadores. Embora muito trabalho ainda seja necessário antes que essa abordagem chegue a pacientes, o estudo delineia um roteiro flexível para terapias celulares mais seguras e adaptáveis contra tumores sólidos complexos.
Citação: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
Palavras-chave: Células CAR T, tumores sólidos, optogenética, escape de antígeno, imunoterapia sintética