Clear Sky Science · zh
膜界面电势决定神经元中α-突触核蛋白的表面凝聚与纤维化
这对大脑健康意味着什么
帕金森病及相关疾病的特征是在脑细胞内出现一种称为α-突触核蛋白的蛋白质团块,但这些团块如何最初出现并在细胞间传播一直是未解之谜。本研究表明,神经元的外层膜可以在极低蛋白水平下悄然将α-突触核蛋白聚集成微小液滴,这些液滴会硬化为损伤性的纤维,进而扭曲甚至破裂膜。理解这种位于细胞表面的隐性前期场所,为思考有害蛋白团块如何起始、成长与在大脑中迁移提供了新的视角。
神经元“皮肤”如何聚拢游离蛋白
作者着眼于包裹细胞的那层薄脂质膜,它由多种脂类混合构成。他们发现,通常在神经元内自由漂浮的α-突触核蛋白可以被吸引到膜上并在膜面形成致密液滴,即便其总体浓度极低。值得注意的是,这种现象仅在膜含有两种常见脂质以6:4比例混合——一种中性脂质与一种带负电的脂质——时出现。正是这一特定配比在膜表面创造了恰当的电气条件来吸引并固定α-突触核蛋白。当这些条件不满足,或相同脂质以游离颗粒而非连续表面存在时,蛋白并不会凝聚成液滴。
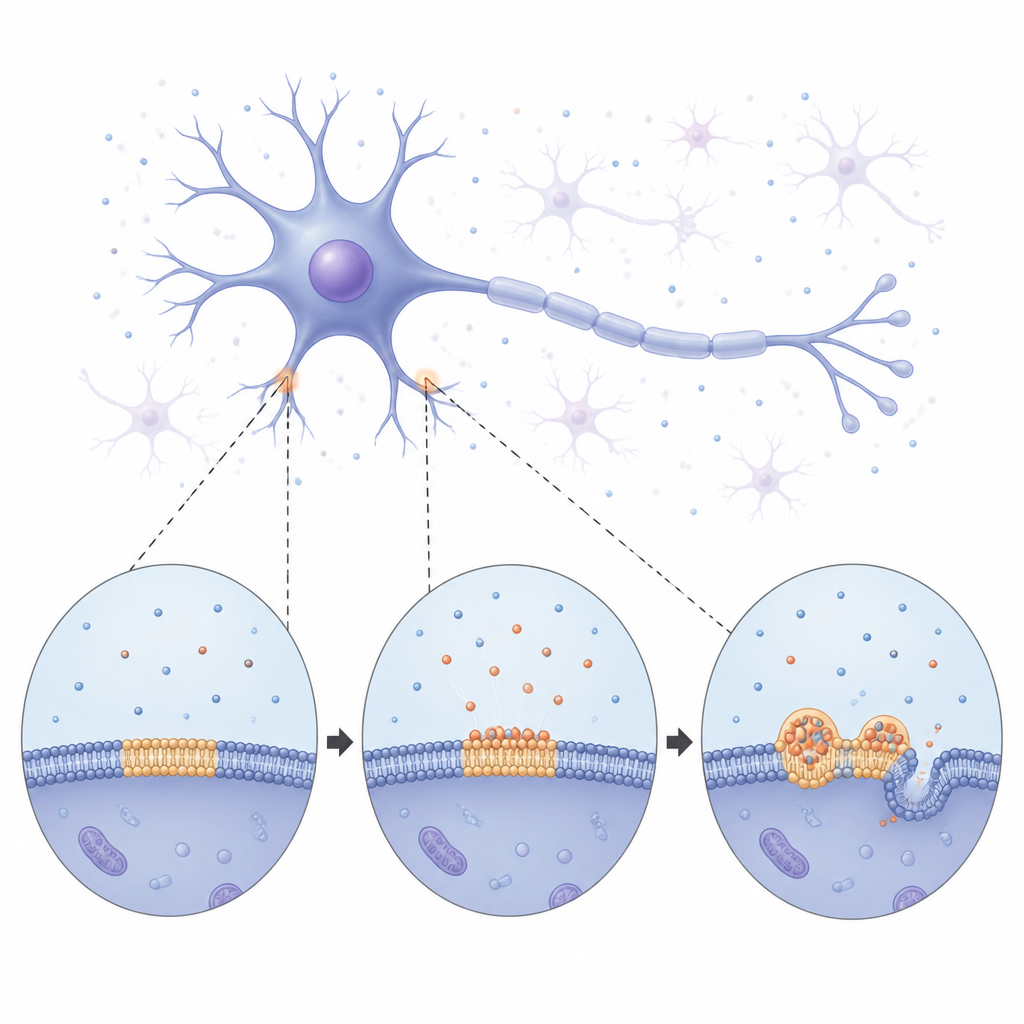
从柔软液滴到刚性纤维
通过长期成像,研究团队观察到α-突触核蛋白逐渐包覆膜面,随后分裂成分布在表面的明亮球状凝聚体。起初这些液滴呈现微小液体斑块行为:它们彼此融合,并通过缓慢从更小的邻近液滴抽取物质而生长。然而随时间推移,液滴变得越来越刚性。通过测量荧光信号在液滴内部的恢复速度,发现蛋白和周围脂质的移动都逐渐减慢,提示从流动态向更固态的转变。最终,细长的类似纤维的结构从液滴中萌发,弯曲并管状化下方膜。这些观察表明,膜结合的液滴充当了暂时的、液体状的集结区,使α-突触核蛋白在固化为与疾病相关的纤维之前得以重组。
膜本身如何被改变
研究还探讨了在这一过程中α-突触核蛋白对膜的影响。对模型膜的实验显示,当蛋白插入到膜表面时,会使脂层更紧密排列且更难被压缩,改变膜的张力和曲率。被微吸管吸入的巨型合成囊泡在加入α-突触核蛋白后放松并滑出,表明膜张力迅速下降并伴随形状改变。数小时内,蛋白与膜的结合变得更牢固。这些力学变化在界面处创造了更硬、更有序的环境,反过来又有利于更多蛋白的聚集和稳定接触,促进液滴的进一步生长及最终的纤维形成。
电性表面电荷的隐性作用
为了解为何仅有特定脂质混合触发凝聚,研究者测量了膜表面的电势。他们发现α-突触核蛋白结合仅在一狭窄的负电表面电荷窗口内发生,而强烈的凝聚在该范围的某一阈值附近出现。计算机模拟支持了这一点,表明一种有吸引力的膜可以引发“预润湿样”转变:即使溶液体相过于稀薄而无法自行相分离,表面上仍会形成一层富含蛋白的厚层。在活细胞中,团队以两种方式改变了这种界面电势:向培养的海马细胞中加入额外带负电的脂质改变了电势并缩小了既存的α-突触核蛋白斑点,而用高钾或谷氨酸去极化原代神经元则增加了α-突触核蛋白液滴的数量并促使其释放。这将神经元的日常电活动直接关联到蛋白质凝聚的地点与方式。
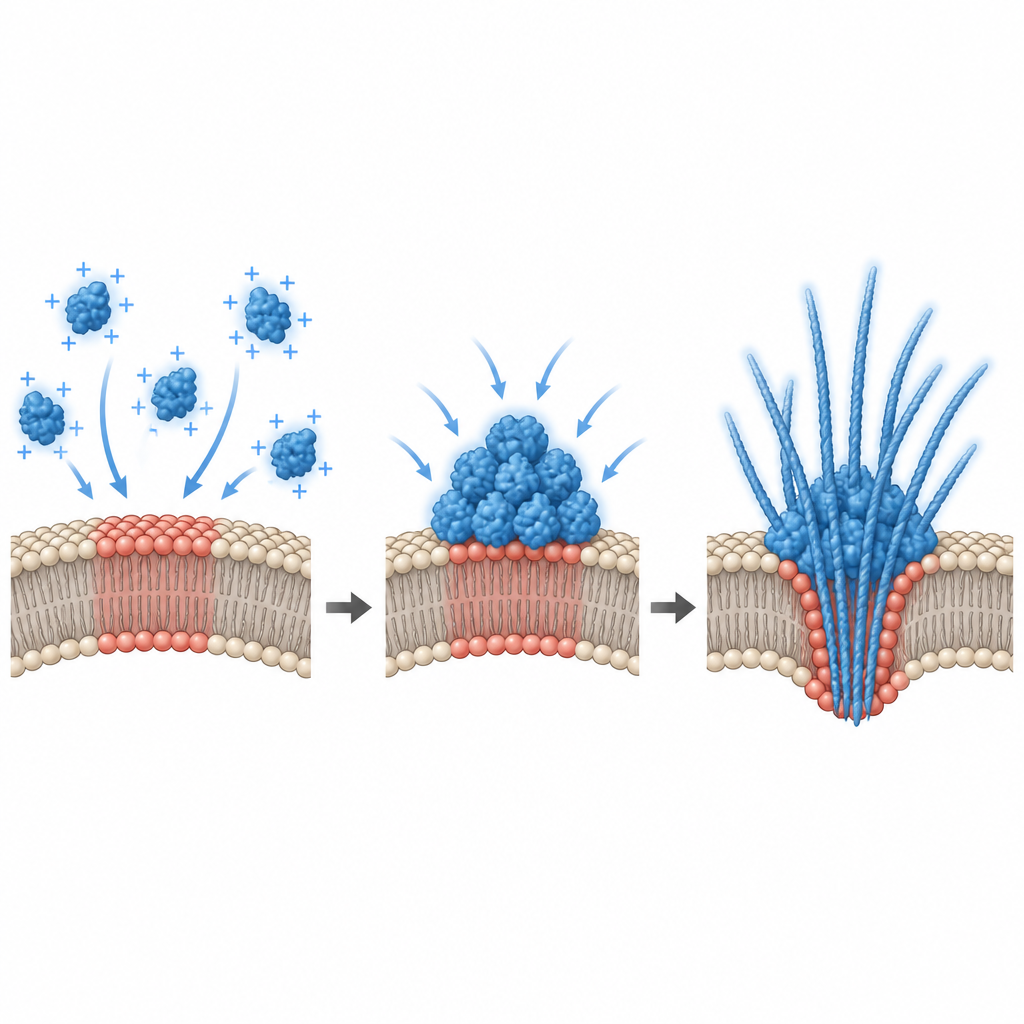
这对神经退行性疾病意味着什么
综合来看,这些发现描绘出一种图景:神经元上特定的膜斑作为α-突触核蛋白液滴在接近健康脑中蛋白水平时的无声组装线。脂质成分或电学状态的细微变化即可将这些表面推入一个发生凝聚、液滴变硬并出现纤维的状态,纤维会使膜变形并有时破裂,同时将蛋白聚合体释放到细胞外。由膜驱动的这一途径为α-突触核蛋白在神经退行性过程中从神经元传播提供了合理的路线,并提示调整膜组成或表面电势可能在早期阶段帮助控制有害蛋白凝聚。
引用: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
关键词: α-突触核蛋白, 帕金森病, 神经元膜, 蛋白质凝聚, 脂质组成