Clear Sky Science · ja
膜の界面電位がニューロンにおけるα-シヌクレインの表面凝縮と線維化を支配する
脳の健康にとっての重要性
パーキンソン病や関連疾患では、α-シヌクレインというタンパク質の凝集体が神経細胞内に見られますが、これらの凝集体がどのようにして最初に出現し細胞間で広がるのかは不明でした。本研究は、神経細胞の外側の皮膜である細胞膜が、ごく低濃度のタンパク質であってもα-シヌクレインを静かに小さな液滴として集め得ること、そしてこれらの液滴が硬化して膜を変形させ果ては破裂させるような有害な繊維に転移しうることを示します。細胞表面というこの見えにくい舞台を理解することは、有害なタンパク質凝集がどのように始まり、成長し、脳内を移動するかについて新たな視点を提供します。
神経細胞の“皮”がゆるいタンパク質を集める仕組み
著者らは細胞を取り囲む薄い脂質二重層、すなわちさまざまな脂質の混合物からなる膜に注目しました。通常は細胞内に自由に存在するα-シヌクレインが、この膜に引き寄せられて濃い液滴を形成し得ることを見出したのです。驚くべきことに、これは膜が2種類の一般的な脂質、中性のものと負に帯電したものを6:4の比率で含む場合にのみ起きました。その特定の組成が膜表面にちょうど適切な電気的条件を作り、α-シヌクレインを引き寄せ保持するのです。この条件が満たされない場合、あるいは同じ脂質が連続した表面ではなく遊離粒子として存在する場合には、タンパク質は液滴として凝縮しませんでした。
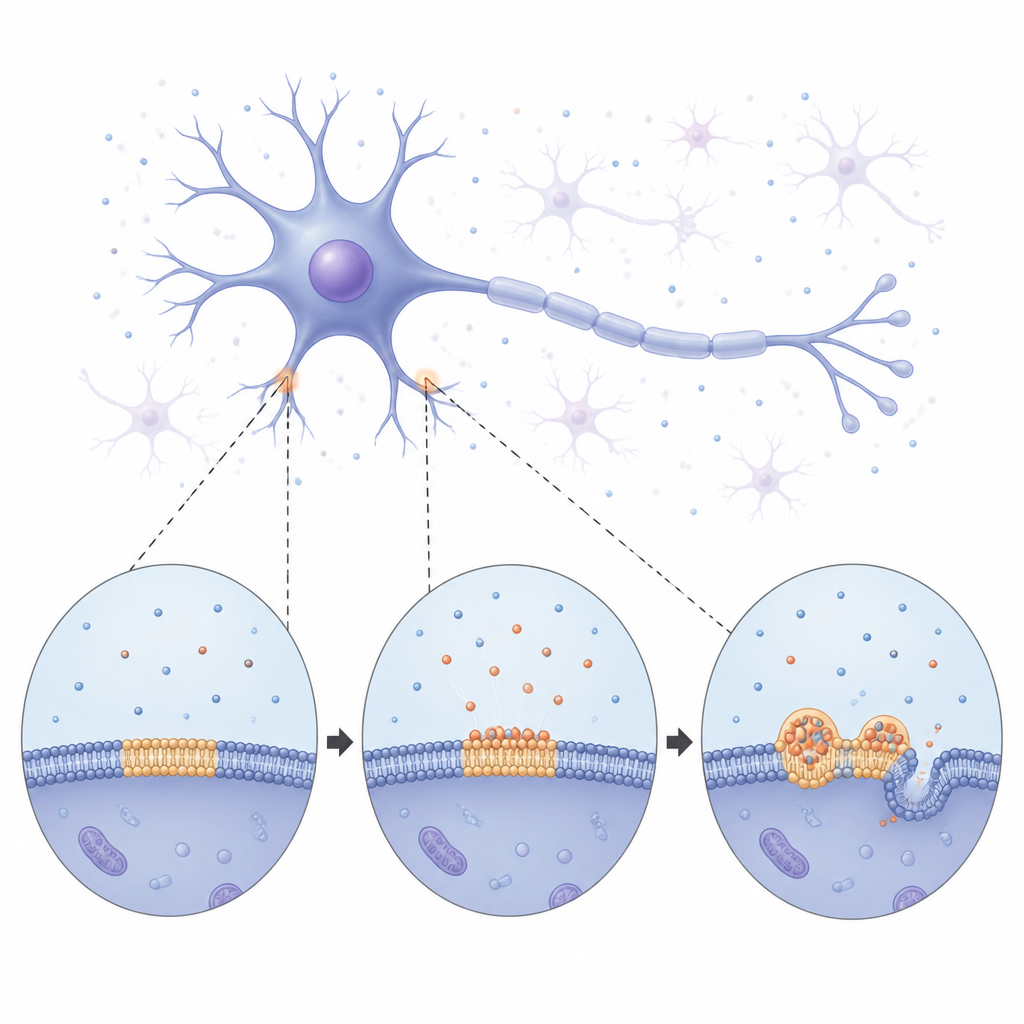
柔らかな液滴から硬い線維へ
長時間イメージングにより、研究チームはα-シヌクレインがゆっくりと膜を覆い、その後表面に明るく丸い凝縮体が散在する様子を観察しました。初めのうちはこれらの液滴は微小な液体の塊のように振る舞い、互いに融合し、小さなものから徐々に物質を取り込んで成長しました。しかし時間とともに液滴はより硬くなっていきました。蛍光回復の測定では、液滴内部のタンパク質や周辺脂質の移動が次第に低下し、流動的な状態からより固体に近い状態へと移行していることが示されました。最終的に液滴から細い繊維状構造が伸び出し、基板となる膜を曲げチューブ状に変形させました。これらの観察は、膜に結合した液滴がα-シヌクレインが再編成してやがて疾患に関連する固い線維へと固定されるまでの一時的な液体の段階を提供することを示唆します。
膜自身が受ける変化
研究はまた、この過程でα-シヌクレインが膜に対して何をするかも調べました。モデル膜を用いた実験では、タンパク質が表面に挿入されると脂質層がより密に詰まり、圧縮しにくくなり、張力や曲率が変化することが示されました。巨視的な合成小胞をマイクロピペットで吸引すると、α-シヌクレインを加えたときに小胞は弛緩して滑り出し、膜張力の急激な低下と形状変化が明らかになりました。数時間を経るとタンパク質の膜への影響は強まりました。こうした力学的変化は界面でより硬く秩序立った環境を生み、さらなるタンパク質の集積と安定した接触を促進し、それが液滴の成長や最終的な線維形成へとフィードバックします。
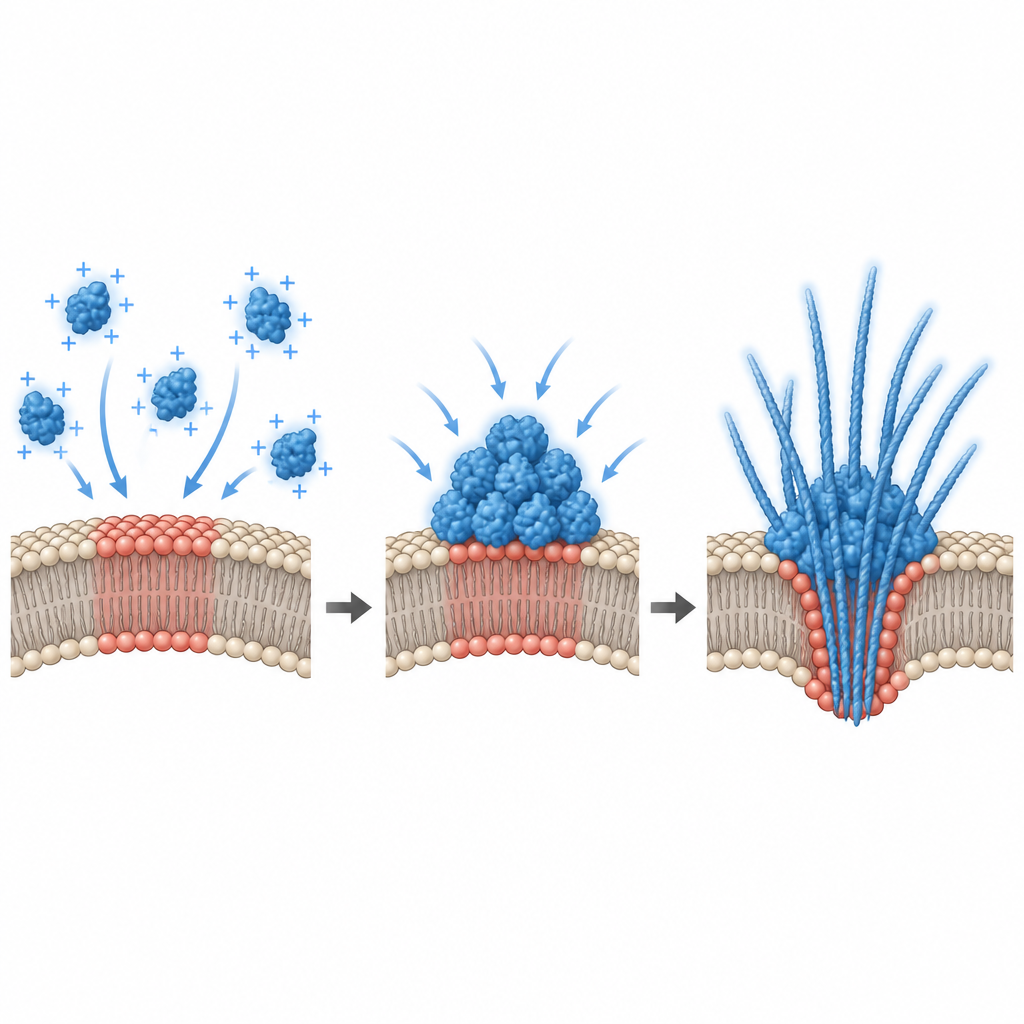
電気的表面電荷の見えざる役割
なぜ特定の脂質混合物だけが凝縮を引き起こすのかを説明するため、研究者らは膜表面の電位を測定しました。α-シヌクレインの結合は負の表面電荷が狭い範囲にあるときにのみ起こり、その範囲のしきい値近傍で強い凝縮が現れることが分かりました。計算シミュレーションもこれを支持し、引き付ける膜は「プレウェッティング様」の転移を引き起こし得ることを示しました:バルク溶液が希薄すぎて単独では相分離しない場合でも、表面に厚いタンパク質豊富な層が形成されるのです。生細胞では、チームは界面電位を二つの方法で変化させました。培養海馬細胞に負に帯電した脂質を追加すると電位が変わり既存のα-シヌクレイン斑点が縮小し、一次ニューロンを高カリウムやグルタミン酸で脱分極させるとα-シヌクレイン液滴の数と放出が増加しました。これによりニューロンの日常的な電気活動がタンパク質凝縮の場所と程度に直接結び付くことが示されます。
神経変性疾患にとっての意味
総じて、これらの発見はニューロンの特定の膜パッチが健康な脳に近いタンパク質レベルでα-シヌクレイン液滴を静かに組み立てる場所として働くという像を描きます。脂質組成や電気状態のわずかな変化が、これらの表面を凝縮が起きる領域へと傾け、液滴が硬化し線維が現れ、膜を変形させ時に破裂させながら細胞外へ凝集体を放出することがあります。この膜駆動型の経路は、神経変性においてα-シヌクレインがニューロン間で伝播する妥当な手段を提供し、膜組成や表面電位の調整が有害なタンパク質凝縮をその最初期段階で制御する手段となり得ることを示唆します。
引用: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
キーワード: α-シヌクレイン, パーキンソン病, 神経細胞膜, タンパク質凝縮, 脂質組成