Clear Sky Science · sv
Membranens gränsytpotential styr ytkondensering och fibrillering av α-synuklein i neuron
Varför detta är viktigt för hjärnhälsan
Parkinsons sjukdom och besläktade sjukdomar kännetecknas av ansamlingar av proteinet alfa‑synuklein inne i nervceller, men hur dessa ansamlingar först uppstår och sprids mellan celler har länge varit oklart. Denna studie visar att nervcellernas yttre skikt, deras membran, tyst kan samla alfa‑synuklein i små droppar vid mycket låga proteinnivåer, och att dessa droppar kan förhärda till skadliga fibrer som deformerar och till och med brister membranet. Att förstå denna dolda uppsamlingsplats på cellens yta ger ett nytt sätt att se på hur skadliga proteinansamlingar startar, växer och sprids i hjärnan.
Hur en nervcells yta kan samla lösa proteiner
Forskarnas fokus var det tunna fettlager som omger cellen, uppbyggt av en blandning av olika lipider. De fann att alfa‑synuklein, som vanligen flyter fritt inne i neuroner, kan lockas till detta membran och bilda täta droppar där, även när dess totala koncentration är extremt låg. Anmärkningsvärt var att detta endast skedde när membranet innehöll en särskild blandning av två vanliga lipider, en neutral och en negativt laddad, i förhållandet 6:4. Denna specifika kombination skapar precis de elektriska förutsättningarna vid membranytan som krävs för att attrahera och hålla kvar alfa‑synuklein. När dessa villkor inte uppfylldes, eller när samma lipider fanns som fria partiklar snarare än en kontinuerlig yta, kondenserade inte proteinet till droppar.
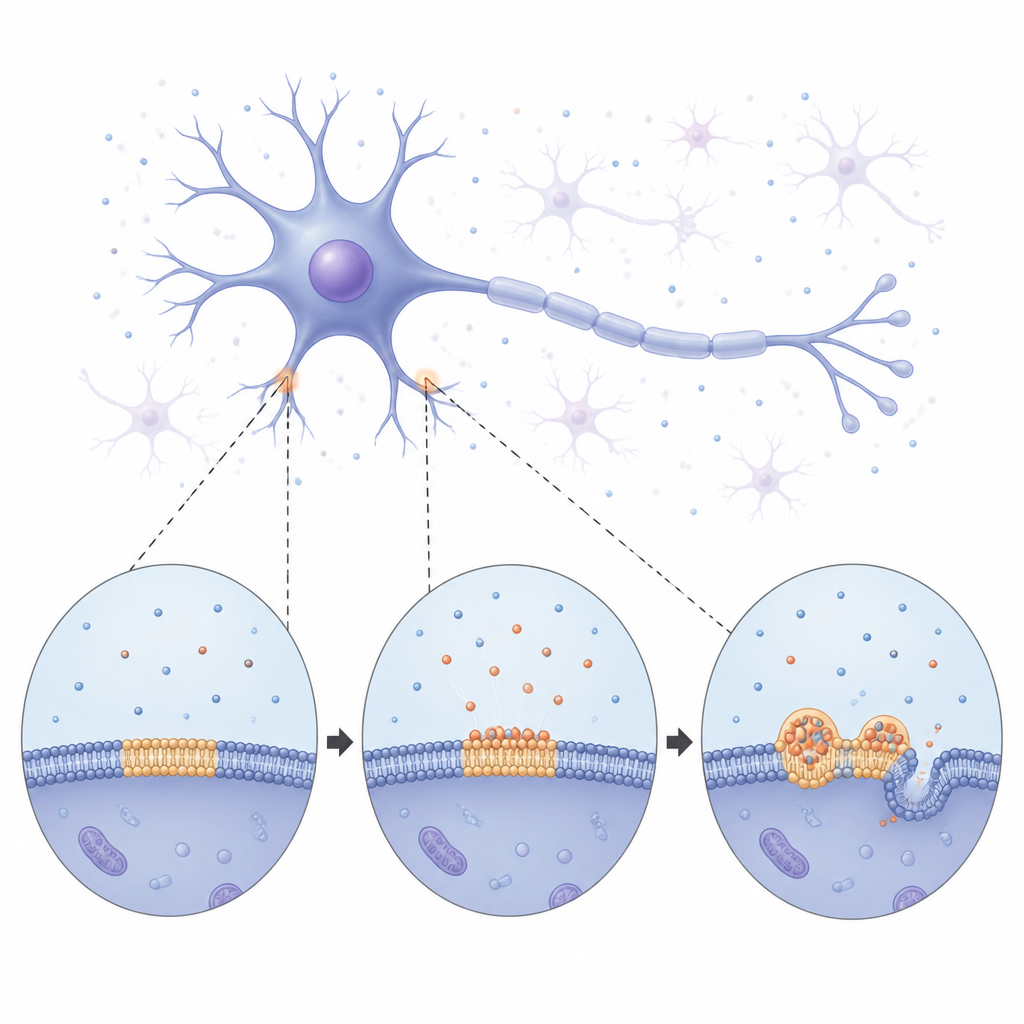
Från mjuka droppar till styva fibrer
Med hjälp av långtidsavbildning såg teamet hur alfa‑synuklein långsamt täckte membranet och sedan bröt upp i ljusa, runda kondensat utspridda över ytan. I början betedde sig dessa droppar som små flytande klumpar: de smälte samman och växte genom att långsamt avlasta material från mindre grannar. Med tiden blev dropparna dock mer styva. Mätningar av hur lätt fluorescerande signaler återhämtade sig inom dem visade att både proteinet och de omgivande lipiderna rörde sig mindre och mindre, vilket signalerar en övergång från flytande till mer fast tillstånd. Så småningom började tunna fibrillika strukturer spira från dropparna och böja samt tubulera det underliggande membranet. Dessa observationer tyder på att membranbundna droppar fungerar som temporära, flytande uppsamlingsplatser där alfa‑synuklein kan omorganisera sig innan det låses i de fasta fibrer som förknippas med sjukdom.
Hur membranet självt förändras
Studien undersökte också vad alfa‑synuklein gör med membranet medan detta pågår. Experiment med modellmembran visade att när proteinet tränger in i ytan blir lipidlagret tätare packat och mindre komprimerbart, vilket förändrar dess spänning och krökning. Jättesyntetiska vesiklar som aspirerades in i mikropipetter slappnade av och gled ut när alfa‑synuklein tillsattes, vilket avslöjade ett snabbt fall i membranspänning och formförändringar. Över timmar stärktes proteinets grepp om membranet. Dessa mekaniska skift skapar en styvare, mer ordnad miljö vid gränsytan, vilket i sin tur gynnar ökad proteinansamling och stabilare kontakter, och driver vidare droppväxt och slutlig fibrillbildning.
Den dolda rollen för elektrisk ytladdning
För att förklara varför endast vissa lipidblandningar utlöste kondensation mätte forskarna den elektriska potentialen vid membranytan. De fann att alfa‑synukleinbindning endast inträffade inom ett smalt fönster av negativ ytladdning, och att robust kondensation uppstod nära ett tröskelvärde i detta intervall. Datorsimuleringar stödde detta och visade att ett attraktiva membran kan orsaka en ”prewetting‑liknande” övergång: ett tjockt proteinrikt skikt bildas på ytan även när den omgivande lösningen är för utspädd för att själv genomgå fasskillnad. I levande celler ändrade teamet denna gränsytpotential på två sätt. Att tillsätta extra negativt laddade lipider till odlade hippocampusceller förändrade potentialen och förminskade redan befintliga alfa‑synukleinpunkter, medan depolarisering av primära neuroner med hög kalium eller glutamat ökade antalet och frisättningen av alfa‑synuklein‑droppar. Detta kopplar neuronernas dagliga elektriska aktivitet direkt till hur och var proteinet kondenserar.
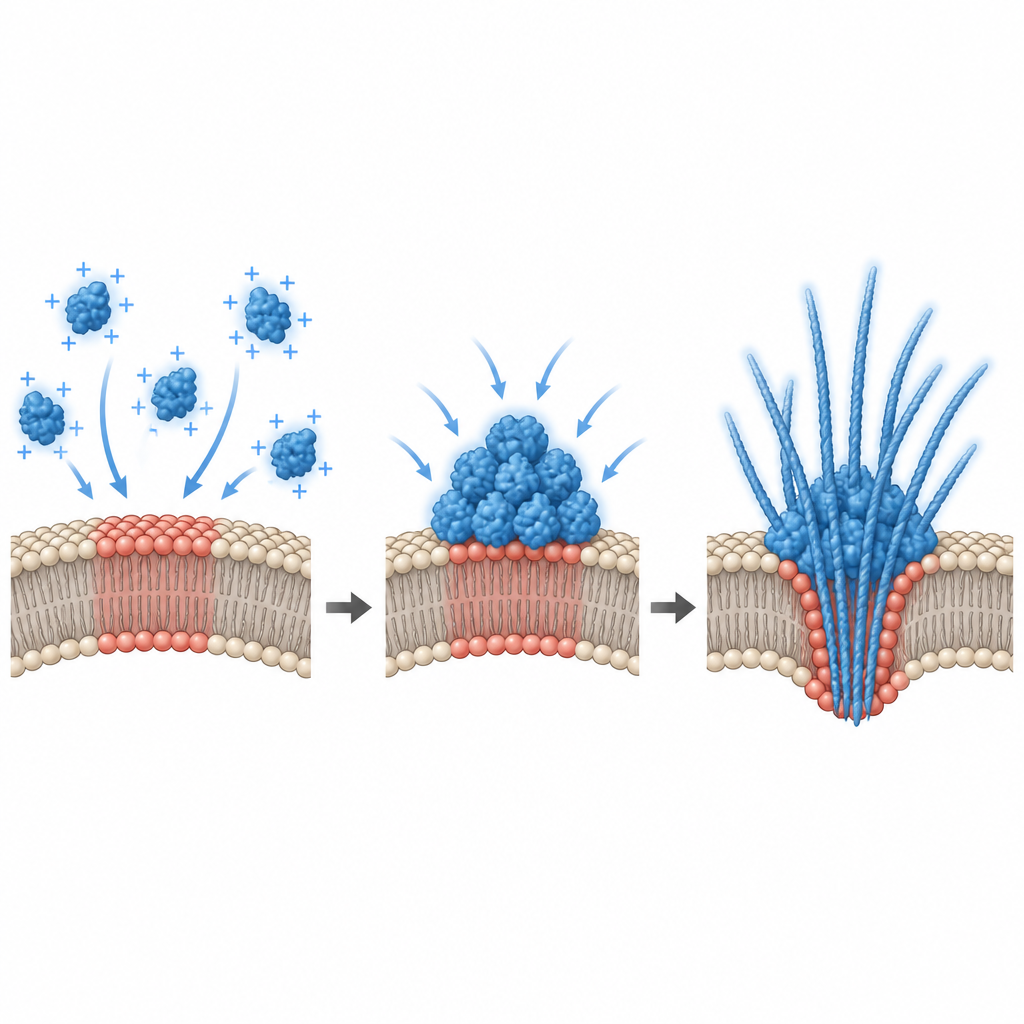
Vad detta betyder för neurodegenerativ sjukdom
Tillsammans målar dessa fynd upp en bild där specifika membranområden på neuroner fungerar som tysta monteringslinjer för alfa‑synuklein‑droppar vid proteinnivåer nära de som finns i en frisk hjärna. Små förändringar i lipidsammansättning eller elektriskt tillstånd kan föra dessa ytor in i ett läge där kondensation sker, dropparna förhårdnar och fibriller uppstår, vilket deformerar och ibland brister membranet samtidigt som proteinaggregat frigörs utanför cellen. Denna membranstyrda väg erbjuder en trovärdig mekanism för hur alfa‑synuklein kan spridas från neuron till neuron under neurodegeneration, och antyder att justering av membransammansättning eller ytpuls potential en dag skulle kunna hjälpa till att kontrollera skadlig proteinkondensation i ett tidigt skede.
Citering: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
Nyckelord: alfa‑synuklein, Parkinsons sjukdom, neuronala membran, proteinkondensation, lipidsammansättning