Clear Sky Science · de
Membran-Oberflächenpotenzial steuert Oberflächenkondensation und Fibrillierung von α-Synuclein in Neuronen
Warum das für die Gehirngesundheit wichtig ist
Die Parkinson-Krankheit und verwandte Erkrankungen sind durch Ansammlungen eines Proteins namens Alpha-Synuclein in Nervenzellen gekennzeichnet, doch wie diese Aggregate zunächst entstehen und von Zelle zu Zelle verbreitet werden, blieb bislang rätselhaft. Die vorliegende Studie zeigt, dass die äußere Hülle von Nervenzellen — ihre Membranen — Alpha-Synuclein bereits bei sehr geringen Proteinmengen unauffällig in winzige Tröpfchen sammeln kann, und dass diese Tröpfchen zu schädlichen Fasern verhärten können, die die Membran verformen und sogar zum Platzen bringen. Das Verständnis dieses verborgenen Vorbereitungsorts an der Zelloberfläche eröffnet eine neue Perspektive darauf, wie schädliche Proteinaggregate beginnen, wachsen und sich im Gehirn ausbreiten.
Wie die Zellhaut lose Proteine zusammenzieht
Die Autoren konzentrierten sich auf die dünne Fettschicht, die Zellen umgibt und aus einer Mischung unterschiedlicher Lipide besteht. Sie fanden, dass Alpha-Synuclein, das normalerweise frei im Inneren von Neuronen vorkommt, zur Membran hingezogen werden und dort dichte Tröpfchen bilden kann, selbst wenn seine Gesamtkonzentration extrem niedrig ist. Auffallend war, dass dies nur geschah, wenn die Membran eine bestimmte Mischung aus zwei verbreiteten Lipiden enthielt, einem neutralen und einem negativ geladenen, im Verhältnis 6:4. Diese spezifische Zusammensetzung schafft genau die richtigen elektrischen Bedingungen an der Membranoberfläche, um Alpha-Synuclein anzuziehen und zu halten. Werden diese Bedingungen nicht erfüllt, oder liegen dieselben Lipide als freie Partikel statt als durchgehende Oberfläche vor, kondensiert das Protein nicht zu Tröpfchen.
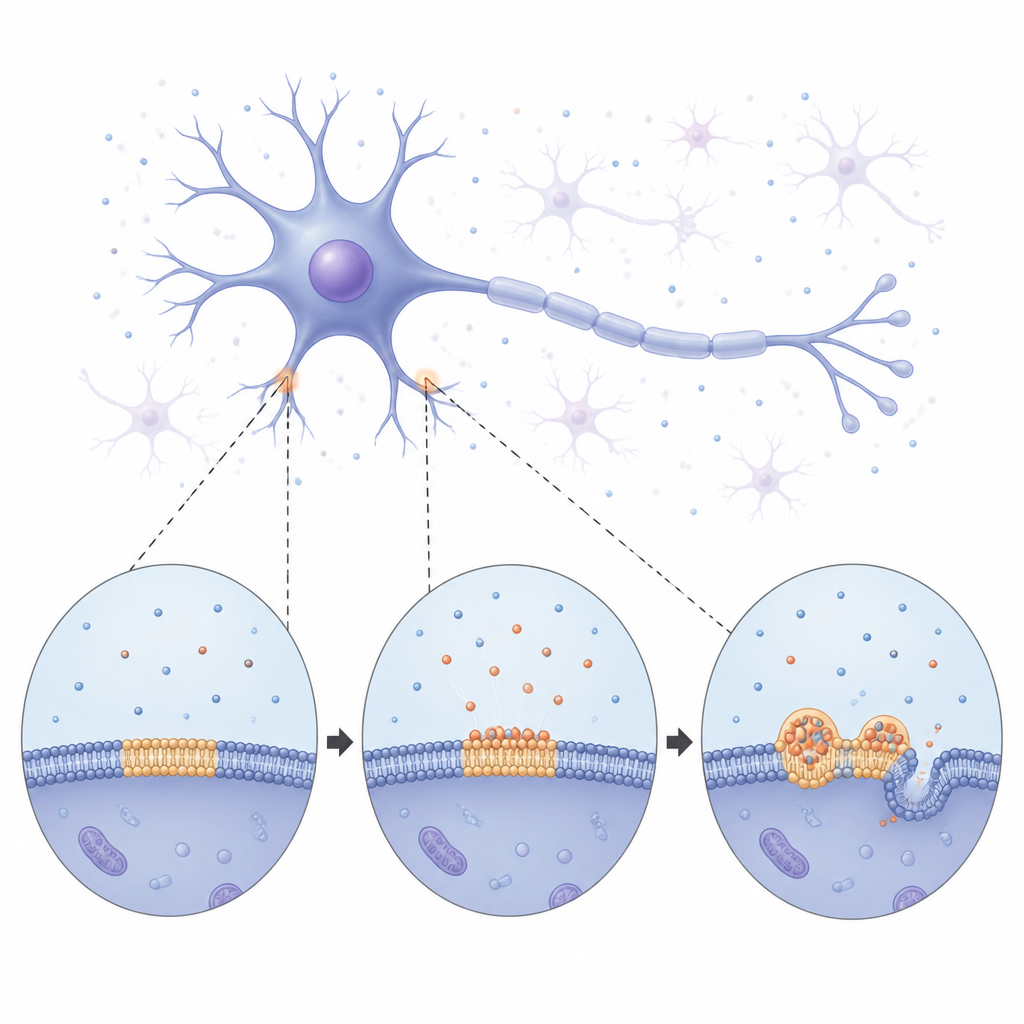
Von weichen Tröpfchen zu starren Fasern
Mit Langzeitaufnahmen beobachtete das Team, wie Alpha-Synuclein die Membran allmählich beschichtete und dann in helle, runde Kondensate zerbrach, die über die Oberfläche verteilt waren. Zunächst verhielten sich diese Tröpfchen wie winzige Flüssigkeitsblobs: sie verschmolzen miteinander und wuchsen, indem sie langsam Material von kleineren Nachbarn abzogen. Im Laufe der Zeit wurden die Tröpfchen jedoch zunehmend starrer. Messungen der Erholung fluoreszenter Signale zeigten, dass sich sowohl das Protein als auch die umgebenden Lipide immer weniger bewegten, was auf einen Übergang von einem flüssigen zu einem festeren Zustand hinweist. Schließlich begannen dünne faserartige Strukturen aus den Tröpfchen herauszuwachsen und die zugrundeliegende Membran zu biegen und zu tubulisieren. Diese Beobachtungen deuten darauf hin, dass membrangebundene Tröpfchen als temporäre, flüssige Sammelplätze dienen, in denen sich Alpha-Synuclein umorganisieren kann, bevor es in die festen Fasern übergeht, die mit Krankheit assoziiert sind.
Wie die Membran selbst verändert wird
Die Studie untersuchte auch, was Alpha-Synuclein während dieses Geschehens mit der Membran anstellt. Experimente mit Modellmembranen zeigten, dass durch das Einlagern des Proteins die Lipidschicht dichter gepackt und weniger komprimierbar wird, wodurch Spannung und Krümmung verändert werden. Riesige synthetische Vesikel, die in Mikropipetten angesaugt wurden, entspannten und rutschten heraus, sobald Alpha-Synuclein hinzugefügt wurde, was auf einen raschen Abfall der Membranspannung und Formveränderungen hinwies. Im Verlauf von Stunden verstärkte sich die Bindung des Proteins an die Membran. Diese mechanischen Veränderungen schaffen an der Schnittstelle eine steifere, geordnete Umgebung, die wiederum stärkere Proteinansammlungen und stabile Kontakte begünstigt, was weiteres Tröpfchenwachstum und schließlich Fibrillenbildung fördert.
Die verborgene Rolle elektrischer Oberflächenladung
Um zu erklären, warum nur bestimmte Lipidmischungen Kondensation auslösten, maßen die Forschenden das elektrische Potenzial an der Membranoberfläche. Sie stellten fest, dass die Bindung von Alpha-Synuclein nur innerhalb eines engen Fensters negativer Oberflächenladung erfolgte und dass starke Kondensation nahe einem Schwellenwert innerhalb dieses Bereichs auftrat. Computersimulationen untermauerten dies und zeigten, dass eine anziehende Membran einen „prewetting-ähnlichen“ Übergang hervorrufen kann: Eine dicke, proteinreiche Schicht bildet sich an der Oberfläche, selbst wenn die Lösung im Volumen zu verdünnt ist, um alleinphasig zu separieren. In lebenden Zellen veränderte das Team dieses Grenzflächenpotenzial auf zwei Wegen. Das Hinzufügen zusätzlicher negativ geladener Lipide zu kultivierten Hippocampus-Zellen veränderte das Potenzial und verkleinerte bestehende Alpha-Synuclein-Punkta, während die Depolarisation von Primärneuronen durch hohes Kalium oder Glutamat Anzahl und Freisetzung von Alpha-Synuclein-Tröpfchen erhöhte. Dies verknüpft die alltägliche elektrische Aktivität von Neuronen direkt damit, wie und wo das Protein kondensiert.
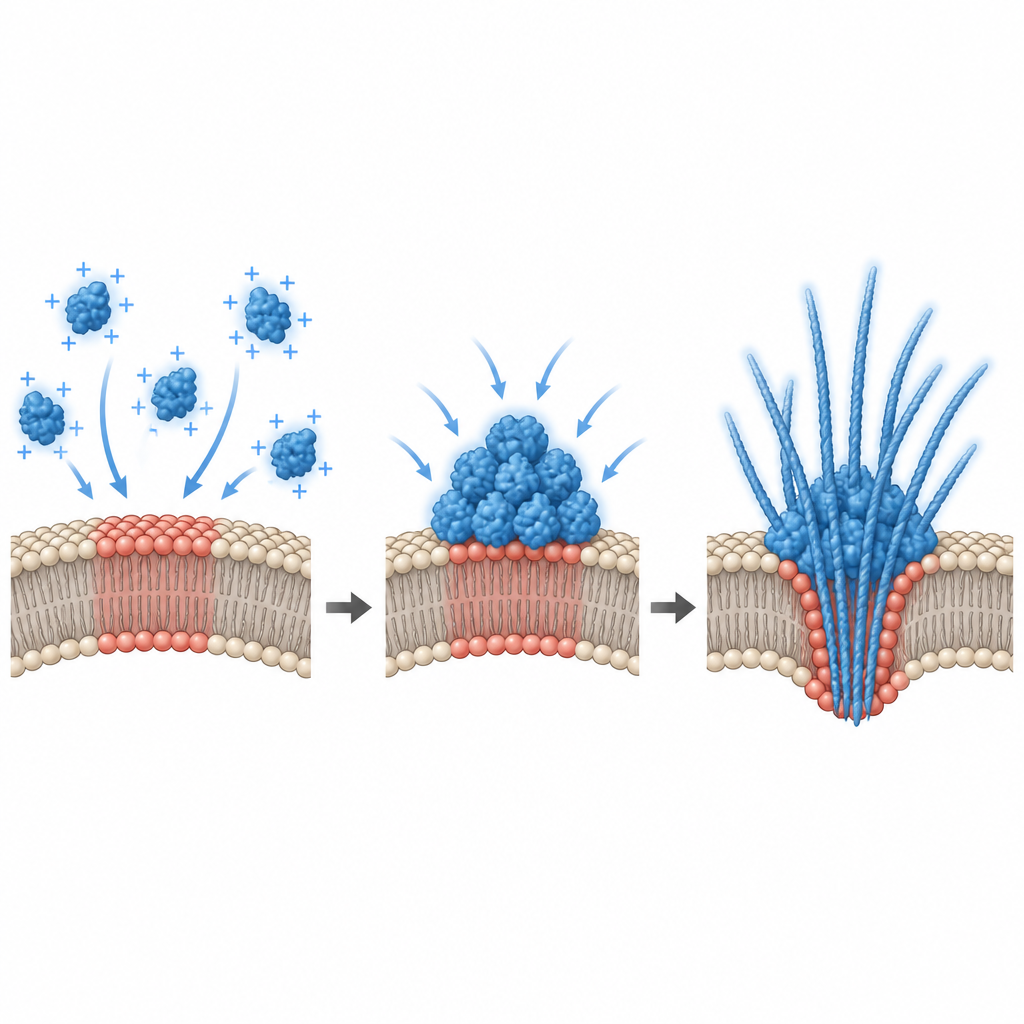
Was das für neurodegenerative Erkrankungen bedeutet
Insgesamt zeichnen diese Befunde ein Bild, in dem spezifische Membranareale von Neuronen als stille Produktionslinien für Alpha-Synuclein-Tröpfchen fungieren — und zwar bei Proteinmengen, die nahe an denen eines gesunden Gehirns liegen. Geringfügige Veränderungen in der Lipidzusammensetzung oder im elektrischen Zustand können diese Oberflächen in einen Bereich kippen, in dem Kondensation stattfindet, Tröpfchen versteifen und Fibrillen entstehen, die die Membran verformen und manchmal zum Aufreißen führen, während Proteinaggregate nach außen freigesetzt werden. Dieser membrangesteuerte Weg bietet eine plausible Route, wie Alpha-Synuclein sich während der Neurodegeneration von Neuron zu Neuron ausbreiten kann, und legt nahe, dass das Einstellen der Membranzusammensetzung oder des Oberflächenpotenzials eines Tages helfen könnte, schädliche Proteinkondensation bereits in den frühesten Stadien zu kontrollieren.
Zitation: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
Schlüsselwörter: alpha synuclein, Parkinson-Krankheit, neuronale Membranen, Proteinkondensation, Lipidzusammensetzung