Clear Sky Science · pt
O potencial interfacial da membrana governa a condensação superficial e a fibrilação da α-sinucleína em neurônios
Por que isso importa para a saúde cerebral
A doença de Parkinson e distúrbios relacionados são marcados por aglomerados de uma proteína chamada alfa-sinucleína dentro das células cerebrais, mas como esses aglomerados surgem inicialmente e se espalham de célula para célula permaneceu um mistério. Este estudo mostra que a camada externa das células nervosas, suas membranas, pode discretamente reunir alfa-sinucleína em minúsculas gotículas em níveis muito baixos da proteína, e que essas gotículas podem endurecer em fibras danosas que distorcem e até rompem a membrana. Entender esse palco escondido na superfície celular oferece uma nova maneira de pensar sobre como aglomerados proteicos nocivos começam, crescem e se movem pelo cérebro.
Como a “pele” de um neurônio consegue reunir proteínas soltas
Os autores focaram na fina camada gordurosa que envolve as células, composta por uma mistura de diferentes lipídios. Eles descobriram que a alfa-sinucleína, que normalmente flutua livremente dentro dos neurônios, pode ser atraída para essa membrana e formar gotículas densas ali, mesmo quando sua concentração global é extremamente baixa. Surpreendentemente, isso só ocorreu quando a membrana continha uma mistura particular de dois lipídios comuns, um neutro e outro carregado negativamente, numa proporção de 6:4. Essa mistura específica cria as condições elétricas adequadas na superfície da membrana para atrair e reter a alfa-sinucleína. Quando essas condições não eram atendidas, ou quando os mesmos lipídios estavam presentes como partículas livres em vez de uma superfície contínua, a proteína não se condensava em gotículas.
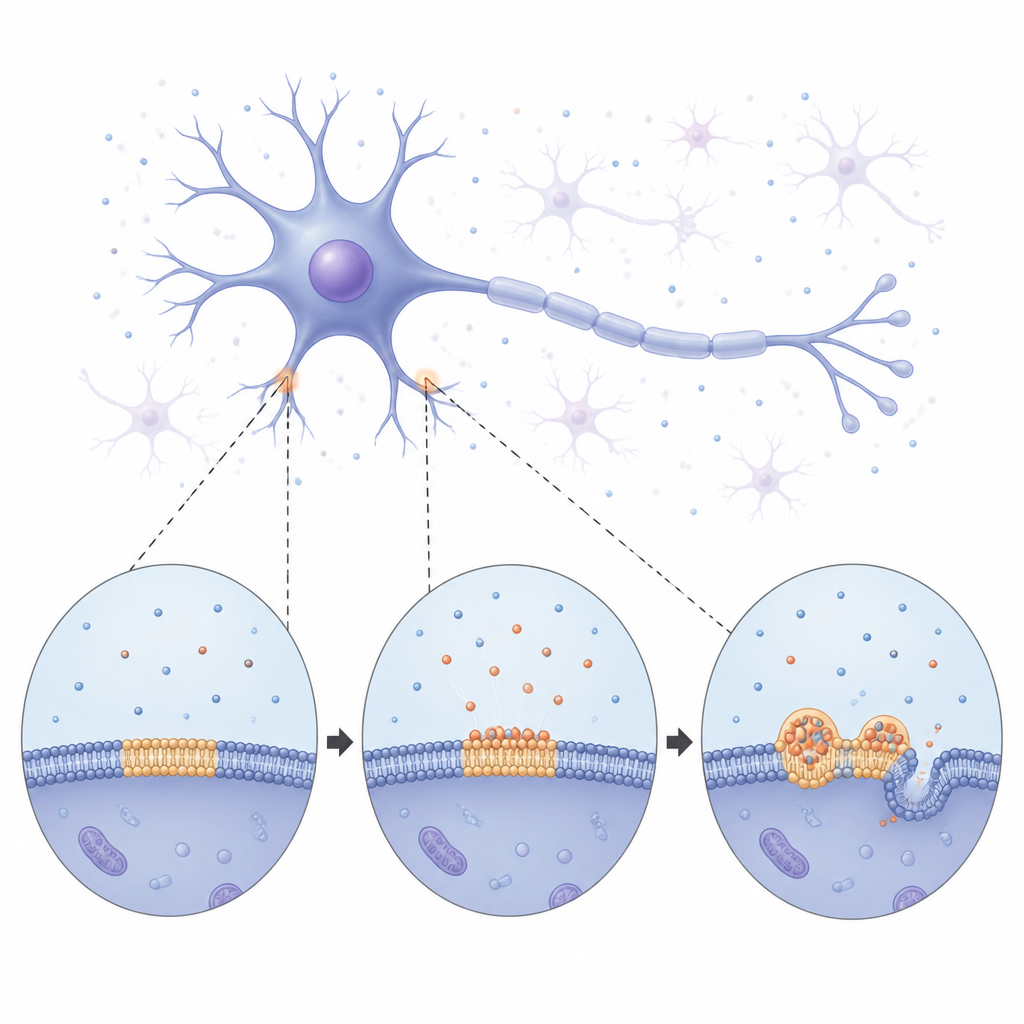
De gotículas macias a fibras rígidas
Usando imagens de longa duração, a equipe observou a alfa-sinucleína lentamente revestir a membrana e então fragmentar-se em condensados brilhantes e redondos espalhados pela superfície. A princípio essas gotículas se comportavam como pequenas massas líquidas: fundiam-se entre si e cresciam drenando material lentamente de vizinhas menores. Com o tempo, porém, as gotículas tornaram-se mais rígidas. Medidas de quão facilmente os sinais fluorescentes se recuperavam dentro delas mostraram que tanto a proteína quanto os lipídios ao redor se movimentavam cada vez menos, sinalizando uma transição de um estado fluido para um mais sólido. Eventualmente, estruturas finas semelhantes a fibras começaram a brotar das gotículas, dobrando e tubulando a membrana subjacente. Essas observações sugerem que as gotículas ligadas à membrana atuam como áreas temporárias e líquidas onde a alfa-sinucleína pode se reorganizar antes de se travar nas fibras sólidas associadas à doença.
Como a própria membrana é alterada
O estudo também investigou o que a alfa-sinucleína faz à membrana enquanto tudo isso ocorre. Experimentos com membranas modelo mostraram que quando a proteína se insere na superfície, ela torna a camada lipídica mais compacta e menos compressível, alterando sua tensão e curvatura. Vesículas sintéticas gigantes aspiradas por micropipetas relaxaram e escaparam uma vez que a alfa-sinucleína foi adicionada, revelando uma queda rápida na tensão da membrana e mudanças de forma. Ao longo de horas, a fixação da proteína à membrana se fortaleceu. Essas mudanças mecânicas criam um ambiente mais rígido e ordenado na interface, o que por sua vez favorece maior aglomeração da proteína e contatos estáveis, retroalimentando o crescimento adicional das gotículas e a formação eventual de fibrilas.
O papel oculto da carga elétrica da superfície
Para explicar por que apenas certas misturas lipídicas desencadearam a condensação, os pesquisadores mediram o potencial elétrico na superfície da membrana. Eles descobriram que a ligação da alfa-sinucleína ocorria apenas dentro de uma janela estreita de carga superficial negativa, e que uma condensação robusta aparecia perto de um valor limiar nessa faixa. Simulações por computador corroboraram isso, mostrando que uma membrana atrativa pode causar uma transição “semelhante ao pré-umedecimento”: forma-se uma camada espessa rica em proteína na superfície mesmo quando a solução em volume está diluída demais para se separar em fases por si só. Em células vivas, a equipe alterou esse potencial interfacial de duas maneiras. Adicionar lipídios extra carregados negativamente a células hipocampais cultivadas mudou o potencial e encolheu puncta pré-existentes de alfa-sinucleína, enquanto despolarizar neurônios primários com alto potássio ou glutamato aumentou o número e a liberação de gotículas de alfa-sinucleína. Isso liga a atividade elétrica cotidiana dos neurônios diretamente a como e onde a proteína se condensa.
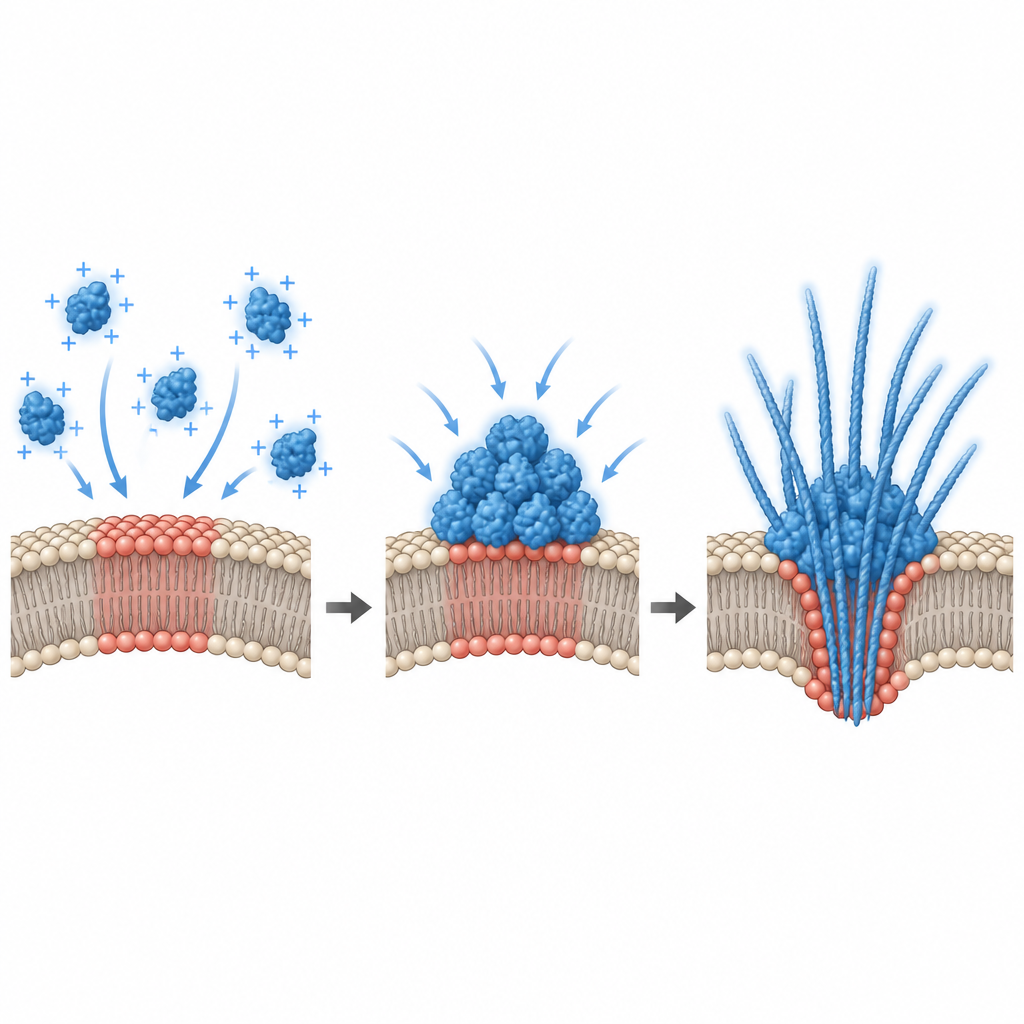
O que isso significa para doenças neurodegenerativas
Em conjunto, essas descobertas desenham um quadro em que trechos específicos da membrana neuronal atuam como linhas de montagem silenciosas para gotículas de alfa-sinucleína em níveis de proteína próximos aos encontrados no cérebro saudável. Pequenas mudanças na composição lipídica ou no estado elétrico podem levar essas superfícies a um regime onde a condensação ocorre, as gotículas se tornam rígidas e surgem fibrilas, deformando e às vezes rompendo a membrana enquanto liberam agregados proteicos para fora da célula. Essa via dirigida pela membrana oferece uma rota plausível para a propagação da alfa-sinucleína de neurônio a neurônio durante a neurodegeneração, e sugere que ajustar a composição da membrana ou o potencial de superfície poderia um dia ajudar a controlar a condensação proteica prejudicial em seus estágios iniciais.
Citação: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
Palavras-chave: alfa sinucleína, doença de Parkinson, membranas neuronais, condensação de proteínas, composição lipídica