Clear Sky Science · it
Il potenziale interfacciale delle membrane governa la condensazione superficiale e la fibrillazione di α-sinucleina nei neuroni
Perché questo è importante per la salute cerebrale
La malattia di Parkinson e i disturbi correlati sono caratterizzati da aggregati di una proteina chiamata alfa-sinucleina all’interno delle cellule cerebrali, ma resta un enigma come questi aggregati compaiano inizialmente e si diffondano da cellula a cellula. Questo studio mostra che la «pelle» esterna delle cellule nervose, le loro membrane, può silenziosamente raccogliere la alfa-sinucleina in minuscole goccioline a livelli molto bassi della proteina, e che queste goccioline possono indurirsi in fibre dannose che deformano e talvolta rompono la membrana. Comprendere questo palcoscenico nascosto sulla superficie cellulare offre un nuovo modo di pensare a come gli aggregati proteici nocivi iniziano, crescono e si spostano nel cervello.
Come la "pelle" di un neurone può raccogliere proteine sciolte
Gli autori si sono concentrati sul sottile strato grasso che circonda le cellule, composto da una miscela di diversi lipidi. Hanno scoperto che la alfa-sinucleina, che di solito fluttua liberamente all’interno dei neuroni, può essere attirata su questa membrana e formare goccioline dense lì, anche quando la sua concentrazione complessiva è estremamente bassa. Notevolmente, questo avveniva solo quando la membrana conteneva una specifica miscela di due lipidi comuni, uno neutro e uno carico negativamente, in rapporto 6:4. Quella miscela crea le condizioni elettriche giuste in superficie per attirare e trattenere la alfa-sinucleina. Quando queste condizioni non erano soddisfatte, o quando gli stessi lipidi erano presenti come particelle libere piuttosto che come superficie continua, la proteina non si condensava in goccioline.
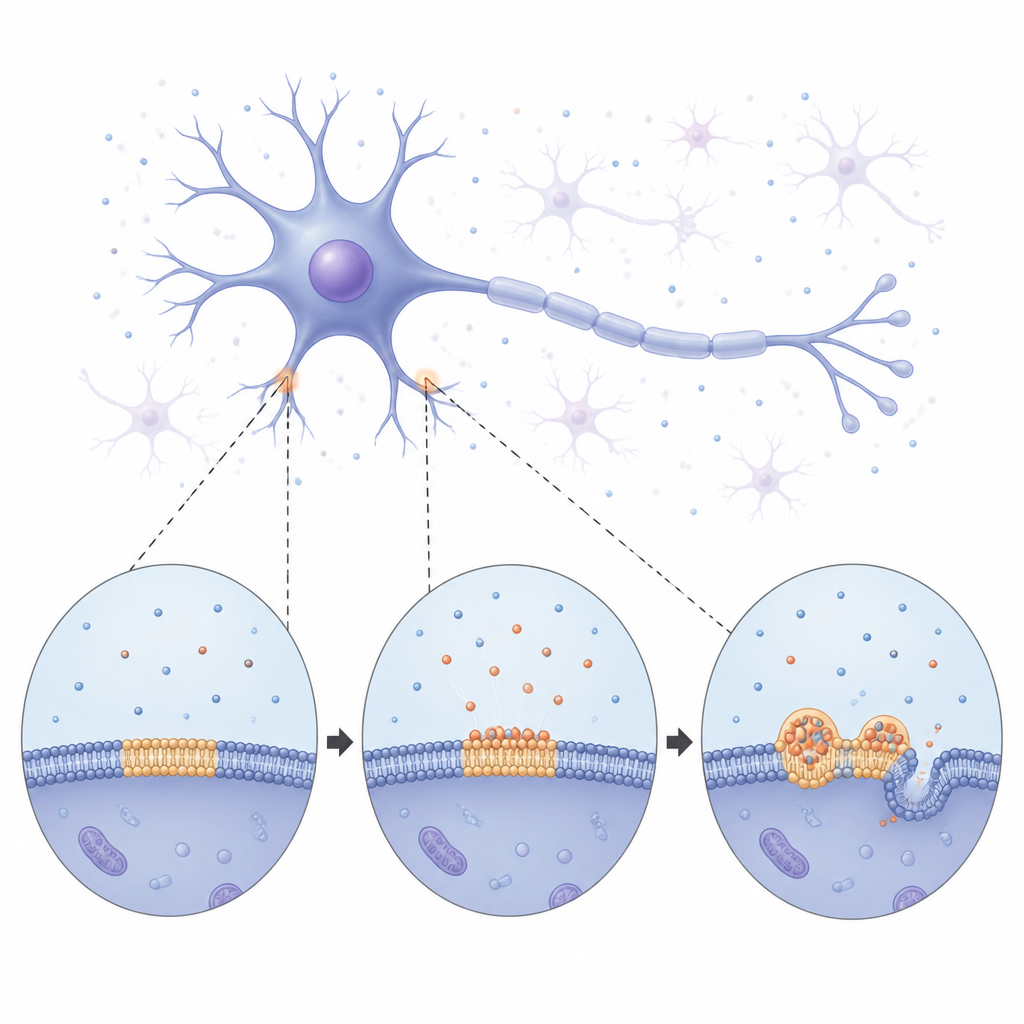
Dalle goccioline morbide alle fibre rigide
Usando imaging a lungo termine, il team ha osservato la alfa-sinucleina che lentamente rivestiva la membrana e poi si frammentava in condensati rotondi e luminosi sparsi sulla superficie. All’inizio queste goccioline si comportavano come piccole masse liquide: si fondevano tra loro e crescevano drenando lentamente materiale dai vicini più piccoli. Col tempo, tuttavia, le goccioline diventavano più rigide. Le misure di quanto facilmente i segnali fluorescenti si recuperavano al loro interno hanno mostrato che sia la proteina sia i lipidi circostanti si muovevano sempre meno, indicando una transizione da uno stato fluido a uno più solido. Alla fine, sottili strutture simili a fibre cominciavano a spuntare dalle goccioline, piegando e tubulizzando la membrana sottostante. Queste osservazioni suggeriscono che i condensati legati alla membrana fungono da aree temporanee e liquide dove la alfa-sinucleina può riorganizzarsi prima di cristallizzarsi nelle fibre solide associate alla malattia.
Come la membrana stessa viene modificata
Lo studio ha anche indagato cosa fa la alfa-sinucleina alla membrana mentre tutto ciò avviene. Esperimenti con membrane modello hanno mostrato che quando la proteina si inserisce nella superficie, rende lo strato lipidico più compatto e meno comprimibile, alterandone tensione e curvatura. Vescicole sintetiche giganti aspirate in micropipette si sono rilassate e sono scivolate fuori una volta aggiunta la alfa-sinucleina, rivelando un rapido calo della tensione di membrana e cambiamenti di forma. Nel corso di ore, la presa della proteina sulla membrana si è rafforzata. Questi cambiamenti meccanici creano un ambiente più rigido e ordinato all’interfaccia, che a sua volta favorisce un maggiore affollamento proteico e contatti stabili, alimentando ulteriormente la crescita delle goccioline e la formazione finale di fibrille.
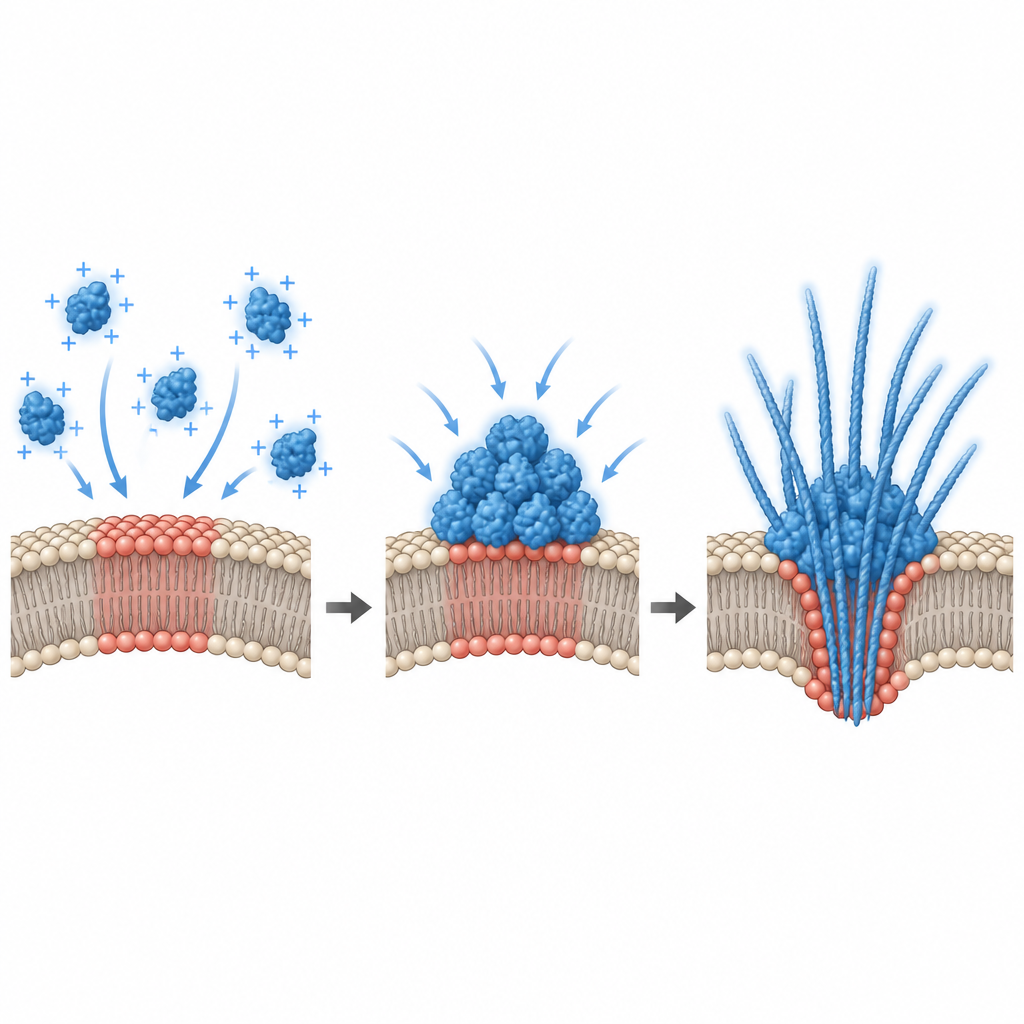
Il ruolo nascosto della carica elettrica superficiale
Per spiegare perché solo certe miscele lipidiche innescassero la condensazione, i ricercatori hanno misurato il potenziale elettrico sulla superficie della membrana. Hanno scoperto che il legame della alfa-sinucleina avveniva solo entro una finestra ristretta di carica superficiale negativa, e che una condensazione robusta compariva vicino a un valore soglia in questo intervallo. Simulazioni computazionali hanno confermato questi risultati, mostrando che una membrana attrattiva può causare una transizione «simile al pre-wetting»: si forma uno strato spesso ricco di proteine sulla superficie anche quando la soluzione bulk è troppo diluita per separarsi in fase da sola. Nelle cellule vive, il team ha modificato questo potenziale interfacciale in due modi. L’aggiunta di lipidi extra carichi negativamente in cellule ippocampali in coltura ha cambiato il potenziale e ridotto i punti preesistenti di alfa-sinucleina, mentre la depolarizzazione di neuroni primari con potassio elevato o glutammato ha aumentato il numero e il rilascio di goccioline di alfa-sinucleina. Ciò collega l’attività elettrica quotidiana dei neuroni a come e dove la proteina si condensa.
Cosa significa per le malattie neurodegenerative
Complessivamente, questi risultati disegnano un quadro in cui specifiche porzioni di membrana sui neuroni agiscono come linee di assemblaggio silenziose per goccioline di alfa-sinucleina a livelli proteici vicini a quelli presenti nel cervello sano. Piccole variazioni nella composizione lipidica o nello stato elettrico possono spostare queste superfici in un regime in cui avviene la condensazione, le goccioline si irrigidiscono e emergono fibrille che deformano e talvolta rompono la membrana rilasciando aggregati proteici all’esterno della cellula. Questa via guidata dalla membrana offre una possibile strada per la propagazione della alfa-sinucleina da neurone a neurone nella neurodegenerazione e suggerisce che modulare la composizione della membrana o il potenziale superficiale potrebbe un giorno aiutare a controllare la condensazione proteica dannosa nelle sue fasi più precoci.
Citazione: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
Parole chiave: alfa sinucleina, morbo di Parkinson, membrane neuronali, condensazione proteica, composizione lipidica