Clear Sky Science · nl
De interfaciale potentiaal van membranen stuurt oppervlakcondensatie en fibrillatie van α-synucleïne in neuronen
Waarom dit belangrijk is voor de gezondheid van de hersenen
Ziektes zoals de ziekte van Parkinson worden gekenmerkt door ophopingen van een eiwit genaamd alfa-synucleïne binnenin hersencellen, maar hoe die ophopingen aanvankelijk ontstaan en van cel tot cel verspreiden bleef onduidelijk. Deze studie laat zien dat de buitenste huid van zenuwcellen, hun membranen, stilletjes alfa-synucleïne kunnen verzamelen in kleine druppels bij zeer lage eiwitniveaus, en dat deze druppels kunnen verharden tot schadelijke vezels die het membraan vervormen en zelfs doen scheuren. Inzicht in deze verborgen stagingplaats aan het celoppervlak biedt een nieuw perspectief op hoe schadelijke eiwitophopingen beginnen, groeien en zich door de hersenen verplaatsen.
Hoe de huid van een zenuwcel losse eiwitten kan verzamelen
De auteurs concentreerden zich op de dunne vetachtige laag die cellen omgeeft, samengesteld uit een mengsel van verschillende lipiden. Ze ontdekten dat alfa-synucleïne, dat doorgaans vrij door neuronen zweeft, naar dit membraan kan worden aangetrokken en daar dichte druppels kan vormen, zelfs wanneer de totale concentratie extreem laag is. Opmerkelijk genoeg trad dit alleen op wanneer het membraan een specifieke verhouding van twee veelvoorkomende lipiden bevatte, één neutraal en één negatief geladen, in een verhouding van 6:4. Dat specifieke mengsel creëert precies de juiste elektrische omstandigheden aan het membraanoppervlak om alfa-synucleïne aan te trekken en vast te houden. Wanneer die omstandigheden niet aanwezig waren, of wanneer dezelfde lipiden als vrije deeltjes in plaats van als een continu oppervlak aanwezig waren, condenseerde het eiwit niet in druppels.
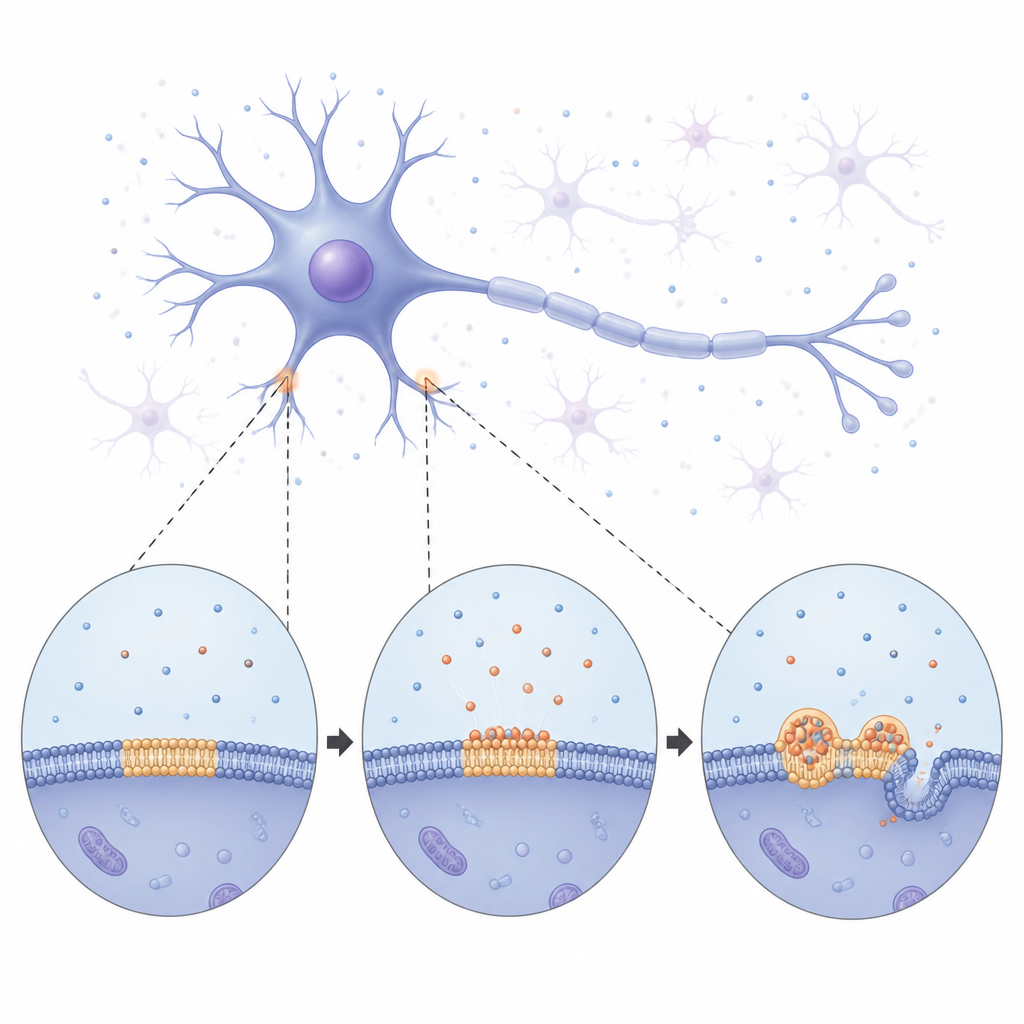
Van zachte druppels naar stijve vezels
Met langdurige beeldvorming volgde het team hoe alfa-synucleïne langzaam het membraan bedekte en vervolgens uiteenviel in heldere, ronde condensaten verspreid over het oppervlak. In het begin gedroegen deze druppels zich als kleine vloeibare bolletjes: ze smolten samen en groeiden door langzaam materiaal te onttrekken aan kleinere buren. In de loop van de tijd werden de druppels echter steeds stijver. Metingen van hoe gemakkelijk fluorescente signalen zich binnenin herstelden lieten zien dat zowel het eiwit als de omringende lipiden steeds minder bewogen, wat duidt op een verschuiving van een vloeibare naar een meer vaste toestand. Uiteindelijk begonnen uit de druppels dunne vezelachtige structuren te ontspruiten die het onderliggende membraan bogen en tubuleerden. Deze observaties suggereren dat de membraangebonden druppels fungeren als tijdelijke, vloeibare staginggebieden waar alfa-synucleïne zich kan reorganiseren voordat het vergrendelt in de vaste fibrillen die met ziekte worden geassocieerd.
Hoe het membraan zelf verandert
De studie onderzocht ook wat alfa-synucleïne met het membraan doet terwijl dit alles gebeurt. Experimenten met modelmembranen toonden aan dat wanneer het eiwit zich in het oppervlak infiltreert, het de lipidenlaag dichter verpakt en minder comprimeerbaar maakt, waardoor de spanning en kromming veranderen. Reusachtige synthetische vesikels die in micropipetten werden geïnsereerd ontspanden en uitgleed toen alfa-synucleïne werd toegevoegd, wat een snelle daling van membraanspanning en vormveranderingen aan het licht bracht. Over uren nam de greep van het eiwit op het membraan toe. Deze mechanische verschuivingen creëren een stijver, meer geordend grensvlak, wat op zijn beurt meer eiwitophoping en stabiele contacten bevordert en zo feedback geeft voor verdere druppelgroei en uiteindelijke fibrilvorming.
De verborgen rol van elektrische oppervlakte-lading
Om te verklaren waarom slechts bepaalde lipidemengsels condensatie uitlokten, maten de onderzoekers het elektrische potentiaal aan het membraanoppervlak. Ze vonden dat binding van alfa-synucleïne alleen optrad binnen een smalle band van negatieve oppervlakte-lading, en dat robuuste condensatie dichtbij een drempelwaarde in dit bereik verscheen. Computersimulaties ondersteunden dit beeld en lieten zien dat een aantrekkelijk membraan een “prewetting-achtige” overgang kan veroorzaken: er vormt zich een dikke eiwitrijk laagje op het oppervlak zelfs wanneer de bulkoplossing te verdund is om zelfstandig te fasen te scheiden. In levende cellen wijzigde het team dit interfaciale potentieel op twee manieren. Het toevoegen van extra negatief geladen lipiden aan gekweekte hippocampale cellen veranderde het potentiaal en verkleinde bestaande alfa-synucleïne-puncta, terwijl het depolariseren van primaire neuronen met hoog kalium of glutamaat het aantal en de vrijgave van alfa-synucleïne-druppels verhoogde. Dit koppelt de alledaagse elektrische activiteit van neuronen direct aan hoe en waar het eiwit condenseert.
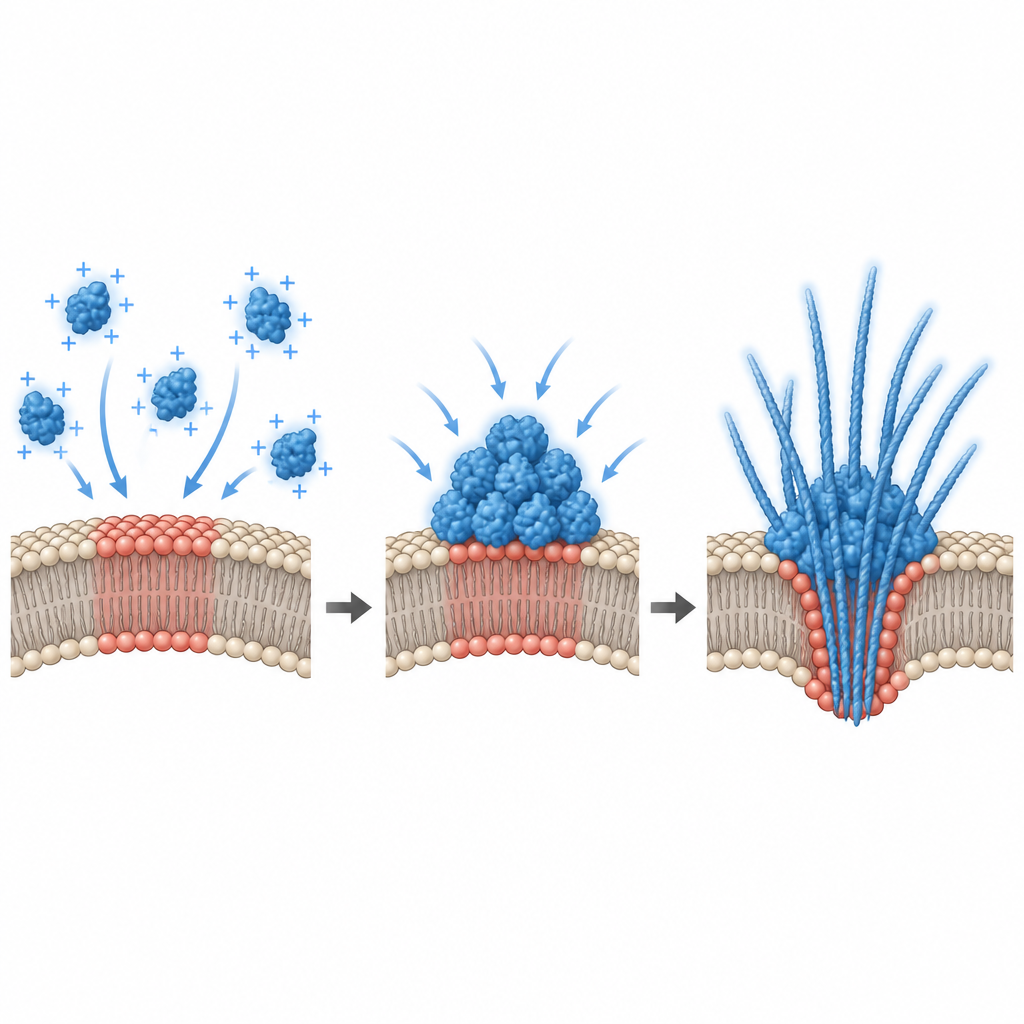
Wat dit betekent voor neurodegeneratieve ziekten
Samen schetsen deze bevindingen een beeld waarin specifieke membraanpatches op neuronen fungeren als stille assemblagelijnen voor alfa-synucleïne-druppels bij eiwitniveaus die dicht bij die in een gezond brein liggen. Kleine veranderingen in lipidesamenstelling of elektrische toestand kunnen deze oppervlakken in een regime duwen waar condensatie optreedt, druppels verstenen en fibrillen ontstaan, het membraan vervormen en soms doen scheuren terwijl eiwitaggregaten buiten de cel worden vrijgegeven. Deze door het membraan aangedreven route biedt een plausibele manier waarop alfa-synucleïne zich tijdens neurodegeneratie van neuron naar neuron kan verspreiden, en suggereert dat het afstemmen van membraansamenstelling of oppervlaktepotentiaal op termijn kan helpen schadelijke eiwitcondensatie in een vroeg stadium te beheersen.
Bronvermelding: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
Trefwoorden: alfa-synucleïne, ziekte van Parkinson, neurale membranen, eiwitcondensatie, lipidesamenstelling