Clear Sky Science · ru
Межфазный потенциал мембраны управляет поверхностной конденсацией и фибриллообразованием α‑синуклеина в нейронах
Почему это важно для здоровья мозга
Болезнь Паркинсона и родственные расстройства характеризуются скоплениями белка α‑синуклеина внутри клеток мозга, но то, как эти скопления впервые появляются и распространяются от клетки к клетке, оставалось неясным. В этом исследовании показано, что наружная оболочка нервных клеток — их мембраны — способна незаметно собирать α‑синуклеин в крошечные капли при очень низких уровнях белка, и эти капли могут затем затвердевать в повреждающие волокна, деформирующие и даже разрывающие мембрану. Понимание этой скрытой «площадки» на поверхности клетки даёт новое представление о том, как вредные белковые скопления возникают, растут и распространяются по мозгу.
Как «кожа» нейрона собирает свободные белки
Авторы сосредоточились на тонком жировом слое, окружающем клетки, который состоит из смеси разных липидов. Они обнаружили, что α‑синуклеин, обычно плавающий внутри нейронов, может притягиваться к этой мембране и образовывать там плотные капли, даже когда его средняя концентрация чрезвычайно низка. Примечательно, что это происходило только при наличии в мембране определённой смеси двух распространённых липидов — одного нейтрального и одного отрицательно заряженного — в соотношении 6:4. Такая специфическая смесь создаёт именно те электрические условия на поверхности мембраны, которые притягивают и удерживают α‑синуклеин. Когда эти условия не выполнялись, либо когда те же липиды присутствовали в виде свободных частиц, а не непрерывной поверхности, белок не конденсировался в капли.
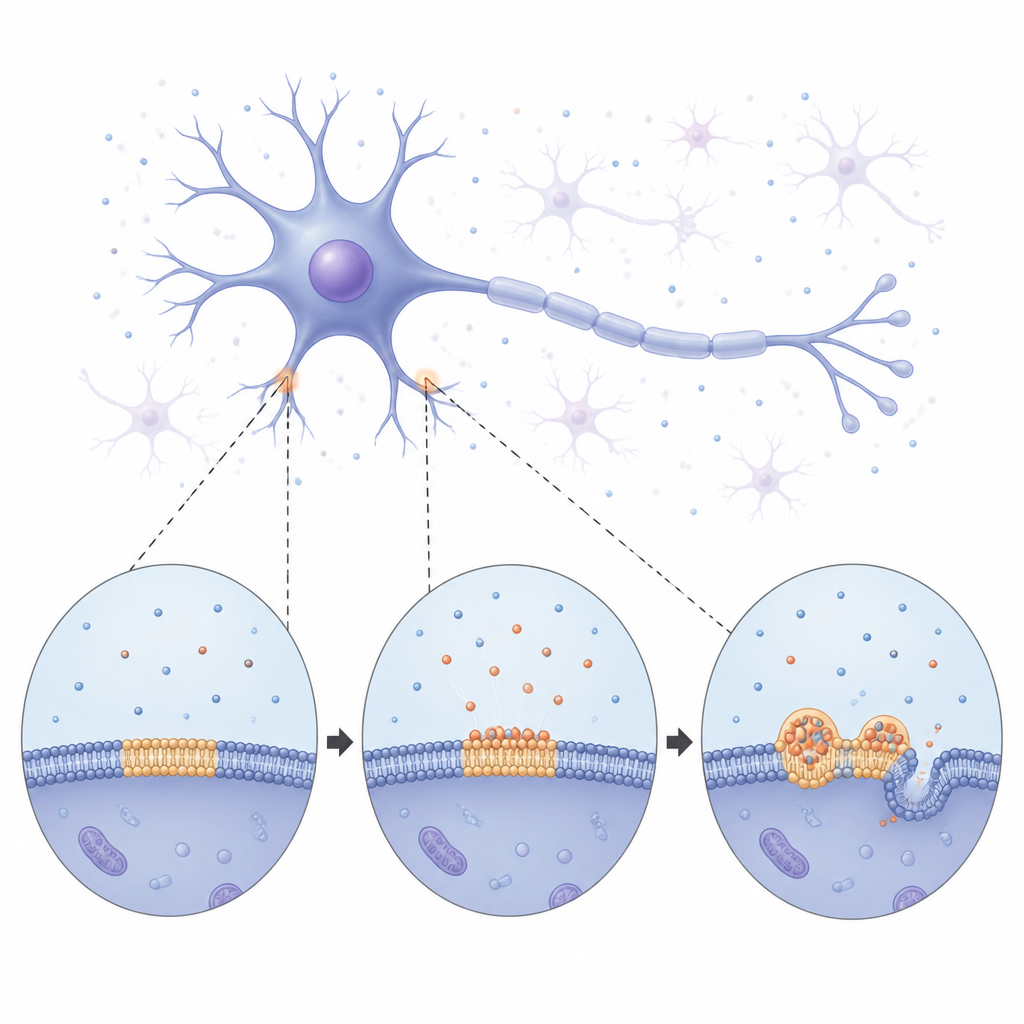
От мягких капель к жёстким волокнам
С помощью длительного видеонаблюдения команда увидела, как α‑синуклеин медленно покрывает мембрану, а затем распадается на яркие круглые конденсаты, разбросанные по поверхности. Сначала эти капли вели себя как маленькие жидкие образования: они сливались друг с другом и росли за счёт медленного перетекания вещества от меньших соседей. Со временем капли становились всё более жёсткими. Измерения восстановления флуоресцентного сигнала внутри них показали, что и белок, и окружающие липиды двигались всё медленнее, что указывает на переход от более жидкого к более твёрдому состоянию. В конце концов из капель начали вырастать тонкие волокновые структуры, искривляющие и трубкующие базовую мембрану. Эти наблюдения позволяют предположить, что мембранно-связанные капли служат временными жидкими «площадками», где α‑синуклеин может реорганизоваться перед тем, как зафиксироваться в твёрдых фибриллах, связанных с заболеванием.
Как сама мембрана меняется
Исследование также рассмотрело, что делает α‑синуклеин с мембраной в процессе. Эксперименты на модельных мембранах показали, что при внедрении белок уплотняет липидный слой и снижает его сжимаемость, изменяя натяжение и кривизну. Гигантские синтетические везикулы, аспирированные в микропипетки, расслаблялись и выскальзывали, когда добавляли α‑синуклеин, что указывало на быстрый спад напряжения мембраны и изменения формы. В течение нескольких часов сцепление белка с мембраной усиливалось. Эти механические сдвиги создают более жёсткую, упорядоченную интерфейсную среду, что в свою очередь способствует дальнейшему скоплению белка и стабилизации контактов, подпитывая рост капель и последующее образование фибрилл.
Скрытая роль электрического заряда поверхности
Чтобы объяснить, почему конденсация возникала лишь при некоторых смесях липидов, исследователи измерили электрический потенциал на поверхности мембраны. Они обнаружили, что связывание α‑синуклеина происходит только в узком диапазоне отрицательного поверхностного заряда, и что интенсивная конденсация появляется близко к пороговому значению в этом диапазоне. Компьютерные симуляции подтвердили это, показав, что привлекательная мембрана может вызвать «предмокрую» фазовую трансформацию: на поверхности формируется толстый слой, богатый белком, даже если в объёме раствор слишком разрежен для самостоятельного расслоения. В живых клетках команда меняла этот межфазный потенциал двумя способами. Добавление дополнительных отрицательно заряженных липидов в культивируемые клетки гиппокампа изменяло потенциал и уменьшало предсуществующие пятна α‑синуклеина, тогда как деполяризация первичных нейронов высоким калием или глутаматом увеличивала количество и высвобождение капель α‑синуклеина. Это связывает повседневную электрическую активность нейронов непосредственно с тем, как и где белок конденсируется.
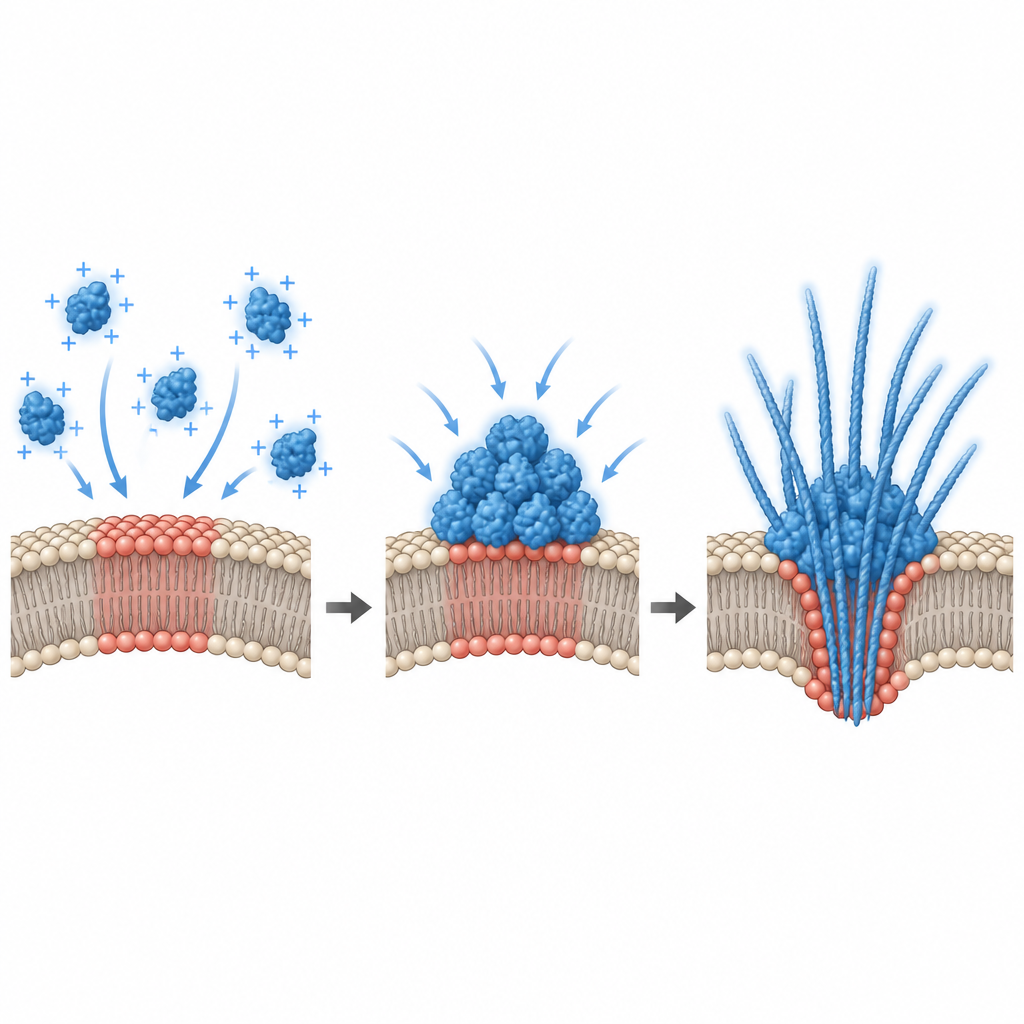
Что это значит для нейродегенеративных болезней
В совокупности эти результаты рисуют картину, в которой специфические участки мембраны нейронов действуют как тихие «конвейеры» для сборки капель α‑синуклеина при уровнях белка, близких к нормальным для здорового мозга. Небольшие изменения в липидном составе или электрическом состоянии могут перевести такие поверхности в режим, в котором происходит конденсация, капли уплотняются и появляются фибриллы, деформирующие и иногда разрывающие мембрану и выбрасывающие белковые агрегаты наружу. Этот путь, управляемый мембраной, даёт правдоподобный механизм распространения α‑синуклеина от нейрона к нейрону при нейродегенерации и указывает на то, что регулирование состава мембраны или поверхностного потенциала могло бы в перспективе помочь контролировать вредную конденсацию белка на её ранних этапах.
Цитирование: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
Ключевые слова: α‑синуклеин, болезнь Паркинсона, мембраны нейронов, конденсация белка, липидный состав