Clear Sky Science · tr
Hücre zarı arayüz potansiyeli, nöronlarda α-Synükleinin yüzey kondensasyonu ve fibrillasyonunu belirler
Beyin sağlığı için bunun önemi
Parkinson hastalığı ve ilişkili bozukluklar, beyin hücreleri içinde alfa sinüklein adı verilen bir proteinin kümelenmesiyle karakterizedir; ancak bu kümelerin ilk olarak nasıl ortaya çıktığı ve hücreden hücreye nasıl yayıldığı uzun süre bilinmezliğini korumuştu. Bu çalışma, sinir hücrelerinin dış cildi olan zarların, proteinin çok düşük seviyelerinde bile alfa sinükleini yüzeyde küçük damlacıklar halinde sessizce toplayabildiğini ve bu damlacıkların membranı bozup hatta yırtabilecek zararlı liflere sertleşebildiğini gösteriyor. Hücre yüzeyindeki bu gizli hazırlık alanını anlamak, zararlı protein kümelerinin nasıl başladığı, büyüdüğü ve beyinde hareket ettiği hakkında yeni bir bakış açısı sunuyor.
Bir sinir hücresinin zarı gevşek proteinleri nasıl toplar
Yazarlar hücreleri çevreleyen ince yağ tabakasına, yani farklı lipitlerin karışımından oluşan zar yapılarına odaklandı. Alfa sinükleinin, genellikle nöronların içinde serbestçe dolaşmasına rağmen, bu zar tarafından çekilip yüzeyde yoğun damlacıklar oluşturabildiğini ve bunun hücre içindeki genel konsantrasyon çok düşük olduğunda bile gerçekleştiğini buldular. Çarpıcı biçimde, bu yalnızca zarın belirli iki yaygın lipidin—biri nötr diğeri negatif yüklü—6:4 oranında bulunduğu durumda gözlendi. Bu özel karışım, alfa sinükleini çekip tutmak için zar yüzeyinde tam olarak gerekli elektriksel koşulları yaratıyor. Bu koşullar karşılanmadığında ya da aynı lipitler sürekli bir yüzey yerine serbest parçacıklar şeklinde bulunduğunda, protein damlacıklar halinde kondense olmadı.
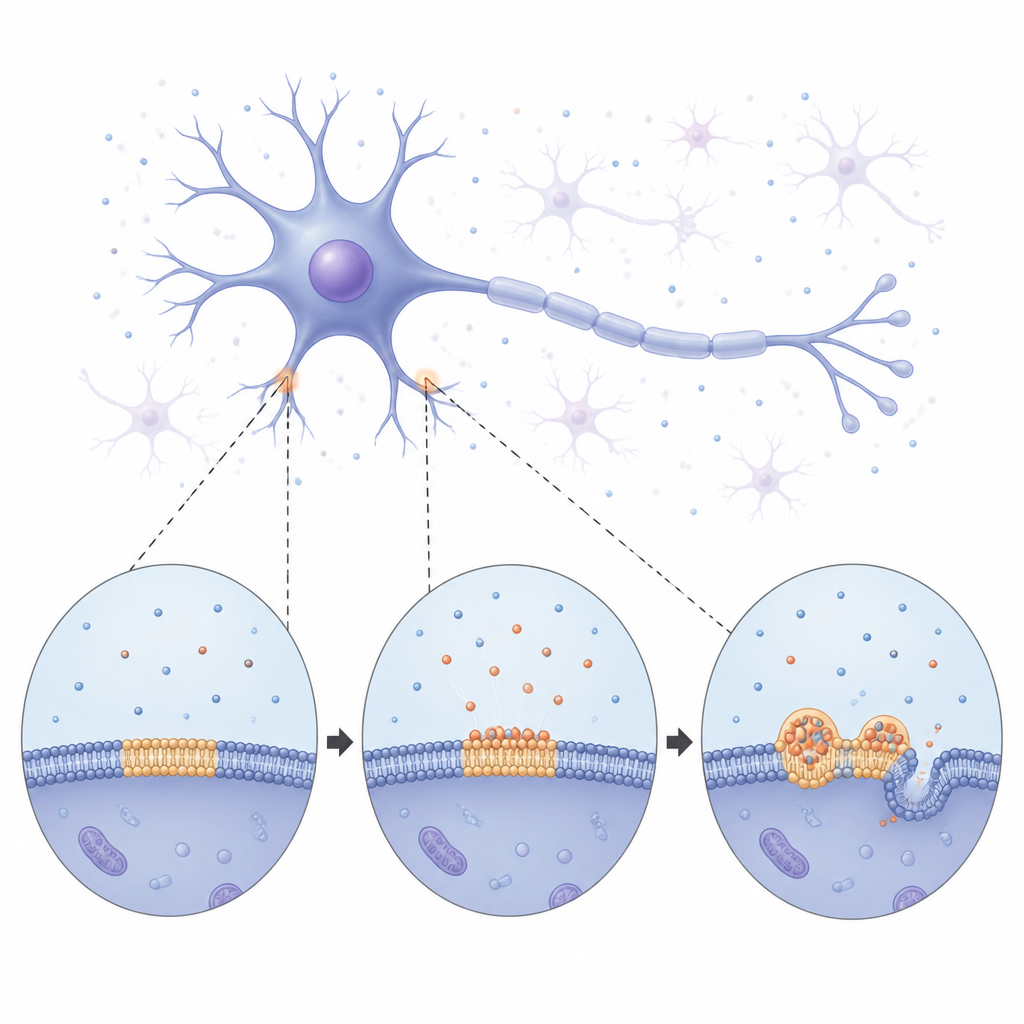
Yumuşak damlacıklardan rijit liflere
Uzun süreli görüntüleme kullanarak ekip, alfa sinükleinin yavaşça zarı kapladığını ve sonra yüzey boyunca yayılan parlak, yuvarlak kondensatlara ayrıldığını izledi. Başlangıçta bu damlacıklar küçük sıvı kabarcıkları gibi davrandı: birbirleriyle kaynaşıyor ve daha küçük komşulardan yavaşça malzeme çekerek büyüyorlardı. Ancak zamanla damlacıklar daha rijit hale geldi. İçlerindeki floresan sinyallerin toparlanma hızları ölçüldüğünde, hem proteinin hem de çevreleyen lipitlerin daha az hareket ettiği görüldü; bu, sıvı halden daha katı bir duruma geçişi işaret ediyordu. Sonunda, damlacıklardan ince lif benzeri yapılar filizlenmeye başladı ve bunlar alttaki zarı büküp tübüleştirdi. Bu gözlemler, zar bağlı damlacıkların alfa sinüklein için katı liflere kilitlenmeden önce yeniden düzenlenebileceği geçici, sıvı hazırlık alanları işlevi gördüğünü düşündürüyor.
Zarın kendisinin nasıl değiştiği
Çalışma ayrıca tüm bunlar olurken alfa sinükleinin zara ne yaptığı sorusunu da ele aldı. Model zarlarla yapılan deneyler, proteinin yüzeye girdiğinde lipit tabakasını daha sıkı paketlediğini ve daha az sıkıştırılabilir hale getirdiğini; bunun da gerilim ve eğrilik üzerinde değişiklikler yarattığını gösterdi. Mikropipetlere aspirasyon yapılan dev sentetik veziküller, alfa sinüklein eklenince gevşedi ve kaydı; bu, zar geriliminde hızlı bir düşüş ve şekil değişikliklerinin meydana geldiğini ortaya koydu. Saatler içinde proteinin zara tutunması güçlendi. Bu mekanik değişimler, arayüzde daha sert ve daha düzenli bir ortam yaratarak daha fazla protein sıkışmasını ve stabil temasları destekler; bu da damlacıkların daha fazla büyümesine ve nihayetinde fibril oluşumuna geri besleme sağlar.
Elektriksel yüzey yükünün gizli rolü
Neden yalnızca belirli lipit karışımlarının kondensasyonu tetiklediğini açıklamak için araştırmacılar zar yüzeyindeki elektriksel potansiyeli ölçtüler. Alfa sinüklein bağlanmasının yalnızca dar bir negatif yüzey yükü aralığında gerçekleştiğini ve güçlü kondensasyonun bu aralıkta bir eşik değere yakın ortaya çıktığını buldular. Bilgisayar simülasyonları bunu destekledi; çekici bir zarın “ön-ıslatma benzeri” bir geçişe neden olabileceğini gösterdiler: toplu çözelti kendi başına faz ayrışması için çok seyrelmiş olsa bile yüzeyde kalın, protein açısından zengin bir tabaka oluşuyor. Canlı hücrelerde ekip, bu arayüz potansiyelini iki yolla değiştirdi. Kültürdeki hipokampal hücrelere fazladan negatif yüklü lipit eklemek potansiyeli değiştirip önceden var olan alfa sinüklein noktalarını küçültürken; yüksek potasyum veya glutamatla primer nöronları depolarize etmek alfa sinüklein damlacıklarının sayısını ve salınımını artırdı. Bu sonuç, nöronların günlük elektriksel aktivitesini proteinin nerede ve nasıl kondense olduğuyla doğrudan ilişkilendiriyor.
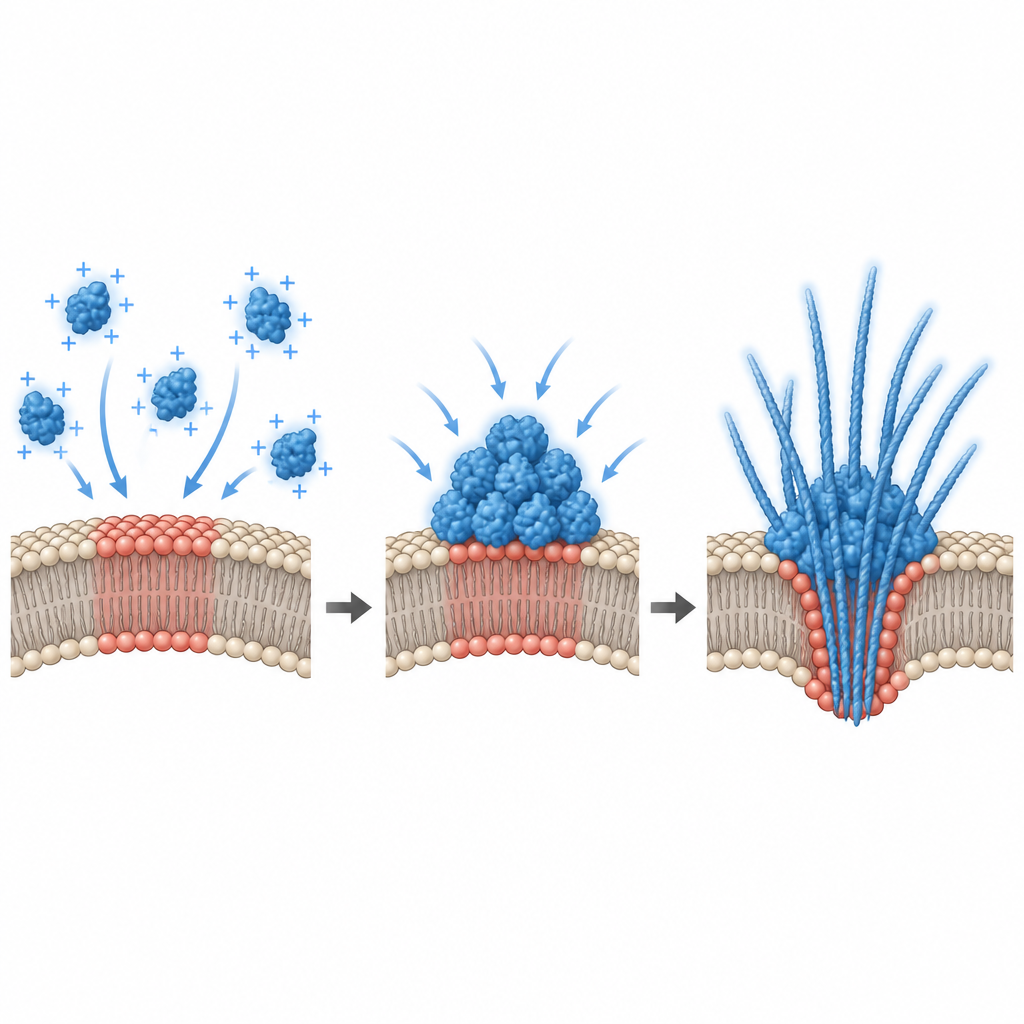
Nörodejeneratif hastalıklar için ne anlama geliyor
Birlikte ele alındığında bu bulgular, belirli nöron zar yaması bölgelerinin alfa sinüklein damlacıkları için sağlıklı beyinde bulunan protein düzeylerine yakın değerlerde bile sessiz montaj hatları gibi davrandığı bir tablo çiziyor. Lipit bileşimi veya elektriksel durumda hafif değişiklikler, bu yüzeyleri kondensasyonun ortaya çıktığı, damlacıkların sertleştiği ve fibrillerin ortaya çıktığı bir rejime itebilir; bu süreçler membranı deforme edip bazen yırtarak hücre dışına protein agregatları salınımına yol açar. Bu zar kaynaklı yolak, alfa sinükleinin nörodejenerasyon sırasında nörondan nörona yayılması için olası bir rota sunuyor ve zar bileşimini veya yüzey potansiyelini ayarlamanın zararlı protein kondensasyonunu en erken aşamalarında kontrol etmeye yardımcı olabileceğini düşündürüyor.
Atıf: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
Anahtar kelimeler: alfa sinüklein, Parkinson hastalığı, nöronal zarlar, protein kondensasyonu, lipit bileşimi