Clear Sky Science · ar
الجهد البيني للغشاء يحكم تكثف وتليف α‑سينوكلين على السطح داخل الخلايا العصبية
لماذا يهم هذا لصحة الدماغ
تتميز أمراض باركنسون والاضطرابات المرتبطة بها بتكتلات من بروتين يُسمّى ألفا‑سينوكلين داخل خلايا الدماغ، لكن كيف تظهر هذه التكتلات أولًا وتنتقل من خلية إلى أخرى ظل لغزًا. تُظهر هذه الدراسة أن غشاء الخلايا العصبية يمكنه جمع ألفا‑سينوكلين إلى قطرات دقيقة عند مستويات منخفضة جدًا من البروتين، وأن هذه القطرات قد تتصلب إلى ألياف ضارة تشوّه الغشاء وحتى تمزقه. فهم هذا المسرح الخفي على سطح الخلية يقدّم منظورًا جديدًا حول كيفية بدء ونمو وانتشار تكتلات البروتين المسببة للضرر في الدماغ.
كيف يجمع «جلد» الخلية البروتينات السائبة
ركّز المؤلفون على الطبقة الدهنية الرقيقة المحيطة بالخلايا، المصنوعة من مزيج من دهون مختلفة. وجدوا أن ألفا‑سينوكلين، الذي يطفو عادة داخل الخلايا العصبية، يمكن أن يجذب إلى هذا الغشاء ويكوّن قطرات مكثفة هناك، حتى عندما تكون تركيزاته الكلية منخفضة للغاية. اللافت أن ذلك حدث فقط عندما احتوى الغشاء على مزيج معين من دهنين شائعين، أحدهما متعادل والآخر مشحون سالبًا، بنسبة 6:4. هذا الخليط المحدد يخلق شروطًا كهربائية على سطح الغشاء تجذب وتحتجز ألفا‑سينوكلين. عندما لم تتحقق هذه الشروط، أو عندما كانت الدهون نفسها موجودة كجسيمات حرة بدلًا من سطح مستمر، لم يتكثف البروتين إلى قطرات.
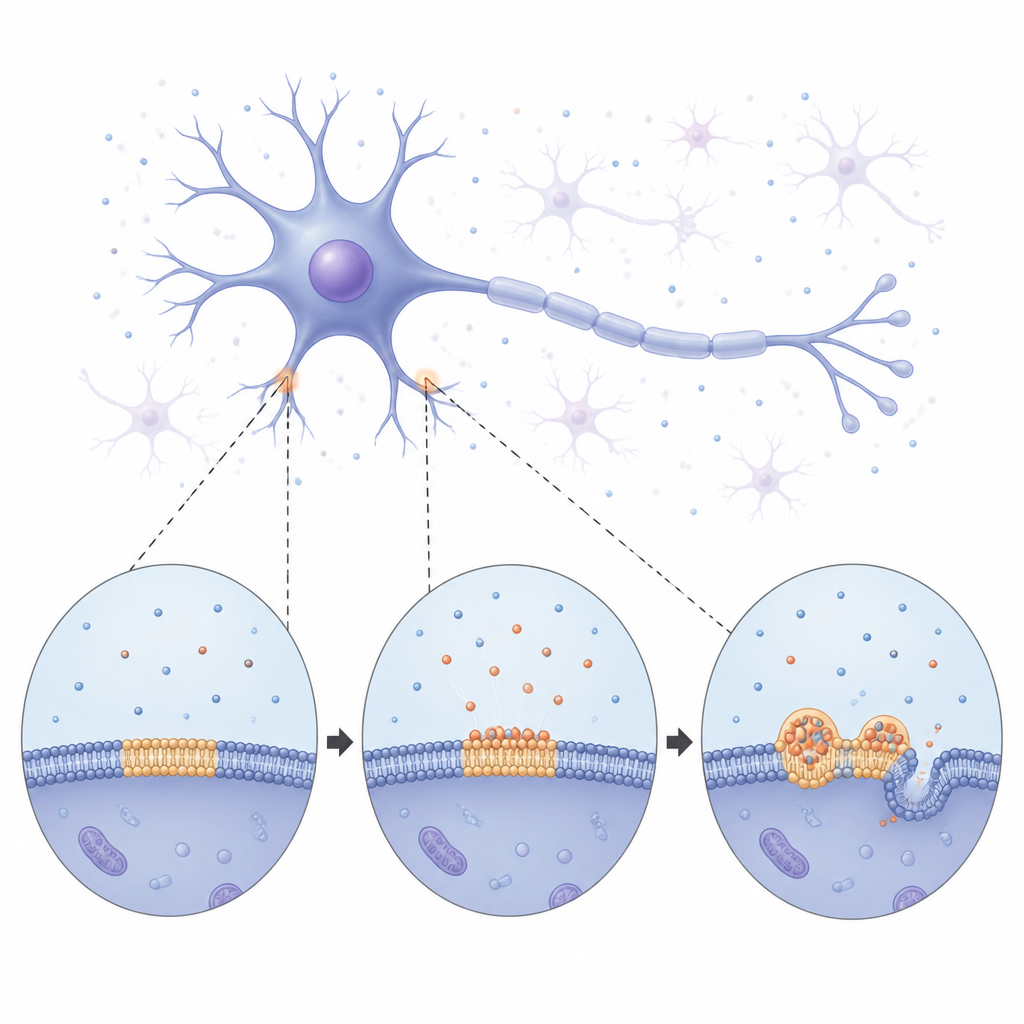
من قطرات لينة إلى ألياف جامدة
بالمراقبة على مدى زمني طويل، لاحظ الفريق أن ألفا‑سينوكلين يغطي الغشاء ببطء ثم يتفتت إلى مكثفات مستديرة ومضيئة منتشرة على السطح. في البداية تصرفت هذه القطرات كقطرات سائلة صغيرة: اندمجت مع بعضها ونمت عن طريق سحب المادة تدريجيًا من الجيران الأصغر. مع مرور الوقت، أصبحت القطرات أكثر صلابة. أظهر قياس مدى استعادة الإشارة الفلورية داخلها أن كلًا من البروتين والدهون المحيطة تحرّكا أقل فأقل، دلالة على انتقال من حالة سائلة إلى حالة أكثر صلابة. في نهاية المطاف، بدأت هياكل رفيعة شبيهة بالألياف تنبت من القطرات، مثنية ومكوّرة الغشاء الأساسي. تشير هذه الملاحظات إلى أن القطرات المرتبطة بالغشاء تعمل كمناطق مرحلية سائلة مؤقتة حيث يمكن لألفا‑سينوكلين إعادة التنظيم قبل أن يتصلب إلى الألياف الصلبة المرتبطة بالمرض.
كيف يتغير الغشاء نفسه
سألت الدراسة أيضًا ماذا يفعل ألفا‑سينوكلين للغشاء أثناء هذه العمليات. أظهرت تجارب على أغشية نموذجية أن إدخال البروتين في السطح يجعل طبقة الدهون أكثر إحكامًا وأقل قابلية للانضغاط، مغيرًا توترها وانحنائها. استرخى فقاعات اصطناعية عملاقة مأخوذة في ميكروبيبتات وانزلق بعضها للخارج بمجرد إضافة ألفا‑سينوكلين، كاشفًا عن هبوط سريع في توتر الغشاء وتغيرات شكلية. على مدى ساعات، تعمّق تشبث البروتين بالغشاء. تخلق هذه التحولات الميكانيكية بيئة أكثر صلابة ونظامية عند الواجهة، مما يعزز تكدس البروتين والروابط الثابتة، ويغذي نمو القطرات وتشكّل الألياف لاحقًا.
الدور الخفي لشحنة السطح الكهربائية
لتوضيح لماذا حفّزت تراكيبات دهونية معينة فقط التكثف، قاس الباحثون الجهد الكهربائي عند سطح الغشاء. وجدوا أن ارتباط ألفا‑سينوكلين حدث فقط ضمن نافذة ضيقة من الشحنة السطحية السالبة، وأن التكثف القوي ظهر قرب قيمة عتبة في هذا النطاق. دعمت المحاكاة الحاسوبية هذا الاستنتاج، مبينة أن غشاءً جذابًا يمكن أن يسبب انتقالًا «شبيهًا بمرحلة ما قبل البلل»: تتكوّن طبقة سميكة غنية بالبروتين على السطح حتى عندما يكون المحلول العام مخففًا جدًا ليخضع للتفكك الطوري بمفرده. في الخلايا الحية، غيّر الفريق هذا الجهد البيني بطريقتين. إضافة دهون سالبة الشحنة إلى خلايا الحُصين المزروعة عدّلت الجهد وقلّصت البقع المسبقة لألفا‑سينوكلين، بينما أدى إزالة الاستقطاب من الخلايا الأولية بتركيز عالٍ من البوتاسيوم أو الغلوتامات إلى زيادة عدد وإفراز قطرات ألفا‑سينوكلين. يربط هذا النشاط الكهربائي اليومي للخلايا العصبية مباشرة بكيفية ومكان تكثف البروتين.
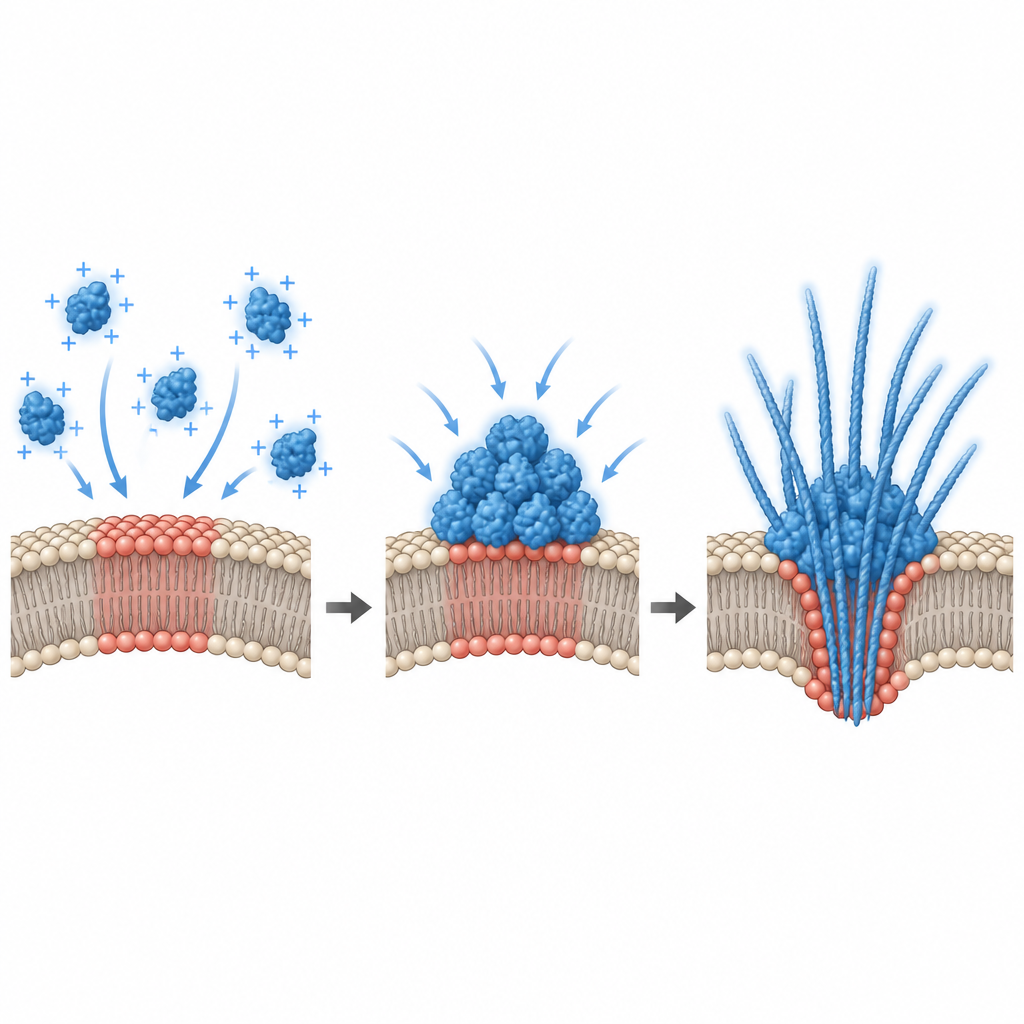
ماذا يعني هذا لأمراض التنكس العصبي
معًا، تصوّر هذه النتائج مشهدًا تعمل فيه بقع غشائية محددة على الخلايا العصبية كخطوط تجميع صامتة لقطرات ألفا‑سينوكلين عند مستويات قريبة من تلك الموجودة في الدماغ السليم. تغييرات طفيفة في تركيبة الدهون أو الحالة الكهربائية قد تقود هذه الأسطح إلى نظام حيث يحدث التكثف، وتتصلب القطرات، وتظهر الألياف التي تشوّه وأحيانًا تمزق الغشاء بينما تطلق تجمعات بروتينية إلى خارج الخلية. يقدّم هذا المسار المدفوع بالغشاء مسارًا معقولًا لانتقال ألفا‑سينوكلين من خلية عصبية إلى أخرى أثناء التنكس العصبي، ويقترح أن تعديل تركيب الغشاء أو جهده السطحي قد يساعد يومًا ما في التحكم بمراحل مبكرة من تكثف البروتين الضار.
الاستشهاد: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
الكلمات المفتاحية: ألفا‑سينوكلين, مرض باركنسون, أغشية عصبية, تكثف البروتين, تركيب الدهون