Clear Sky Science · es
El potencial interfacial de la membrana gobierna la condensación superficial y la fibrilación de α-sinucleína en neuronas
Por qué esto importa para la salud cerebral
La enfermedad de Parkinson y trastornos relacionados se caracterizan por agregados de una proteína llamada alfa sinucleína dentro de las células cerebrales, pero sigue sin quedar claro cómo aparecen por primera vez estos agregados y cómo se propagan de célula a célula. Este estudio muestra que la capa externa de las neuronas, sus membranas, puede reunir silenciosamente la alfa sinucleína en pequeñas gotas incluso a niveles muy bajos de la proteína, y que estas gotas pueden endurecerse en fibras dañinas que deforman e incluso rompen la membrana. Comprender este escenario clandestino en la superficie celular ofrece una forma nueva de pensar cómo comienzan, crecen y se mueven los agregados proteicos perjudiciales en el cerebro.
Cómo la “piel” de una neurona puede concentrar proteínas sueltas
Los autores se centraron en la delgada capa grasa que rodea a las células, compuesta por una mezcla de distintos lípidos. Encontraron que la alfa sinucleína, que normalmente flota libre dentro de las neuronas, puede ser atraída hacia esta membrana y formar gotas densas en ella, incluso cuando su concentración global es extremadamente baja. Sorprendentemente, esto solo ocurrió cuando la membrana contenía una mezcla particular de dos lípidos comunes, uno neutro y otro con carga negativa, en una proporción 6:4. Esa mezcla específica crea las condiciones eléctricas adecuadas en la superficie de la membrana para atraer y retener la alfa sinucleína. Cuando no se daban estas condiciones, o cuando los mismos lípidos estaban presentes como partículas libres en lugar de una superficie continua, la proteína no se condensaba en gotas.
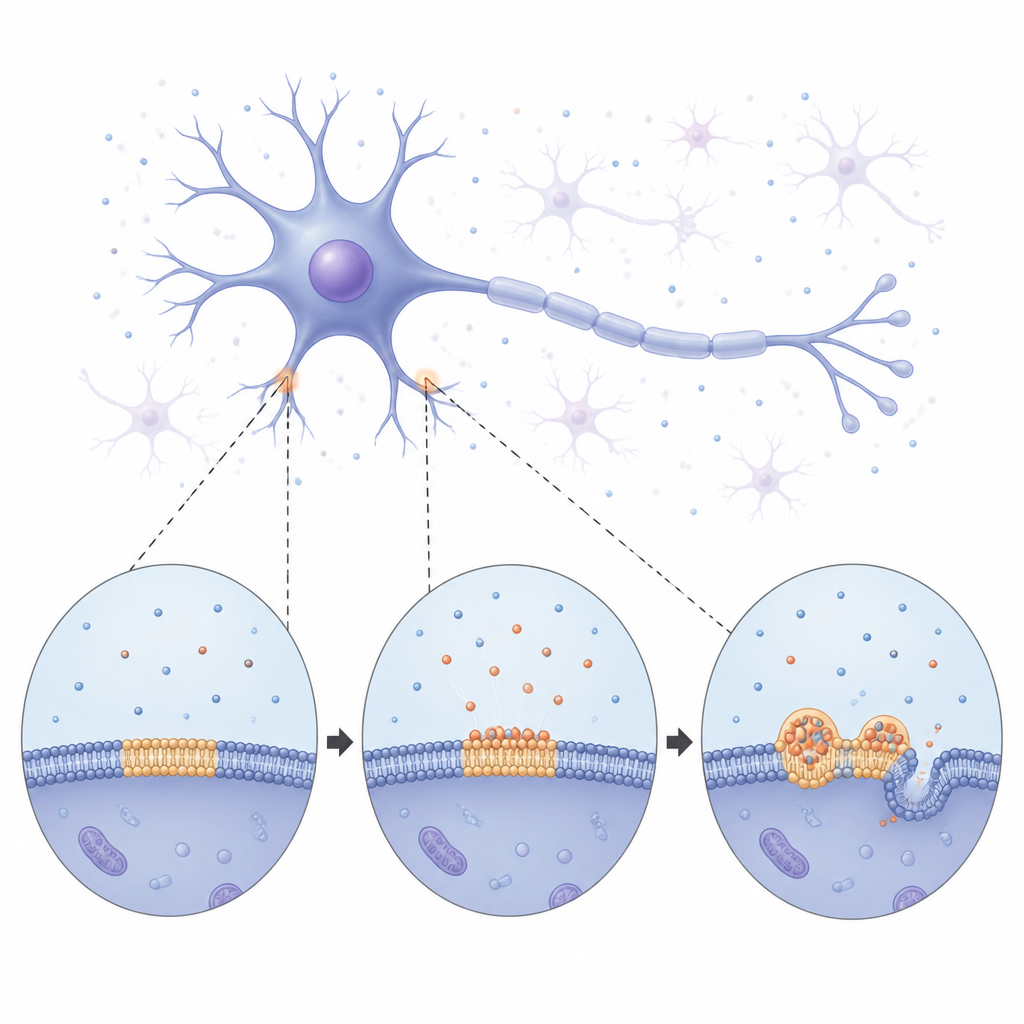
De gotas blandas a fibras rígidas
Mediante imágenes a largo plazo, el equipo observó cómo la alfa sinucleína recubría lentamente la membrana y luego se fragmentaba en condensados brillantes y redondeados repartidos por la superficie. Al principio, estas gotas se comportaban como pequeñas gotas líquidas: se fusionaban entre sí y crecían drenando material de vecinas más pequeñas. Con el tiempo, sin embargo, las gotas se volvían más rígidas. Mediciones de la recuperación de señales fluorescentes en su interior mostraron que tanto la proteína como los lípidos circundantes se movían cada vez menos, indicando un cambio de un estado fluido a otro más sólido. Eventualmente, empezaron a brotar de las gotas estructuras delgadas semejantes a fibras, que doblaban y tubularizaban la membrana subyacente. Estas observaciones sugieren que las gotas unidas a la membrana actúan como áreas de ensayo temporales y líquidas donde la alfa sinucleína puede reorganizarse antes de fijarse en las fibras sólidas asociadas a la enfermedad.
Cómo se modifica la propia membrana
El estudio también investigó qué hace la alfa sinucleína a la membrana mientras ocurre todo esto. Experimentos con membranas modelo mostraron que cuando la proteína se inserta en la superficie, hace que la capa lipídica se empaquete más estrechamente y sea menos compresible, alterando su tensión y curvatura. Vesículas sintéticas gigantes aspiradas en micropipetas se relajaron y deslizaron al añadir alfa sinucleína, revelando una caída rápida de la tensión de membrana y cambios de forma. A lo largo de horas, la unión de la proteína a la membrana se fortaleció. Estos cambios mecánicos crean un entorno más rígido y ordenado en la interfaz, lo que a su vez favorece una mayor aglomeración proteica y contactos estables, retroalimentando el crecimiento de las gotas y la eventual formación de fibrillas.
El papel oculto de la carga eléctrica superficial
Para explicar por qué solo ciertas mezclas de lípidos provocaban la condensación, los investigadores midieron el potencial eléctrico en la superficie de la membrana. Encontraron que la unión de alfa sinucleína se producía únicamente dentro de una ventana estrecha de carga superficial negativa, y que una condensación robusta aparecía cerca de un valor umbral en ese rango. Simulaciones por ordenador respaldaron estos resultados, mostrando que una membrana atractiva puede causar una transición “similar al prehumedecimiento”: se forma una capa gruesa rica en proteína en la superficie incluso cuando la solución en bloque está demasiado diluida para separarse en fases por sí sola. En células vivas, el equipo alteró este potencial interfacial de dos maneras. Añadir lípidos extra con carga negativa a células de hipocampo en cultivo cambió el potencial y redujo los puntos preexistentes de alfa sinucleína, mientras que despolarizar neuronas primarias con alto potasio o glutamato aumentó el número y la liberación de gotas de alfa sinucleína. Esto vincula la actividad eléctrica cotidiana de las neuronas directamente con cómo y dónde se condensa la proteína.
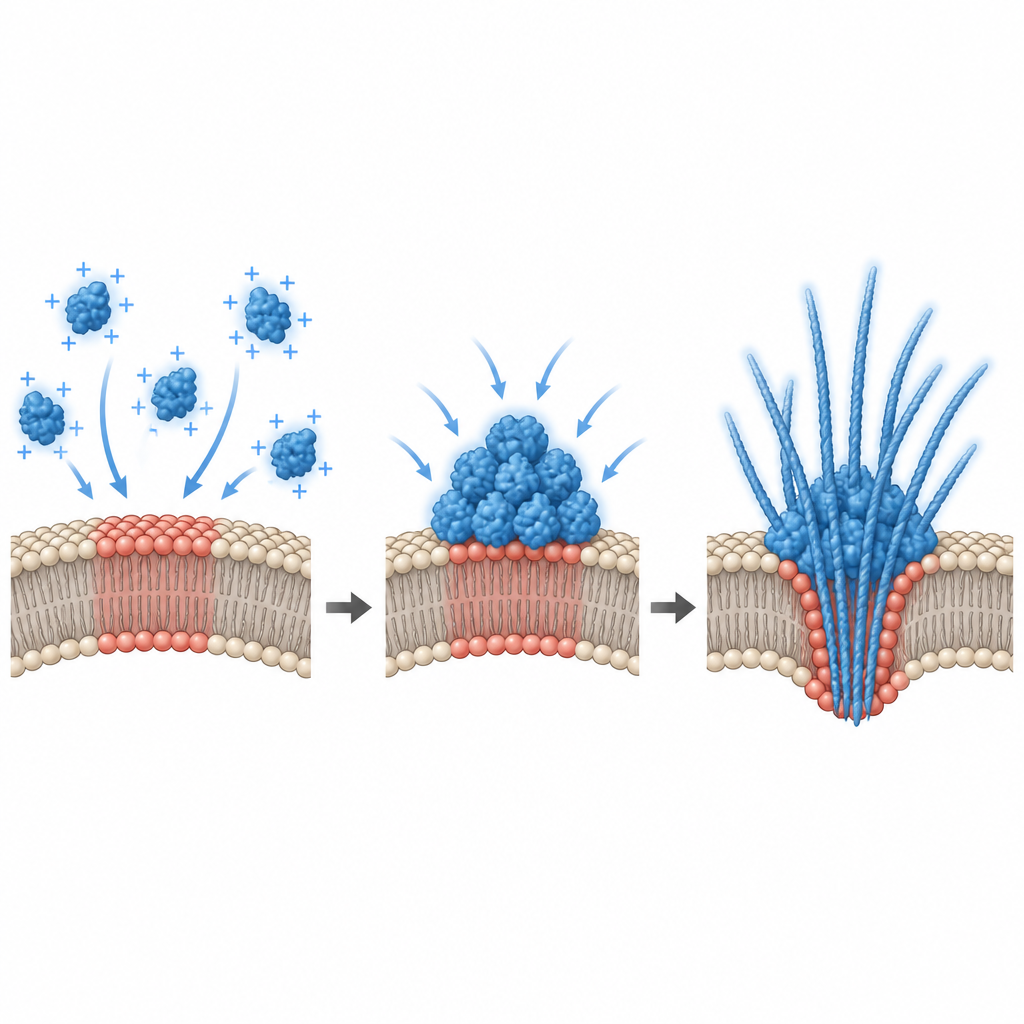
Qué significa esto para las enfermedades neurodegenerativas
En conjunto, estos hallazgos dibujan un panorama en el que parches específicos de membrana en las neuronas actúan como líneas de ensamblaje silenciosas para gotas de alfa sinucleína a niveles de proteína cercanos a los que se encuentran en el cerebro sano. Pequeños cambios en la composición lipídica o en el estado eléctrico pueden inclinar estas superficies hacia un régimen donde ocurre la condensación, las gotas se endurecen y emergen fibrillas que deforman y a veces rompen la membrana mientras liberan agregados proteicos fuera de la célula. Esta vía impulsada por la membrana ofrece una ruta plausible para que la alfa sinucleína se propague de neurona a neurona durante la neurodegeneración, y sugiere que ajustar la composición de la membrana o el potencial superficial podría algún día ayudar a controlar la condensación proteica dañina en sus etapas más tempranas.
Cita: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
Palabras clave: alfa sinucleína, enfermedad de Parkinson, membranas neuronales, condensación de proteínas, composición lipídica