Clear Sky Science · fr
Le potentiel interfacial de la membrane régit la condensation en surface et la fibrillation de l’α-synucléine dans les neurones
Pourquoi c’est important pour la santé cérébrale
La maladie de Parkinson et des troubles apparentés se caractérisent par des amas d’une protéine appelée alpha-synucléine à l’intérieur des cellules cérébrales, mais la façon dont ces amas apparaissent et se propagent d’une cellule à l’autre restait énigmatique. Cette étude montre que l’enveloppe externe des neurones, leur membrane, peut discrètement rassembler l’alpha-synucléine en toutes petites gouttelettes à des concentrations très faibles de la protéine, et que ces gouttelettes peuvent se solidifier en fibres dommageables qui déforment et parfois rompent la membrane. Comprendre cet espace de préparation caché à la surface cellulaire offre une nouvelle perspective sur la manière dont les agrégats protéiques nocifs démarrent, croissent et se propagent dans le cerveau.
Comment la « peau » d’un neurone peut rassembler des protéines libres
Les auteurs se sont concentrés sur la fine couche lipidique qui entoure les cellules, composée d’un mélange de lipides différents. Ils ont découvert que l’alpha-synucléine, qui circule habituellement librement à l’intérieur des neurones, peut être attirée vers cette membrane et y former des gouttelettes denses, même lorsque sa concentration globale est extrêmement faible. De manière frappante, cela n’est survenu que lorsque la membrane contenait un mélange particulier de deux lipides courants, l’un neutre et l’autre chargé négativement, dans un rapport 6:4. Ce mélange précis crée les conditions électriques adéquates à la surface membranaire pour attirer et retenir l’alpha-synucléine. Lorsque ces conditions n’étaient pas réunies, ou lorsque ces mêmes lipides étaient présents sous forme de particules libres plutôt que comme surface continue, la protéine ne se condensait pas en gouttelettes.
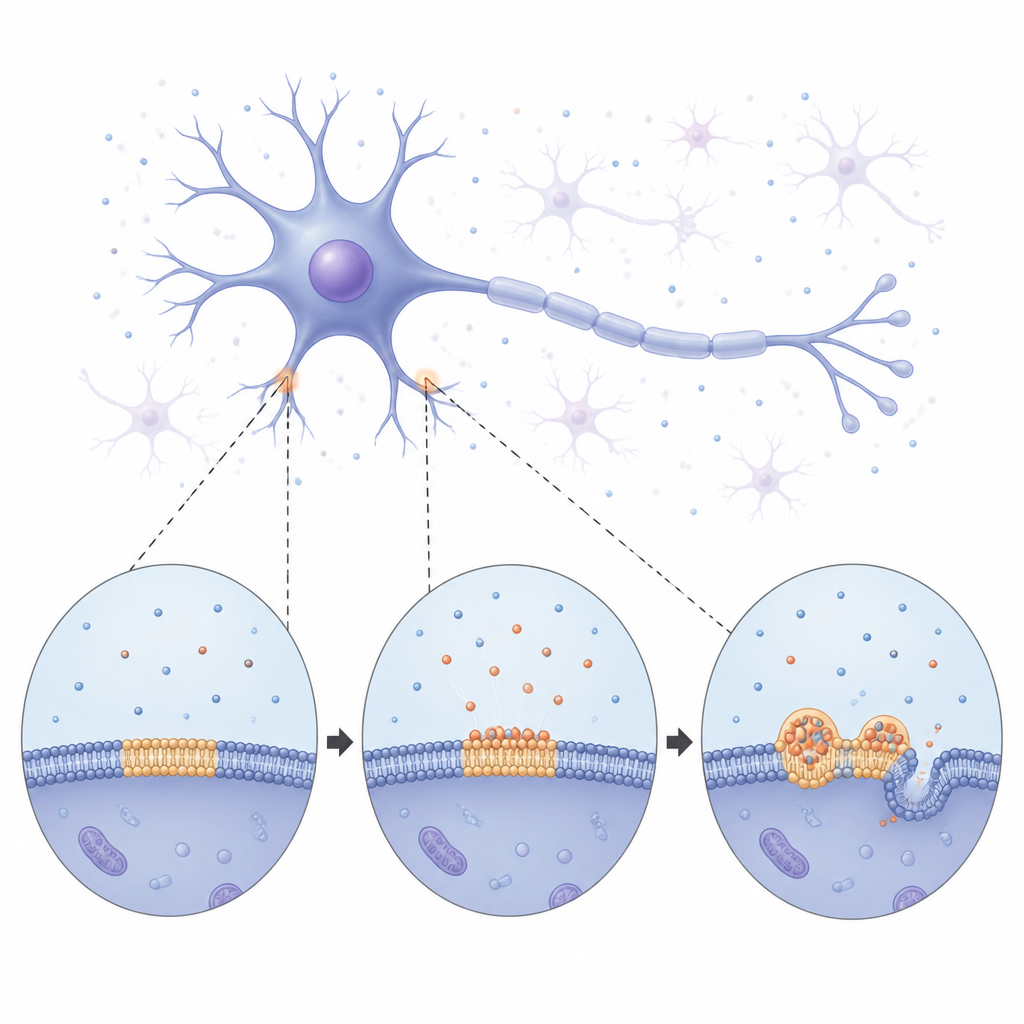
Des gouttelettes molles aux fibres rigides
Grâce à des observations à long terme, l’équipe a vu l’alpha-synucléine enrober lentement la membrane puis se fragmenter en condensats ronds et brillants répartis à la surface. Au départ, ces gouttelettes se comportaient comme de minuscules blobs liquides : elles fusionnaient entre elles et croissaient en drainant lentement de la matière de leurs plus petits voisins. Avec le temps, cependant, les gouttelettes devenaient plus rigides. Des mesures de la récupération des signaux fluorescents à l’intérieur d’elles montraient que la protéine et les lipides environnants bougeaient de moins en moins, indiquant une transition d’un état fluide vers un état plus solide. Finalement, de fines structures filamenteuses ont commencé à germer des gouttelettes, pliant et tubulant la membrane sous-jacente. Ces observations suggèrent que les gouttelettes liées à la membrane servent de zones liquides temporaires où l’alpha-synucléine peut se réorganiser avant de se figer en fibres solides associées à la maladie.
Comment la membrane elle-même est modifiée
L’étude s’est aussi intéressée à l’effet de l’alpha-synucléine sur la membrane pendant ce processus. Des expériences sur des membranes modèles ont montré que lorsque la protéine s’insère dans la surface, elle rend la couche lipidique plus compactée et moins compressible, modifiant sa tension et sa courbure. De grosses vésicules synthétiques aspirées dans des micropipettes se sont relâchées et ont glissé hors de l’aspiration dès l’ajout d’alpha-synucléine, révélant une chute rapide de la tension membranaire et des changements de forme. Sur plusieurs heures, l’adhérence de la protéine à la membrane s’est renforcée. Ces modifications mécaniques créent à l’interface un environnement plus rigide et plus ordonné, ce qui favorise à son tour un davantage d’encombrement protéique et de contacts stables, alimentant la croissance des gouttelettes et la formation ultérieure de fibrilles.
Le rôle caché de la charge électrique de surface
Pour expliquer pourquoi seuls certains mélanges lipidiques déclenchaient la condensation, les chercheurs ont mesuré le potentiel électrique à la surface membranaire. Ils ont constaté que la liaison de l’alpha-synucléine n’avait lieu que dans une fenêtre étroite de charge de surface négative, et que la condensation robuste apparaissait près d’une valeur seuil dans cette plage. Des simulations informatiques ont confirmé ces résultats, montrant qu’une membrane attractive peut provoquer une transition de type « pré-mouillage » : une couche épaisse riche en protéine se forme à la surface même lorsque la solution en volume est trop diluée pour se séparer en phases par elle-même. Dans des cellules vivantes, l’équipe a modifié ce potentiel interfacial de deux façons. L’ajout de lipides supplémentaires chargés négativement à des cellules hippocampiques en culture a modifié le potentiel et réduit des poncta d’alpha-synucléine préexistants, tandis que la dépolarisation de neurones primaires par du potassium élevé ou du glutamate a augmenté le nombre et la libération de gouttelettes d’alpha-synucléine. Cela relie l’activité électrique quotidienne des neurones directement à la façon et au lieu où la protéine se condense.
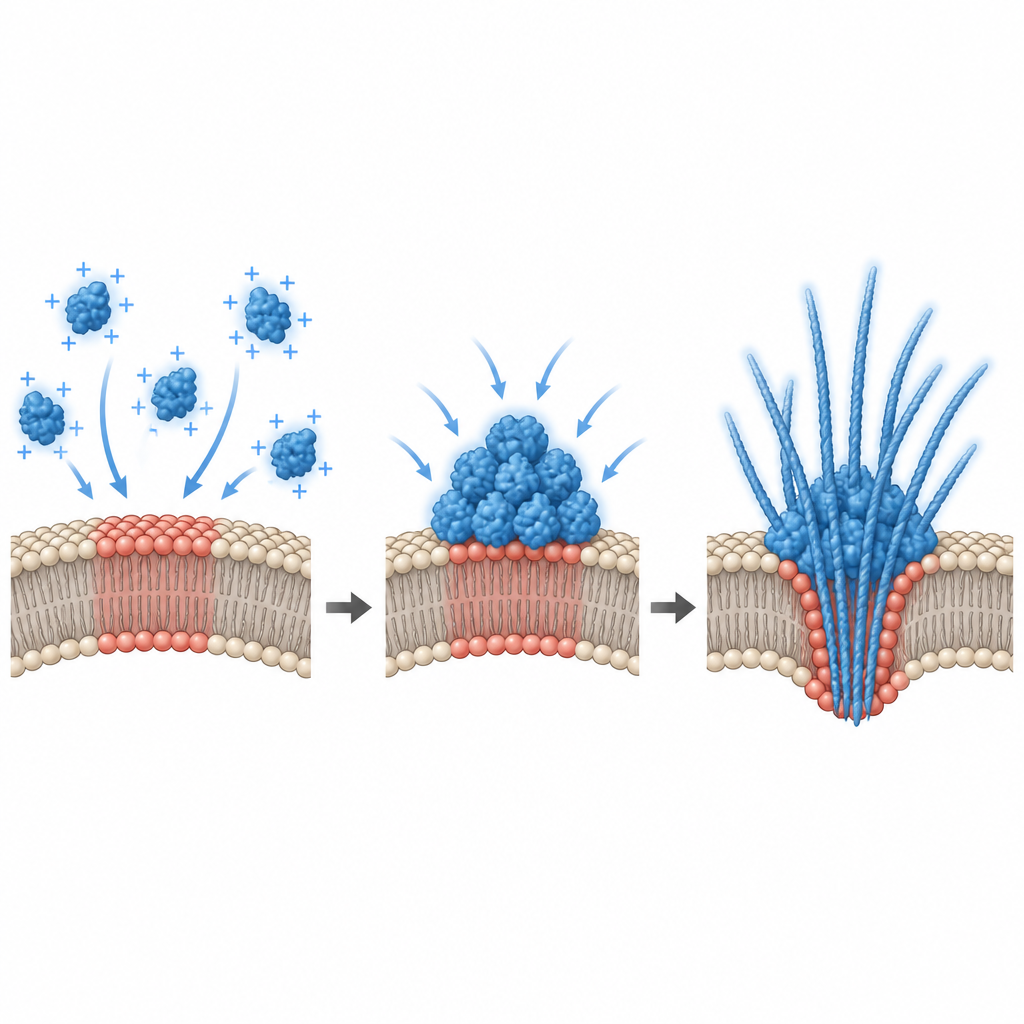
Ce que cela signifie pour les maladies neurodégénératives
Pris ensemble, ces résultats dressent le portrait de zones membranaires spécifiques sur les neurones agissant comme des lignes d’assemblage silencieuses pour des gouttelettes d’alpha-synucléine à des niveaux de protéine proches de ceux observés dans un cerveau sain. De légers changements dans la composition lipidique ou l’état électrique peuvent basculer ces surfaces dans un régime où la condensation se produit, les gouttelettes se rigidifient et des fibrilles émergent, déformant et parfois rompant la membrane tout en libérant des agrégats protéiques à l’extérieur de la cellule. Cette voie, pilotée par la membrane, offre une route plausible pour la propagation de l’alpha-synucléine de neurone à neurone lors de la neurodégénérescence, et suggère que moduler la composition membranaire ou le potentiel de surface pourrait un jour aider à contrôler la condensation protéique nocive à ses stades les plus précoces.
Citation: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
Mots-clés: alpha synuclein, maladie de Parkinson, membranes neuronales, condensation des protéines, composition des lipides