Clear Sky Science · pl
Potencjał interfejsu błonowego reguluje kondensację powierzchniową i fibrylację α-synukleiny w neuronach
Dlaczego to ma znaczenie dla zdrowia mózgu
Choroba Parkinsona i pokrewne zaburzenia charakteryzują się skupiskami białka zwanego alfa-synukleiną wewnątrz komórek mózgowych, lecz to, jak te skupiska powstają i rozprzestrzeniają się z komórki na komórkę, pozostawało zagadką. Badanie pokazuje, że zewnętrzna „skóra” komórek nerwowych — ich błony — może cicho gromadzić alfa-synukleinę w maleńkich kropelkach przy bardzo niskich poziomach białka, a te kropelki mogą utwardzać się w uszkadzające włókna, które deformują, a nawet rozpierają błonę. Poznanie tego ukrytego miejsca na powierzchni komórki daje nową perspektywę na to, jak szkodliwe agregaty białek powstają, rosną i przemieszczają się po mózgu.
Jak „skóra” neuronu może przyciągać rozproszone białka
Autorzy skupili się na cienkiej, tłuszczowej warstwie otaczającej komórki, złożonej z mieszaniny różnych lipidów. Stwierdzili, że alfa-synukleina, która zwykle swobodnie krąży wewnątrz neuronów, może być przyciągana do tej błony i tworzyć tam gęste kropelki, nawet gdy jej całkowite stężenie jest ekstremalnie niskie. Co istotne, działo się to tylko wtedy, gdy błona zawierała konkretną mieszankę dwóch powszechnych lipidów — jednego obojętnego i jednego ujemnie naładowanego — w stosunku 6:4. Ten specyficzny układ tworzy odpowiednie warunki elektryczne na powierzchni błony, które przyciągają i utrzymują alfa-synukleinę. Gdy warunki nie były spełnione lub gdy te same lipidy występowały jako wolne cząstki zamiast ciągłej powierzchni, białko nie kondensowało w kropelki.
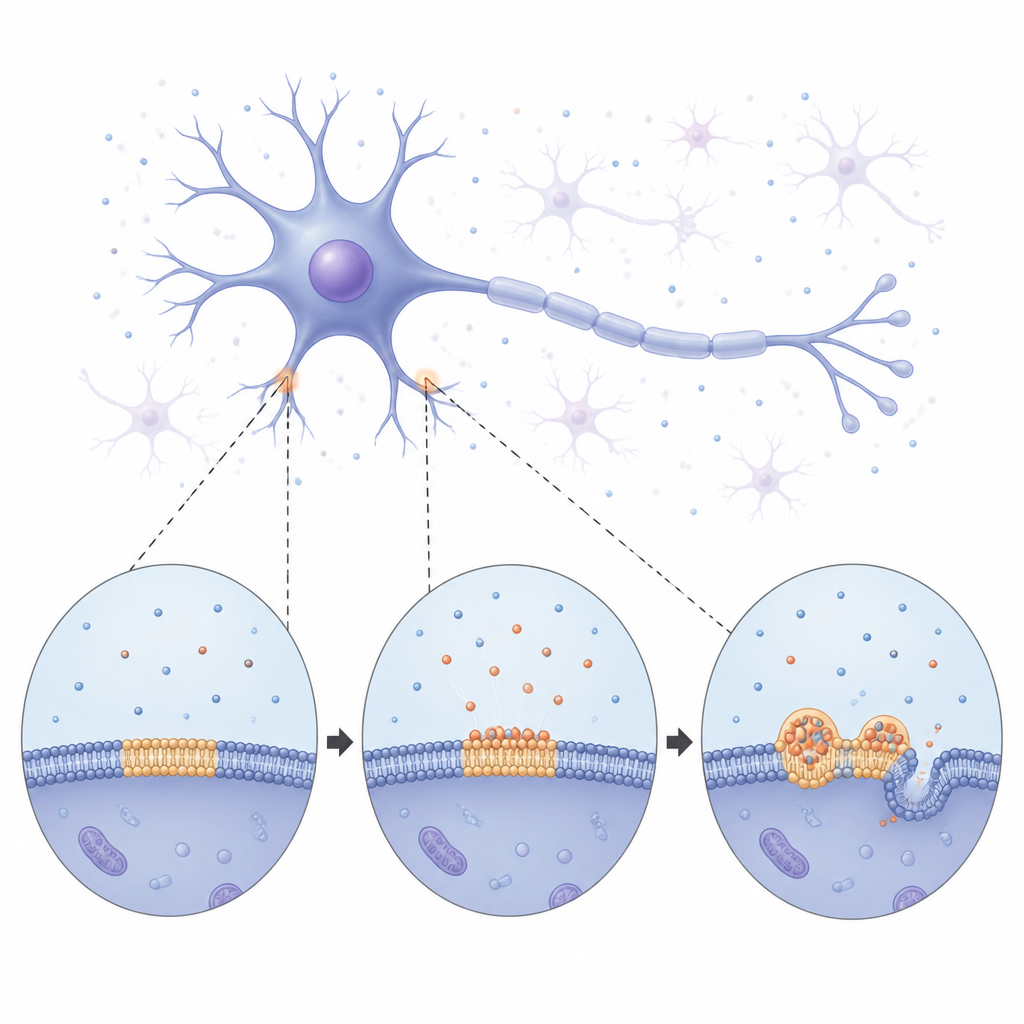
Od miękkich kropelek do sztywnych włókien
Wykorzystując długoterminowe obrazowanie, zespół obserwował, jak alfa-synukleina powoli pokrywa błonę, a następnie rozpada się na jasne, okrągłe kondensaty rozproszone po powierzchni. Początkowo te kropelki zachowywały się jak maleńkie płynne krople: łączyły się ze sobą i rosły przez powolne odpływanie materiału z mniejszych sąsiadów. Z czasem jednak kropelki stawały się coraz bardziej sztywne. Pomiary odzyskiwania sygnału fluorescencyjnego wewnątrz nich wykazały, że zarówno białko, jak i otaczające lipidy poruszały się coraz mniej, co sygnalizowało przejście ze stanu płynnego do bardziej stałego. W końcu z kropelek zaczęły wyrastać cienkie struktury przypominające włókna, wyginając i tworząc kanaliki w leżącej poniżej błonie. Obserwacje te sugerują, że krople związane z błoną funkcjonują jako tymczasowe, płynne strefy, w których alfa-synukleina może się reorganizować, zanim zablokuje się w stałe włókna powiązane z chorobą.
Jak zmienia się sama błona
Badanie pytało też, co alfa-synukleina robi z błoną w trakcie tych procesów. Eksperymenty na modelowych błonach wykazały, że gdy białko wnika w powierzchnię, powoduje ściślejsze pakowanie warstwy lipidowej i obniżenie jej ściśliwości, zmieniając napięcie i krzywiznę. Olbrzymie syntetyczne pęcherzyki aspirujące do mikropipet rozluźniały się i wysuwały z nich po dodaniu alfa-synukleiny, ujawniając szybki spadek napięcia błony i zmiany kształtu. W ciągu godzin przyczepność białka do błony wzmacniała się. Te mechaniczne przesunięcia tworzą bardziej sztywne, uporządkowane środowisko na interfejsie, co z kolei sprzyja dalszemu zagęszczaniu białka i stabilnym kontaktom, napędzając wzrost kropelek i ostateczne tworzenie włókien.
Ukryta rola ładunku powierzchniowego
Aby wyjaśnić, dlaczego tylko niektóre mieszanki lipidowe wywoływały kondensację, naukowcy zmierzyli potencjał elektryczny na powierzchni błony. Odkryli, że wiązanie alfa-synukleiny zachodziło tylko w wąskim zakresie ujemnego ładunku powierzchniowego, a silna kondensacja pojawiała się blisko wartości progowej w tym zakresie. Symulacje komputerowe potwierdziły te wyniki, pokazując, że atrakcyjna błona może wywołać przejście „przypominające pre-wetting”: na powierzchni tworzy się gruba warstwa bogata w białko nawet wtedy, gdy roztwór bulkowy jest zbyt rozcieńczony, by samodzielnie przejść w fazę oddzielną. W żywych komórkach zespół zmieniał ten potencjał interfejsu na dwa sposoby. Dodanie dodatkowych ujemnie naładowanych lipidów do hodowanych komórek hipokampa zmieniło potencjał i zmniejszyło istniejące punkty alfa-synukleiny, podczas gdy depolaryzacja neuronów pierwotnych za pomocą wysokiego stężenia potasu lub glutaminianu zwiększała liczbę i uwalnianie kropelek alfa-synukleiny. To łączy codzienną aktywność elektryczną neuronów bezpośrednio z tym, jak i gdzie białko kondensuje.
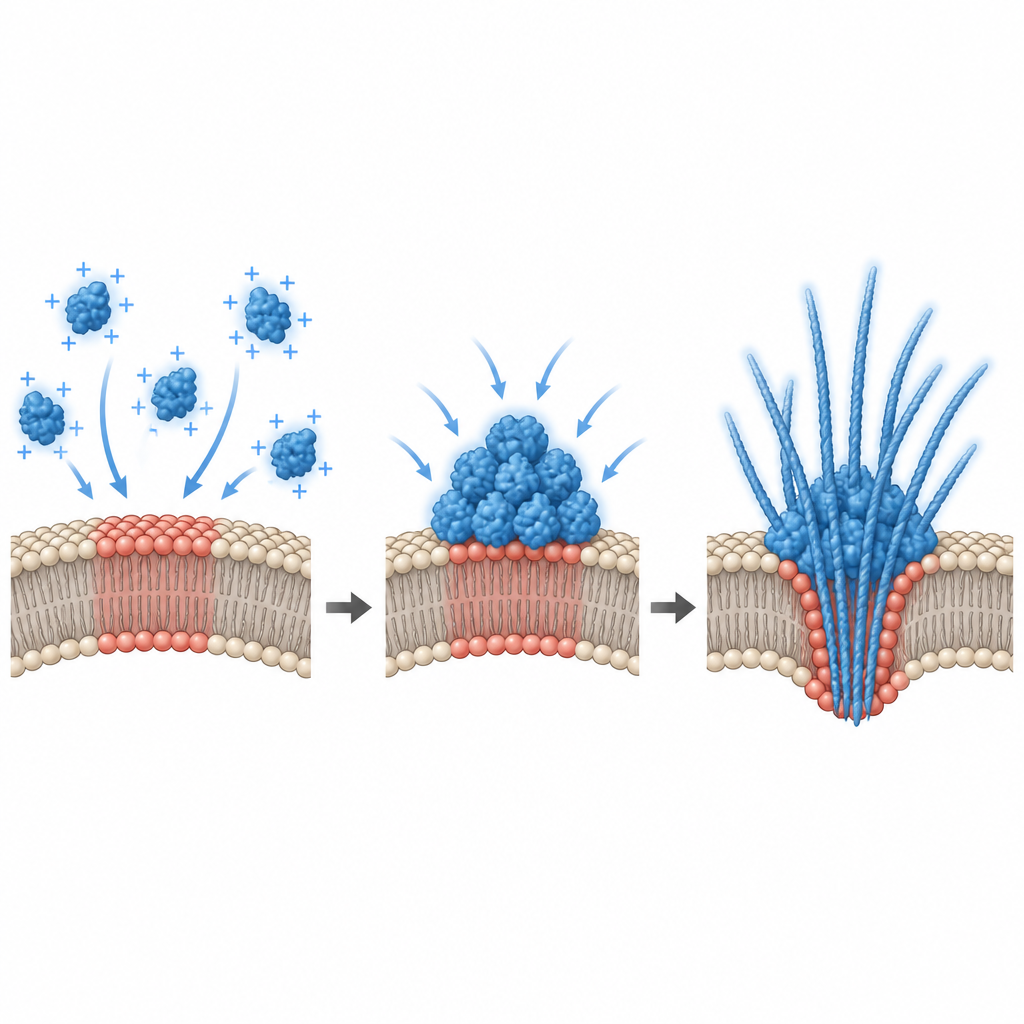
Co to oznacza dla chorób neurodegeneracyjnych
Razem te odkrycia kreślą obraz, w którym określone fragmenty błon neuronów działają jak ciche linie montażowe dla kropelek alfa-synukleiny przy poziomach białka zbliżonych do tych występujących w zdrowym mózgu. Niewielkie zmiany w składzie lipidów lub stanie elektrycznym mogą przesunąć te powierzchnie w rejony, gdzie zachodzi kondensacja, kropelki twardnieją, a włókna powstają, deformując i czasem rozrywając błonę oraz uwalniając agregaty białkowe poza komórkę. Ta droga napędzana przez błonę stanowi wiarygodny mechanizm, dzięki któremu alfa-synukleina może rozprzestrzeniać się z neuronu na neuron podczas neurodegeneracji, i sugeruje, że modulacja składu błony lub potencjału powierzchniowego mogłaby w przyszłości pomóc kontrolować szkodliwą kondensację białek na jej najwcześniejszych etapach.
Cytowanie: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
Słowa kluczowe: alfa-synukleina, choroba Parkinsona, błony neuronalne, kondensacja białek, skład lipidów