Clear Sky Science · he
הפוטנציאל הבין־ממברנלי שולט בעיבוי פני השטח וביצירת פיברילות של α‑סינוקלאין בתאים עצביים
מדוע זה חשוב לבריאות המוח
מחלת פרקינסון ומחלות נלוות מתאפיינות בגושים של חלבון הנקרא α‑סינוקלאין בתוך תאי מוח, אך כיצד גושים אלה מופיעים ומדביקים תאים נוספים נשאר חידה. מחקר זה מראה שמעטפת התאים העצביים — הממברנה — יכולה בשקט לרכז α‑סינוקלאין לטיפות זעירות גם בריכוזים נמוכים מאוד של החלבון, ושהטיפות הללו עלולות להתמצק לסיבים מזיקים המעוותים ואף מקריעים את הממברנה. הבנה של הבמה הסמויה הזו על פני התא מציעה פרספקטיבה חדשה על האופן שבו גושי חלבון מזיקים מתחילים, צומחים ומתקדמים במוח.
כיצד עור התא העיצבי יכול לרכז חלבונים חופשיים
המחברים התמקדו בשכבה השומנית הדקה העוטפת את התאים, שמורכבת מתערובת של ליפידים שונים. הם מצאו ש‑α‑סינוקלאין, שלרוב צף חופשי בתוך הנוירונים, יכול להימשך לממברנה ולהתאגד שם לטיפות צפופות, גם כאשר ריכוזו הכולל נמוך מאוד. באופן מפתיע, זה התרחש רק כשהממברנה הכילה תערובת מסוימת של שני ליפידים נפוצים, אחד ניטרלי ואחד שלילי, ביחס של 6:4. התערובת הספציפית הזו יוצרת את התנאים החשמליים המתאימים על פני השטח של הממברנה כדי למשוך ולהחזיק את α‑סינוקלאין. כאשר התנאים הללו לא התקיימו, או כאשר אותם ליפידים התקיימו כחלקיקים חופשיים במקום כמשטח רציף, החלבון לא התעבה לטיפות.
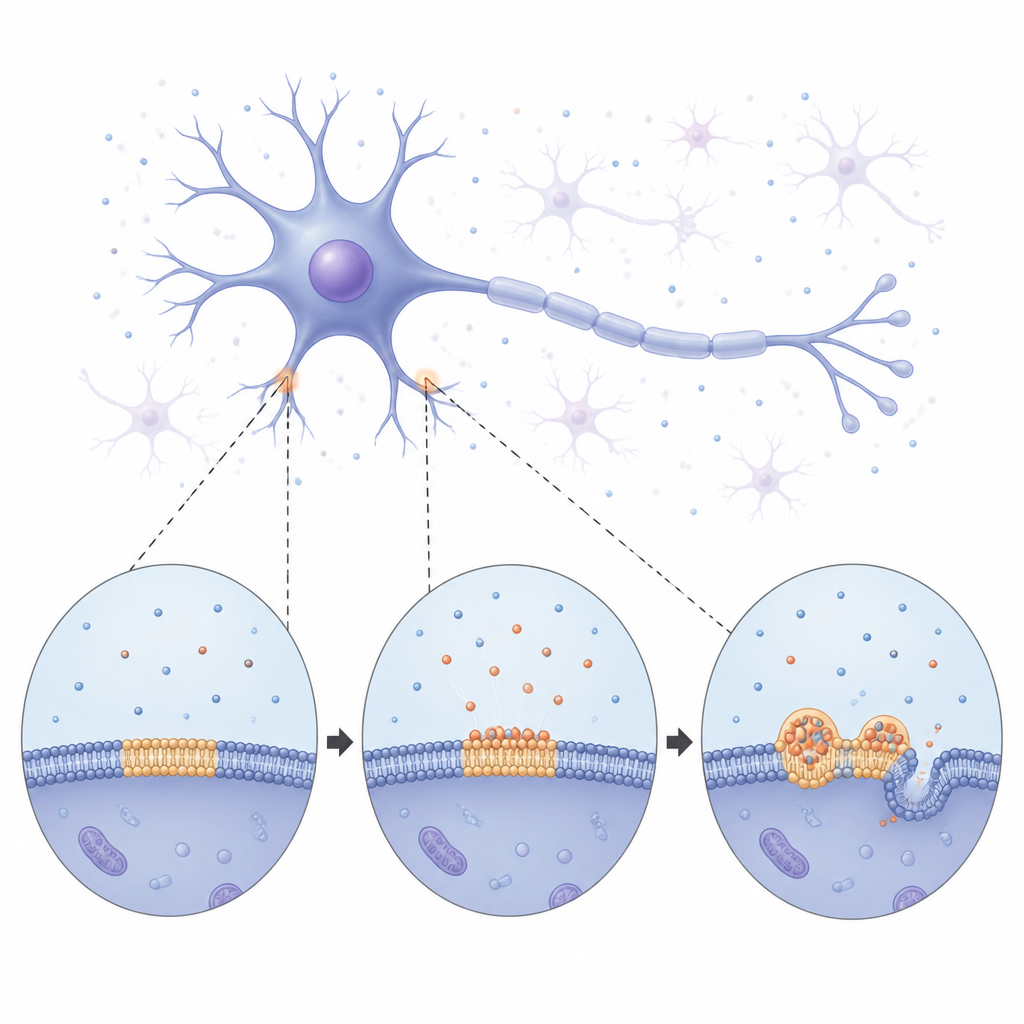
מטריות רכות לפיברילים קשיחים
באמצעות הדמיה ארוכת טווח, הצוות עקב אחרי ציפוי אטי של הממברנה ב‑α‑סינוקלאין ולאחר מכן פירוקה לקונדנסנטים עגולים ובהירים הפזורים על המשטח. בתחילה הטיפות התנהגו ככתמים נוזליים זעירים: הן התמזגו זו עם זו וגודלו על ידי ניקוז איטי של חומר משכנים קטנים יותר. עם הזמן, לעומת זאת, הטיפות הפכו לקשיחות יותר. מדידות של החלמה של איתותים פלואורסצנטיים בתוכן הראו שגם החלבון וגם הליפידים הסמוכים נעו פחות ויותר, מה שמעיד על מעבר ממצב נוזלי למצב מוצק יותר. בסופו של דבר החלו להופיע מהטיפות מבנים דמויי סיבים דקים, שעיקמו וחיזקו את הממברנה התחתית וגרמו להיצרות ויצירת צינוריות. תצפיות אלה מרמזות שהטיפות הקשורות לממברנה פועלות כבמות זמניות נוזליות שבהן α‑סינוקלאין יכול להתארגן לפני שננעל למצב הסיבי המוצק המקושר למחלה.
כיצד הממברנה עצמה משתנה
המחקר גם בדק מה α‑סינוקלאין עושה לממברנה בזמן שהתהליכים האלה מתרחשים. ניסויים עם ממברנות מודל הראו שכאשר החלבון משתלב במשטח, הוא מייצר דחיסה רבה יותר של שכבת הליפידים ופחות דחיסות דחיסה, ומשנה את המתיחות והעקמומיות שלה. וניקולות סינתטיות ענקיות שנשאבו למיקרו‑מַחטות התרככו וגלשו ברגע שנוסף α‑סינוקלאין, מה שגילה ירידה מהירה במתיחות הממברנה ושינויים בצורתה. לאורך שעות, אחיזת החלבון על הממברנה התהדקה. הזעזועים המכניים האלה יוצרים סביבה קשיחה ומסודרת יותר בממשק, שמקדמת הצטופפות חלבונים ומגעים יציבים יותר, וכך מזינה גדילת טיפות נוספת ולבסוף היווצרות פיברילים.
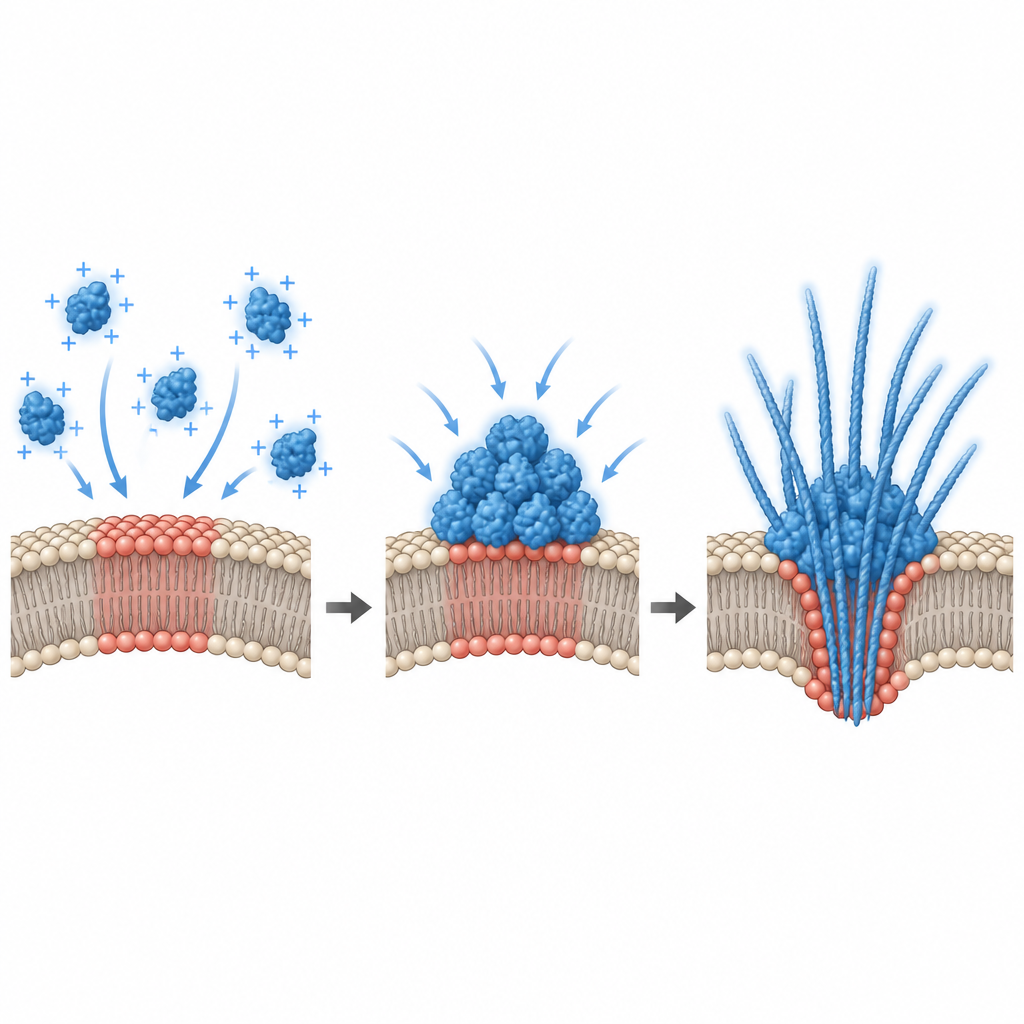
התפקיד הסמוי של מטען חשמלי פני השטח
כדי להסביר מדוע רק תערובות ליפידיות מסוימות עוררו עיבוי, החוקרים מדדו את הפוטנציאל החשמלי על פני הממברנה. הם גילו שקשירת α‑סינוקלאין התרחשה רק בתוך חלון צר של מטען פני שטח שלילי, ועיבוי חזק הופיע בקרבת ערך סף בטווח זה. סימולציות מחשב תמכו בממצא, והראו שממברנה אטרקטיבית יכולה לגרום למעבר בסגנון "טרום‑רטוב": שכבה עבה העשירה בחלבון נוצרת על פני השטח גם כאשר התמיסה הסמוכה מדוללת מדי כדי להפריד פאזה מעצמה. בתאים חיים, הצוות שינה את הפוטנציאל הבין‑ממברי בשתי דרכים. הוספת ליפידים טעונים שלילית לתאים היפוקמפליים בתרבית שינתה את הפוטנציאל וקימטה נקודות קיימות של α‑סינוקלאין, בעוד דפלוריזציה של נוירונים ראשוניים בעזרת אשלגן גבוה או גלוטמט הגדילה את מספר והפרשת טיפות α‑סינוקלאין. זה מקשר באופן ישיר בין הפעילות החשמלית היומיומית של נוירונים לאופן ולמקום שבו החלבון מתעבה.
מה משמעות הדבר למחלת עצבים ניוונית
ביחד, הממצאים מציירים תמונה שבה כתמי ממברנה ספציפיים על נוירונים פועלים כמסלקות הרכבה שקטות של טיפות α‑סינוקלאין ברמות חלבון הקרובות לאלו שבמוח הבריא. שינויים קלים בהרכב הליפידים או במצב החשמלי יכולים להזיז משטחים אלה לאזור שבו מתרחש עיבוי, הטיפות מתמצקות והפיברילים מופיעים, מעקמים ולפעמים מקרעים את הממברנה ומשחררים אגגרגטים של חלבון מחוץ לתא. נתיב המונע על‑ידי ממברנה זה מספק מסלול סביר לפיזור של α‑סינוקלאין מתא עצב אחד לאחר במהלך ניו‑דגנרציה, ומציע שאיזון הרכב הממברנה או פוטנציאל פני השטח עשוי יום אחד לסייע לשלוט בעיבוי חלבון מזיק בשלבים המוקדמים ביותר.
ציטוט: Shaikh, J., Nagarajan, A., Mitra, T. et al. Membrane interfacial potential governs surface condensation and fibrillation of α-Synuclein in neurons. Nat Commun 17, 4247 (2026). https://doi.org/10.1038/s41467-026-70840-2
מילות מפתח: α‑סינוקלאין, מחלת פרקינסון, ממברנות עצביות, עיבוי חלבון, הרכב ליפידי