Clear Sky Science · zh
用于联合分析单细胞RNA和T细胞受体测序数据的多模态框架可预测T细胞对癌症免疫疗法的反应
为何预测免疫反应很重要
癌症免疫疗法,例如检查点抑制剂,通过释放患者自身的T细胞去攻击肿瘤发挥作用。然而只有部分患者能获益,医生目前在预测谁会应答方面工具有限。本研究提出了一个称为TRIM的计算框架,它从血液和肿瘤中对T细胞进行的详尽单细胞测量中学习。通过将每个细胞的基因活性信息与其独特的T细胞受体信息结合,TRIM能够预测治疗后T细胞的扩增与状态变化,从而提供一种可能仅凭常规血液样本就能预见治疗成效的方法。
窥探单个T细胞内部
T细胞在体内巡逻,通过其T细胞受体识别特定的分子片段以寻找危险信号。当T细胞遇到癌细胞时,它可以扩增为大量近乎相同的克隆,并承担不同角色,从活跃的肿瘤杀伤者到无法有效作战的衰竭细胞。现代单细胞技术现在可以同时读取每个T细胞的基因表达谱(哪些基因被开启或关闭)和其受体序列。作者在来自头颈部、结直肠及其他几种癌症患者的数千个T细胞上应用了这些工具,采集了治疗前后来自血液和肿瘤组织的样本。
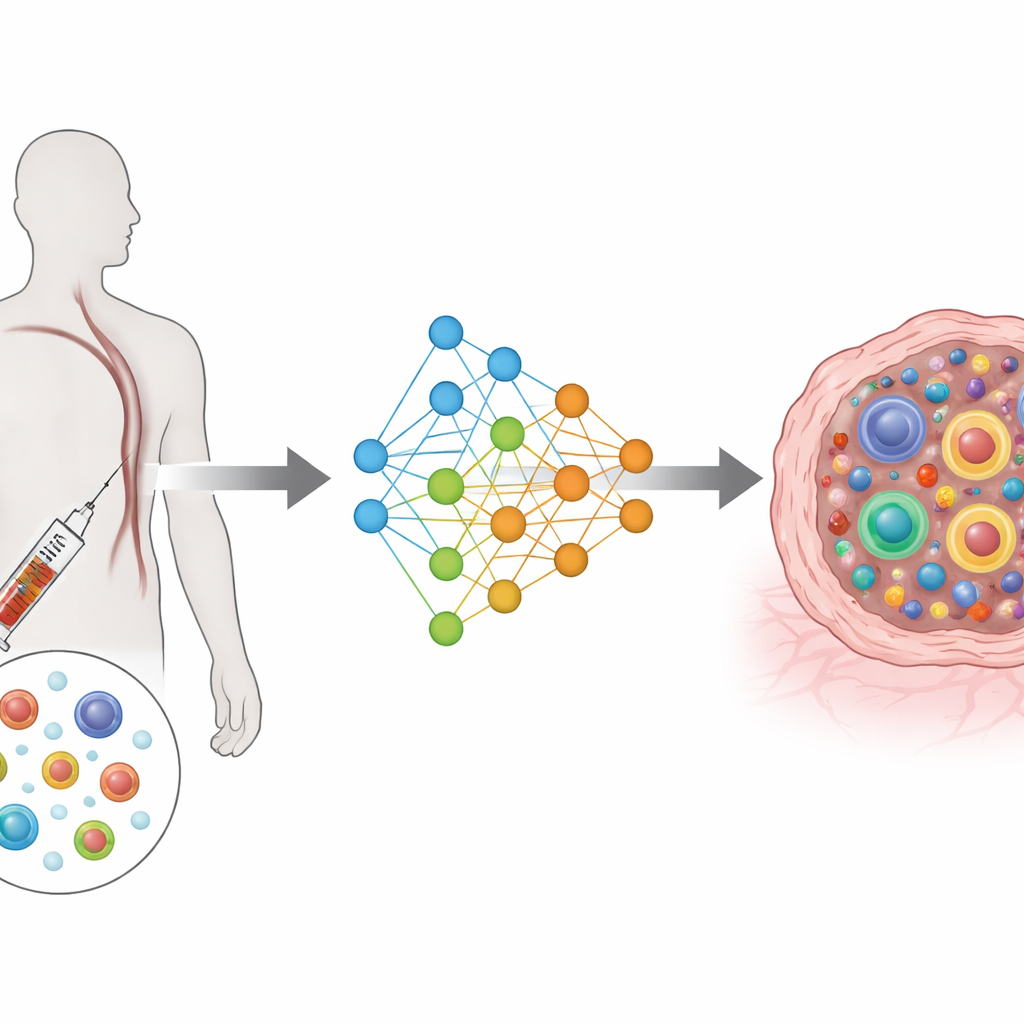
从复杂测量到共享地图
TRIM基于一种被称为条件变分自编码器的深度学习架构。简单来说,它将来自每个细胞的丰富基因和受体信息压缩到一个共享的低维地图中,同时考虑患者身份、细胞来源(血液或肿瘤)以及采样时间(治疗前或治疗后)。独立的输入模块读取基因活动和受体特征,独立的输出模块尝试重构这些信息。一个特殊的损失函数促使属于同一克隆的细胞在该地图上彼此靠近,同时将不同克隆分开。这一设计使模型聚焦于生物学上最重要的方面:每个克隆的大小以及其细胞在功能状态间的分布。
受体、基因活性与克隆之间的联系
通过在多个数据集上系统比较受体相似性和基因表达,研究者发现共享完全相同受体的细胞在基因活性上确实比随机T细胞更为相似,尤其是在大规模扩增的克隆中。然而,超出完全匹配之外,受体序列的微小差异并不能可靠地反映两细胞在基因表达上的相似程度。换言之,受体几乎相同的细胞在表型上可能与受体完全无关的细胞一样不同。这使研究团队将注意力集中在克隆身份和克隆大小上,而不是精细的受体序列相似性,作为受体信息与细胞状态之间的关键桥梁。
从血液预测肿瘤内T细胞
对TRIM的核心测试是:它是否仅基于患者治疗前的血液数据,就能为该患者预测治疗后肿瘤和血液中T细胞的真实情况。作者采用留一法训练TRIM——对除一名患者外的所有患者进行训练,然后预测被留出的患者,并在各个队列中重复这一过程。他们展示了模型能准确捕捉不同条件下T细胞基因状态和克隆多样性的整体景观。更显著的是,对于治疗前存在的单个受体克隆,TRIM能够高度准确地预测哪些克隆将在治疗后扩增,明显优于常规的机器学习方法。它还复现了已知的成功应答特征,例如活化且增殖的CD8 T细胞增加以及与有效肿瘤杀伤相关的特定基因程序。
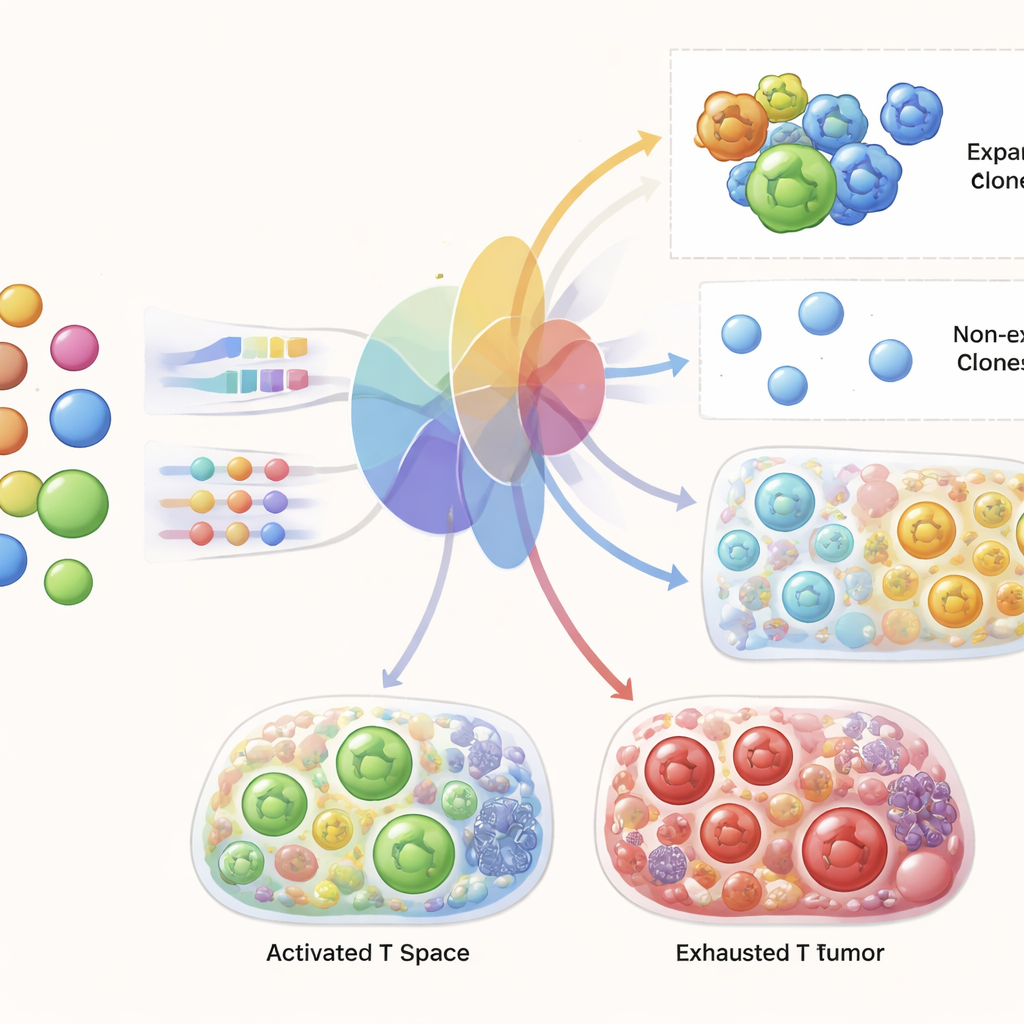
揭示成功扩增背后的基因
由于TRIM在内部需要判定哪些细胞可能扩增,作者得以探查模型所依赖的基因。TRIM标记的基因与T细胞激活的核心特征一致:控制增殖的细胞周期调控因子、参与靶细胞杀伤的分子、调节激活与细胞间通信的蛋白质,以及帮助T细胞迁移进入并在肿瘤内发挥功能的代谢与迁移相关因子。重要的是,模型在预测时仅使用治疗前的血液数据就识别出这些程序,表明循环T细胞中早期的分子差异能预示它们在接受治疗并遭遇肿瘤信号后将如何应答。
对患者的意义
本质上,这项工作表明,经过精心设计的模型可以从多模态单细胞数据中学习,以预测患者在癌症免疫疗法过程中T细胞的行为。TRIM使用治疗前的血样来推断哪些克隆会扩增、它们将进入何种状态以及哪些基因程序会驱动这种行为,甚至在那些难以直接取样的组织中也是如此。尽管在临床应用之前仍需进一步验证和更大的数据集,但这一方法指向了这样的未来:肿瘤科医生或许能借助简单的血液检测,配合像TRIM这样的模型,来预测治疗反应、监测病情进展并发现指导个体化免疫治疗决策的新生物标志物。
引用: He, C., Amodio, M., Ashenberg, O. et al. Multimodal framework for the joint analysis of single-cell RNA and T cell receptor sequencing data predicts T cell response to cancer immunotherapy. Nat Commun 17, 3840 (2026). https://doi.org/10.1038/s41467-026-70505-0
关键词: 癌症免疫疗法, T细胞, 单细胞测序, 机器学习模型, 肿瘤生物标志物