Clear Sky Science · he
מסגרת מולטימודלית לניתוח משותף של רצף RNA בתא יחיד ורצף קולטני T מנבאת את תגובת תאי ה-T לאימונותרפיה של סרטן
מדוע חיזוי תגובה חיסונית חשוב
אימונותרפיות לסרטן, כגון מעכבי נקודות בקרה, פועלות על ידי שחרור תאי ה-T של המטופל להתקפה על הגידולים. עם זאת רק חלק מהמטופלים נהנים מהטיפול, והרופאים כיום מצוידים בכלים מוגבלים כדי לחזות מי יגיב. מחקר זה מציג מסגרת חישובית בשם TRIM שלומדת ממדידות מפורטות בתא יחיד של תאי T בדם ובגידול. על ידי שילוב מידע על פעילות הגנים של כל תא ועל רצף קולטני ה-T הייחודי שלו, TRIM יכולה לנבא כיצד תאי ה-T יתרחבו וישתנו לאחר הטיפול, ומציעה דרך אפשרית לצפות בהצלחת הטיפול מתוך דגימת דם שגרתית.
מסתכלים בתוך תאי T בודדים
תאי T סורקים את הגוף ומחפשים סימני סכנה באמצעות קולטני ה-T שלהם, המזהים שברי מולקולות מסוימים. כאשר תא T פוגש סרטן, הוא יכול להתחלק לקבוצה של שכפולים—קלון—שכוללים תאים כמעט זהים ולהנחות תפקידים שונים, מטורפים פעילים של הגידול ועד תאים מותשים שאינם מסוגלים להילחם ביעילות. טכנולוגיות מודרניות בתא יחיד מסוגלות כיום לקרוא, עבור כל תא T, גם את פרופיל הביטוי הגנטי שלו (אילו גנים פעילים או כבויים) וגם את רצף הקולטן שלו. המחברים יישמו את הכלים הללו על אלפי תאי T ממטופלים עם סרטן הראש והצוואר, סרטן המעי הגס ומספר סוגי סרטן נוספים, ודגמו הן דם והן רקמת גידול לפני ואחרי אימונותרפיה.
ממדידות מורכבות למפה משותפת
TRIM בנויה על סוג של ארכיטקטורת למידת עומק הידועה כאוטואינקודר ואריאציונלי מותנה (conditional variational autoencoder). בפשטות, היא מכווצת את המידע העשיר על גני התא ועל הקולטן למפה משותפת ובממד נמוך, תוך התחשבות גם במיהו המטופל, מאיפה התא נלקח (דם או גידול) ומתי נאסף (לפני או אחרי הטיפול). מודולים קלט נפרדים קוראים את פעילויות הגנים ואת מאפייני הקולטן, ומודולי פלט נפרדים מנסים לשחזר אותם. פונקציית אובדן מיוחדת דוחפת תאים ששייכים לאותו קלון לשבת זה לצד זה במפה, בעוד שמרחיקה קלונות שונות זה מזה. עיצוב זה ממקד את המודל במה שחשוב ביולוגית: גודל כל קלון וכיצד תאים שלו מתפלגים בין מצבים פונקציונליים.
מה מקשר בין קולטן, פעילות גנים וקלונות
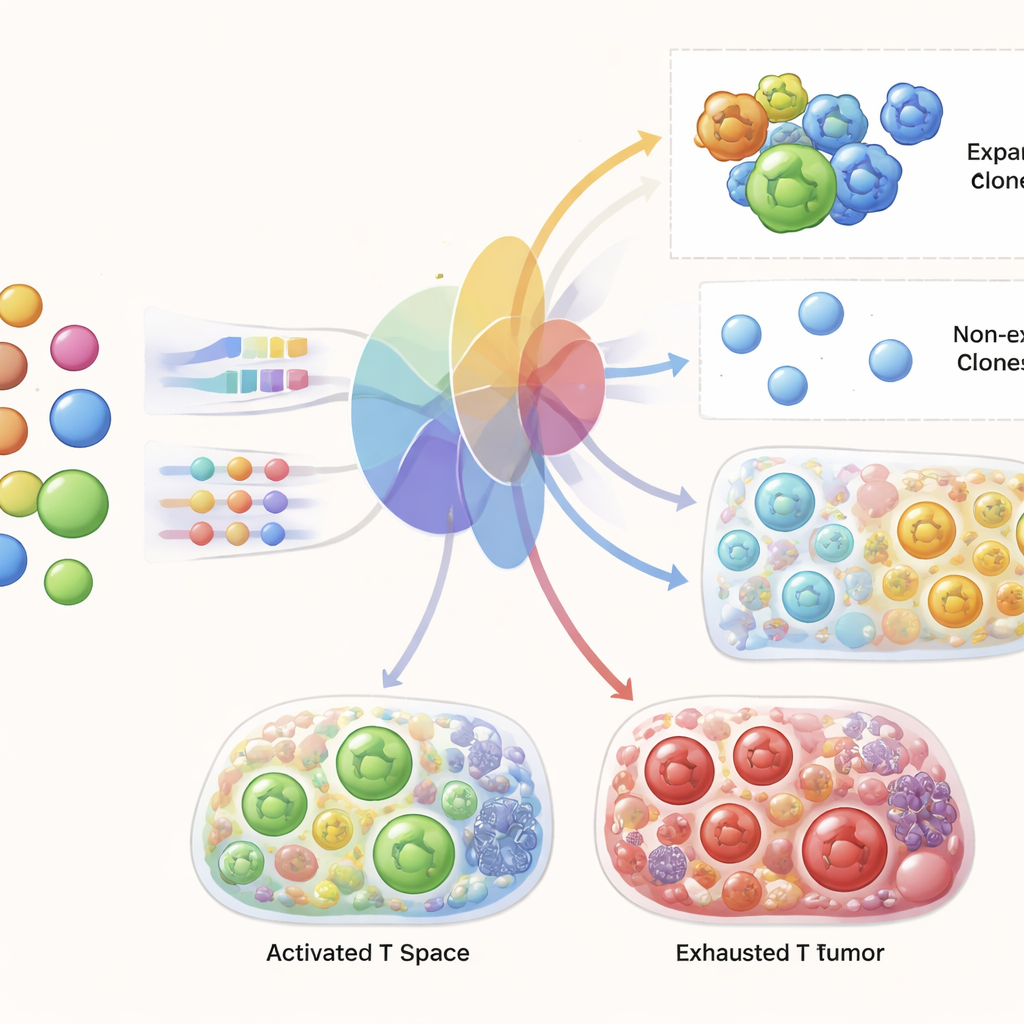
בהשוואה שיטתית בין דמיון הרצפטור וביטוי הגנים על פני מערכי נתונים מרובים, החוקרים מצאו שתאים שמשתפים בדיוק את אותו קולטן הם אכן דומים יותר בפעילות הגנטית שלהם לעומת תאי T אקראיים, במיוחד בקלונות גדולים ומורחבים. עם זאת, מעבר להתאמות מדויקות, שינויים קטנים ברצף הקולטן אינם עוקבים באופן מהימן אחרי מידת הדמיון בביטוי הגנים בין שני תאים. במילים אחרות, תאים עם קולטן כמעט זהה יכולים להיראות שונים בדיוק כמו תאים עם קולטן שאין ביניהם קשר. ממצא זה הוביל את הצוות להתמקד בזהות הקלון וגודל הקלון, ולא בדמיון רצף מדויק של הקולטן, כגשר מרכזי בין מידע הקולטן למצב התא.
חיזוי תאי T קשורים לגידול מתוך הדם
המבחן המרכזי ל-TRIM היה האם היא יכולה לקחת רק נתוני דם מהמטופל שנלקחו לפני הטיפול ולייצר תחזיות מציאותיות לתאי ה-T של אותו מטופל ברקמת הגידול ובדם לאחר הטיפול. המחברים אימנו את TRIM על כל המטופלים פרט לאחד, ואז ביקשו ממנה לחזות את המטופל שלא נכלל באימון, וחזרו על כך על פני קבוצות שונות. הם הראו שהמודל לתפוס במדויק את הנוף הכולל של מצבי ביטוי הגנים ומגוון הקלונות של תאי ה-T בתנאים השונים. באופן בולט יותר, עבור קלונות רצפטור בודדים שנמצאו לפני הטיפול, TRIM יכל לחזות אילו מהם יתרחבו לאחר הטיפול בדיוק גבוה, ובכך עלה על גישות סטנדרטיות של למידת מכונה. היא גם שחזרה חתימות ידועות של תגובה מוצלחת, כגון עלייה בתאי CD8 פעילים ומתחלקים ותוכניות גנטיות ספציפיות המשויכות להרג אפקטיבי של הגידול.
חשיפת הגנים שמאחורי ההתרחבות המוצלחת
מכיוון ש-TRIM חייבת להחליט בתוך המודל אילו תאים סבירים שיתרחבו, החוקרים יכלו לבדוק אילו גנים המודל מתבסס עליהם. הגנים שנבחרו על ידי TRIM תואמים לתכונות מרכזיות של הפעלת תאי T: רגולטורים במחזור התא ששולטים על התפשטות, מולקולות המעורבות בהריגת תאים מטרה, חלבונים השולטים על הפעלה ותקשורת, וכן גורמים מטבוליים וקשורים לנדידה שעוזרים לתאי T לחדור לפעול בתוך הגידולים. חשוב לציין שהמודל זיהה תוכניות אלו באמצעות נתוני דם לפני הטיפול בלבד בזמן החיזוי, מה שמרמז כי הבדלים מולקולריים מוקדמים בתאי T שמסתובבים בדם מנבאים כיצד הם יגיבו כאשר הטיפול יתחיל והשורות יפגשו אותות הגידול.
מה משמעות הדבר עבור המטופלים
בעצם, עבודה זו מראה שמודל שעוצב בקפידה יכול ללמוד מנתונים מולטימודאליים של תא יחיד כדי לחזות כיצד תאי ה-T של מטופל יתנהגו במהלך אימונותרפיה לסרטן. TRIM משתמשת בדגימות דם שנלקחו לפני הטיפול כדי להסיק אילו קלונות יתרחבו, אילו מצבים יתפסו, ואילו תוכניות גנטיות יניעו התנהגות זו, גם ברקמות שקשה לדגום ישירות. בעוד שדרושה אימות נוסף ומערכי נתונים גדולים יותר לפני שימוש קליני, הגישה מצביעה על עתיד שבו אונקולוגים עשויים להשתמש בבדיקת דם פשוטה, בשילוב עם מודלים כמו TRIM, כדי לחזות תגובת טיפול, לנטר התקדמות המחלה ולגלות סמנים ביולוגיים חדשים שמנחים החלטות אימונותרפיה מותאמת אישית.
ציטוט: He, C., Amodio, M., Ashenberg, O. et al. Multimodal framework for the joint analysis of single-cell RNA and T cell receptor sequencing data predicts T cell response to cancer immunotherapy. Nat Commun 17, 3840 (2026). https://doi.org/10.1038/s41467-026-70505-0
מילות מפתח: אימונותרפיה של סרטן, תאי T, ריצוף תא יחיד, מודל למידת מכונה, סמנים ביולוגיים של גידול