Clear Sky Science · ru
Мультимодальная платформа для совместного анализа одно-клеточной РНК и секвенирования T-клеточных рецепторов предсказывает ответ T-клеток на противораковую иммунотерапию
Почему важно предсказывать иммунный ответ
Противораковые иммунотерапии, такие как ингибиторы контрольных точек, действуют, освобождая собственные T-клетки пациента для атаки опухолей. Однако лишь часть пациентов получает от этого пользу, и у врачей пока мало инструментов, чтобы заранее определить, кто ответит на лечение. В этом исследовании представлена вычислительная платформа под названием TRIM, которая обучается на подробных одно-клеточных измерениях T-клеток в крови и опухолях. Комбинируя информацию о генетической активности каждой клетки и её уникальном T-клеточном рецепторе, TRIM может предсказывать, как T-клетки будут расширяться и изменяться после терапии, предлагая потенциальный способ прогнозировать эффективность лечения по обычному анализу крови.
Взгляд внутрь отдельных T-клеток
T-клетки патрулируют организм и ищут признаки опасности с помощью своих рецепторов, которые распознают специфические молекулярные фрагменты. Когда T-клетка сталкивается с раком, она может размножаться в клон из множества почти идентичных клеток и принимать различные функции: от активных киллеров опухоли до истощённых клеток, которые уже не в состоянии эффективно бороться. Современные одно-клеточные технологии позволяют для каждой T-клетки читать и профиль экспрессии генов (какие гены включены или выключены), и последовательность её рецептора. Авторы применили эти инструменты к тысячам T-клеток пациентов с раком головы и шеи, колоректальным и несколькими другими типами опухолей, отбирая образцы крови и опухолевой ткани до и после иммунотерапии.
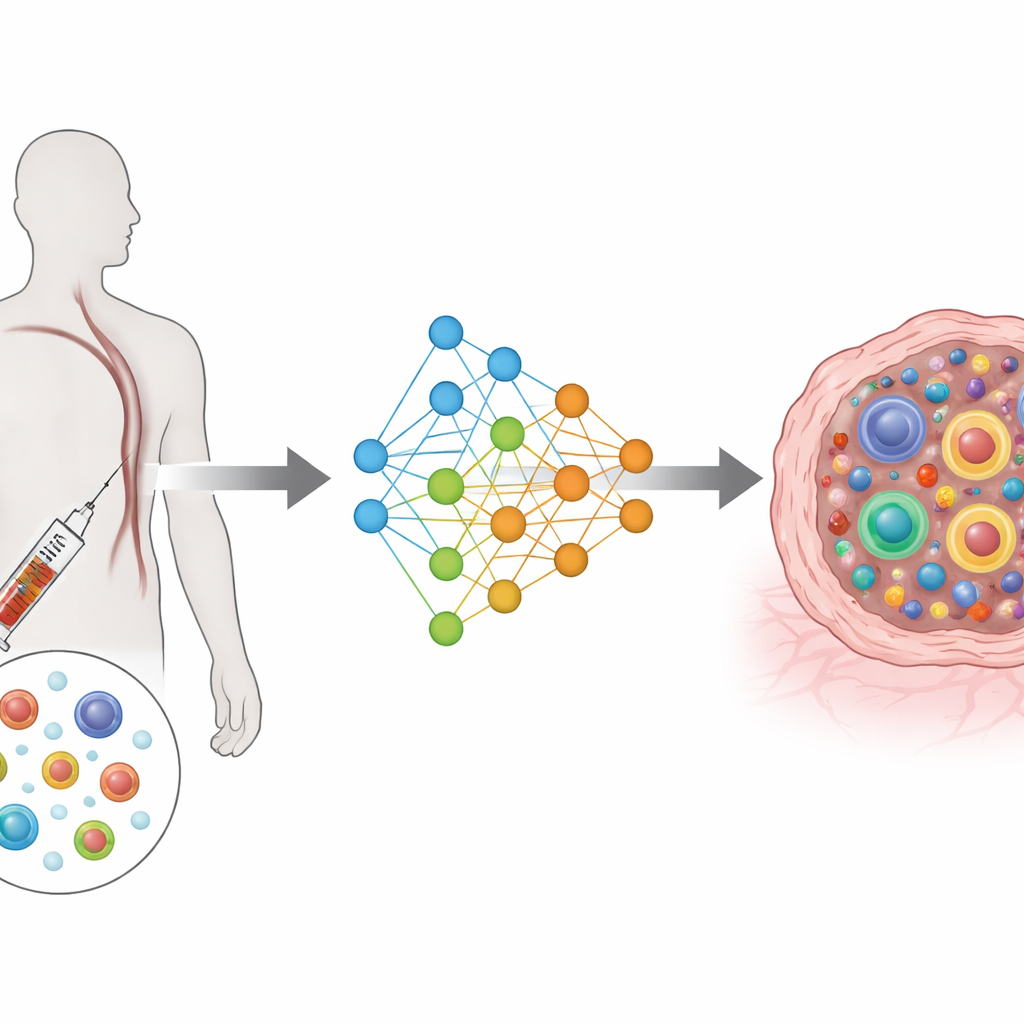
От сложных измерений к общей карте
TRIM основан на типе глубокой нейронной архитектуры, известной как условный вариационный автокодировщик. Проще говоря, он сжимает богатую информацию о генах и рецепторе каждой клетки в общую низкоразмерную карту, при этом учитывая, к какому пациенту принадлежит клетка, откуда она взята (кровь или опухоль) и когда была собрана (до или после лечения). Отдельные входные модули читают особенности экспрессии и рецептора, а отдельные выходные модули пытаются их восстановить. Специальная функция потерь подталкивает клетки одного клона располагаться близко друг к другу на этой карте, одновременно разделяя разные клоны. Такая конструкция концентрирует модель на биологически важных вещах: размере каждого клона и распределении его клеток по функциональным состояниям.
Что связывает рецепторы, экспрессию генов и клоны
Систематически сравнивая сходство рецепторов и профиль экспрессии в нескольких наборах данных, исследователи обнаружили, что клетки, имеющие точно такой же рецептор, действительно более похожи друг на друга по экспрессии генов, чем случайные T-клетки, особенно в крупных, расширенных клонах. Однако вне точных совпадений небольшие изменения в последовательности рецептора не надежно коррелируют с похожестью двух клеток по экспрессии генов. Иными словами, клетки с почти идентичными рецепторами могут выглядеть так же по-разному, как клетки с совершенно разными рецепторами. Это привело команду к сосредоточению внимания на идентичности клонов и их размере, а не на тонкой последовательностной похожести рецепторов, как на ключевом мосте между информацией о рецепторе и состоянием клетки.
Прогнозирование опухолевых T-клеток по крови
Ключевым испытанием для TRIM было то, сможет ли он, имея только данные крови до лечения, сгенерировать реалистичные прогнозы для T-клеток того же пациента в опухоли и в крови после терапии. Авторы обучали TRIM на всех пациентах кроме одного и затем просили предсказать отложенного пациента, повторяя это по когорте. Они показали, что модель точно отражает общую картину состояний T-клеток и разнообразия клонов между условиями. Ещё более примечательно, что для отдельных реципторных клонов, присутствовавших до терапии, TRIM мог предсказывать, какие из них будут расширяться после лечения, с высокой точностью, существенно превосходя стандартные методы машинного обучения. Модель также воспроизводила известные сигнатуры успешного ответа, например увеличение активных, пролиферирующих CD8 T-клеток и специфические генные программы, связанные с эффективным убийством опухоли.
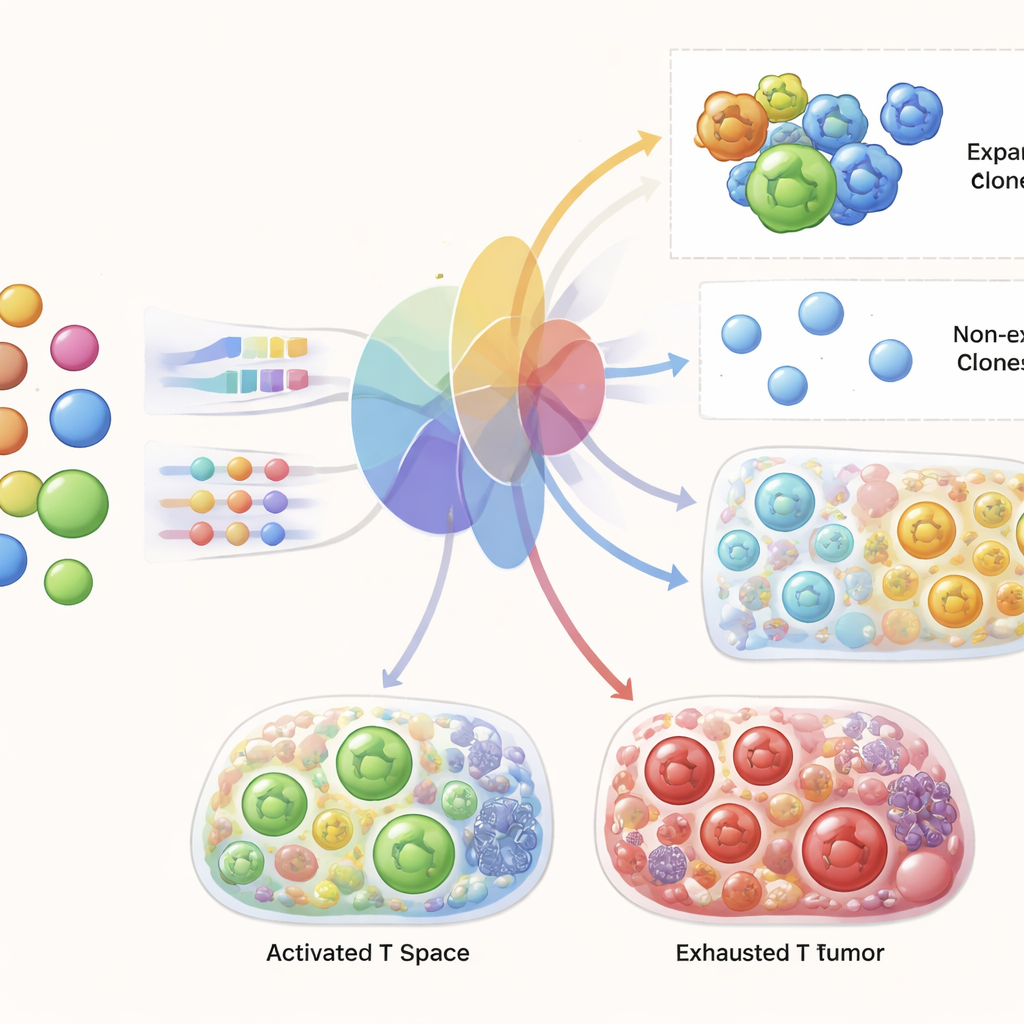
Выявление генов, стоящих за успешным расширением
Поскольку TRIM должен внутри себя решать, какие клетки, вероятно, расширятся, авторы могли исследовать модель, чтобы понять, на какие гены она опирается. Гены, выделенные TRIM, соответствуют ключевым признакам активации T-клеток: регуляторы клеточного цикла, контролирующие пролиферацию, молекулы, участвующие в уничтожении целей, белки, управляющие активацией и коммуникацией, а также метаболические и миграционные факторы, которые помогают T-клеткам проникать в опухоль и функционировать в ней. Важно, что модель выявила эти программы, используя только предлечебные данные крови на этапе предсказания, что указывает на то, что ранние молекулярные различия в циркулирующих T-клетках предвосхищают их дальнейшее поведение при встрече с опухолевыми сигналами после начала терапии.
Что это значит для пациентов
По сути, эта работа демонстрирует, что тщательно спроектированная модель может научиться на мультимодальных одно-клеточных данных и прогнозировать поведение T-клеток пациента в ходе противораковой иммунотерапии. TRIM использует образцы крови до лечения, чтобы определить, какие клоны будут расширяться, в какие состояния они перейдут и какие генные программы будут этому способствовать, даже в тканях, которые трудно напрямую исследовать. Хотя для клинического применения требуется дальнейшая валидация и больший объём данных, подход указывает на будущее, в котором онкологи смогут использовать простой анализ крови в сочетании с моделями наподобие TRIM для прогнозирования ответа на лечение, мониторинга прогрессирования болезни и поиска новых биомаркеров, которые направляют персонализированные решения по иммунотерапии.
Цитирование: He, C., Amodio, M., Ashenberg, O. et al. Multimodal framework for the joint analysis of single-cell RNA and T cell receptor sequencing data predicts T cell response to cancer immunotherapy. Nat Commun 17, 3840 (2026). https://doi.org/10.1038/s41467-026-70505-0
Ключевые слова: противораковая иммунотерапия, T-клетки, одно-клеточное секвенирование, модель машинного обучения, биомаркеры опухоли