Clear Sky Science · sv
Multimodalt ramverk för gemensam analys av enkelcells-RNA och T‑cellreceptorsekvenser för att förutsäga T‑cellsrespons vid cancerimmunterapi
Varför det är viktigt att förutsäga immunrespons
Cancerimmunterapier, såsom läkemedel som hämmar kontrollpunkter, fungerar genom att frigöra patientens egna T‑celler så att de kan angripa tumörer. Endast en del av patienterna gynnas dock, och läkare har i dag begränsade verktyg för att förutse vem som kommer att svara. Denna studie presenterar ett beräkningsramverk kallat TRIM som lär sig från detaljerade enkelcellsmätningar av T‑celler i blod och tumörer. Genom att kombinera information om varje cells genaktivitet och dess unika T‑cellreceptor kan TRIM förutsäga hur T‑celler kommer att expandera och förändras efter behandling, vilket erbjuder ett potentiellt sätt att förutse behandlingseffekt med ett rutinmässigt blodprov.
En inblick i enskilda T‑celler
T‑celler patrullerar kroppen och söker efter tecken på fara med hjälp av sina T‑cellreceptorer, som känner igen specifika molekylära fragment. När en T‑cell möter cancer kan den multiplicera sig till en klon av många nästintill identiska celler och inta olika roller, från aktiva tumördödare till utmattade celler som inte längre kan bekämpa effektivt. Moderna enkelcellstekniker kan nu läsa, för varje T‑cell, både dess genuttrycksprofil (vilka gener som är på- eller avstängda) och dess receptorsekvens. Författarna tillämpade dessa verktyg på tusentals T‑celler från patienter med huvud‑ och halscancer, kolorektalcancer och flera andra cancerformer, med provtagning från både blod och tumörvävnad före och efter immunterapi.
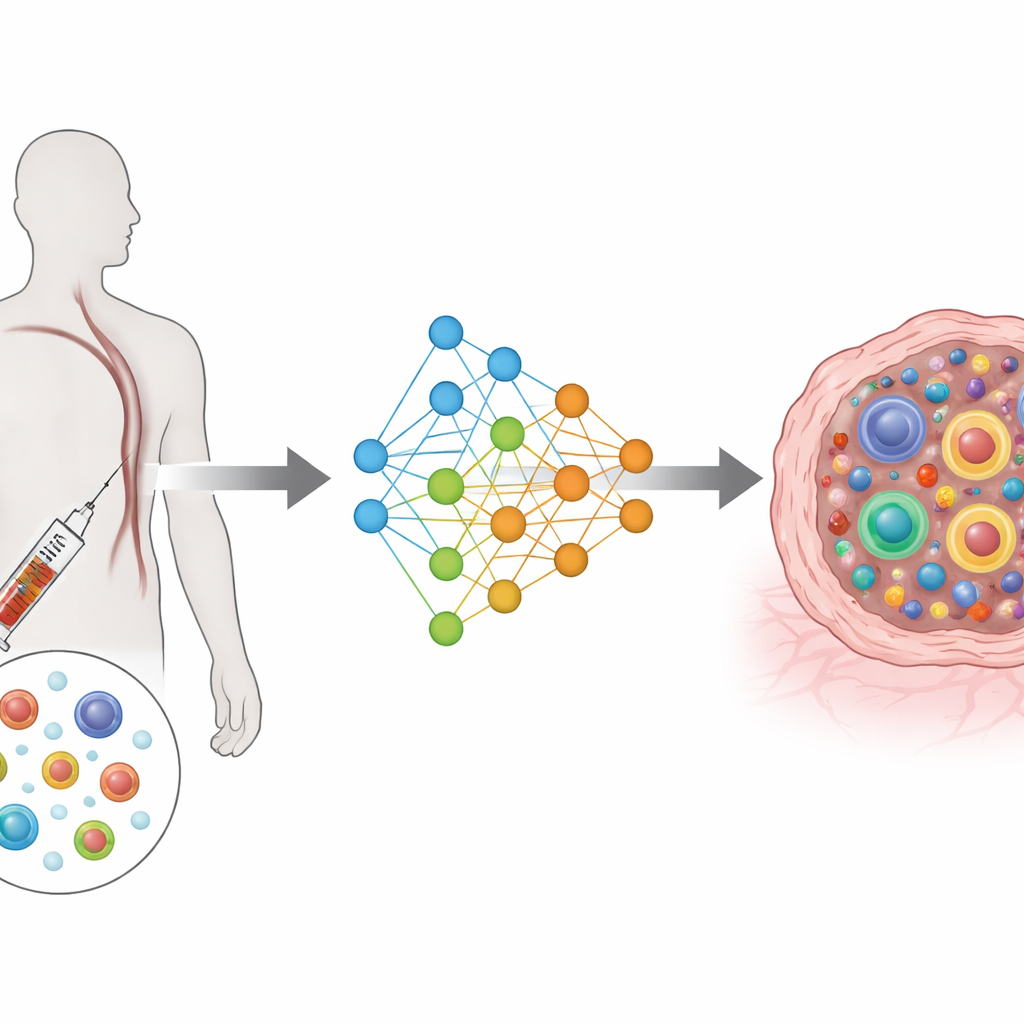
Från komplexa mätningar till en gemensam karta
TRIM bygger på en typ av djupinlärningsarkitektur som kallas villkorad variational autoencoder. Enkelt uttryckt komprimerar den den rika informationen från varje cells gener och receptor till en delad lågdimensionell karta, samtidigt som den tar hänsyn till vem patienten är, var cellen kom ifrån (blod eller tumör) och när den samlades in (före eller efter behandling). Separata inmatningsmoduler läser av genaktivitet och receptorfunktioner, och separata utmatningsmoduler försöker rekonstruera dem. En särskild förlustfunktion styr celler som tillhör samma klon att placera sig nära varandra i denna karta, samtidigt som olika kloner hålls isär. Denna design riktar modellens fokus mot det som biologiskt är viktigast: hur stor varje klon är och hur dess celler fördelas över funktionella tillstånd.
Vad som binder samman receptorer, genaktivitet och kloner
Genom att systematiskt jämföra receptorsimilaritet och genuttryck över flera dataset fann forskarna att celler som delar exakt samma receptor faktiskt är mer lika varandra i genaktivitet än slumpmässiga T‑celler, särskilt för stora, expanderade kloner. Men utöver exakta matchningar korrelerar små förändringar i receptorsekvensen inte pålitligt med hur lika två celler är i sitt genuttryck. Med andra ord kan celler med nästan identiska receptorer se lika olika ut som celler med helt orelaterade receptorer. Detta ledde teamet till att fokusera på klonidentitet och klonstorlek, snarare än finmaskig receptorsekvenslikhet, som den avgörande bron mellan receptorinformation och celltillstånd.
Att förutsäga tumörbindna T‑celler från blod
Det centrala testet för TRIM var om modellen enbart utifrån pre‑behandlingsbloddata från en patient kunde generera realistiska förutsägelser för den patientens T‑celler i tumören och i blodet efter terapi. Författarna tränade TRIM på alla utom en patient och bad sedan modellen förutsäga den utelämnade patienten, och upprepade detta över kohorter. De visade att modellen exakt fångar det övergripande landskapet av T‑cellsgenstatus och klondiversitet över betingelser. Ännu mer anmärkningsvärt var att för individuella receptorkloner som var närvarande före terapi kunde TRIM förutsäga vilka som skulle expandera efter behandling med hög noggrannhet, och klart överträffa standardmetoder inom maskininlärning. Den återgav också kända signaturer för framgångsrikt svar, såsom en ökning av aktiverade, prolifererande CD8‑T‑celler och specifika genprogram kopplade till effektiv tumördödning.
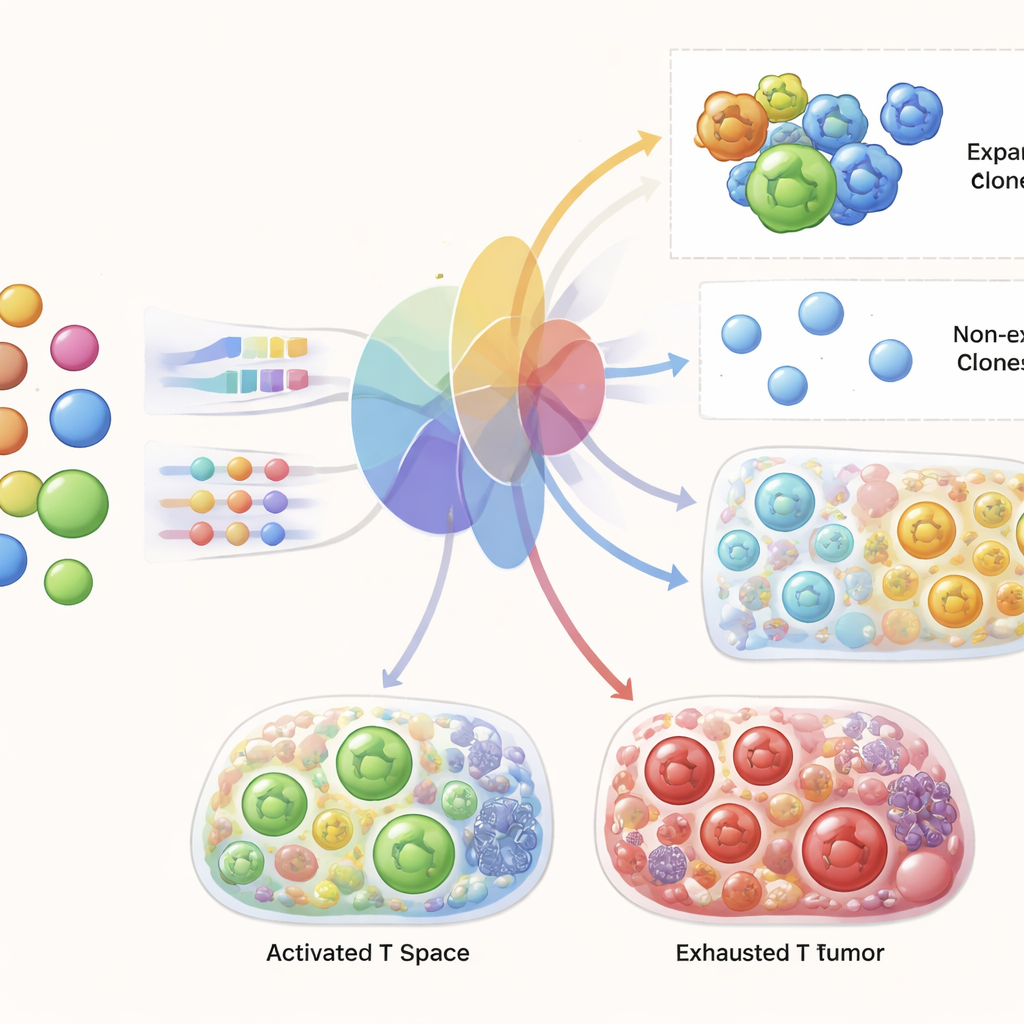
Att avslöja generna bakom framgångsrik expansion
Eftersom TRIM internt måste avgöra vilka celler som sannolikt kommer att expandera kunde författarna undersöka modellen för att se vilka gener den förlitar sig på. De gener som TRIM pekade ut stämmer överens med centrala drag vid T‑cellsaktivering: cellcykelregulatorer som styr proliferation, molekyler inblandade i målcellsdöd, proteiner som reglerar aktivering och kommunikation samt metabola och migrationsrelaterade faktorer som hjälper T‑celler att röra sig in i och fungera i tumörer. Viktigt är att modellen identifierade dessa program enbart utifrån pre‑behandlingsbloddata vid prediktionstidpunkten, vilket antyder att tidiga molekylära skillnader i cirkulerande T‑celler förebådar hur de kommer att svara när behandlingen börjar och de möter tumörsignaler.
Vad detta betyder för patienter
I huvudsak visar detta arbete att en noggrant utformad modell kan lära sig från multimodala enkelcellsdata för att förutsäga hur en patients T‑celler kommer att bete sig under cancerimmunterapi. TRIM använder pre‑behandlingsblodprover för att härleda vilka kloner som kommer att expandera, vilka tillstånd de kommer att inta och vilka genprogram som driver detta beteende, även i vävnader som är svåra att få tag på direkt. Även om vidare validering och större datamängder krävs innan klinisk användning, pekar tillvägagångssättet mot en framtid där onkologer kan använda ett enkelt blodprov, tillsammans med modeller som TRIM, för att förutsäga behandlingssvar, övervaka sjukdomsutveckling och upptäcka nya biomarkörer som styr personligt anpassade immunterapibeslut.
Citering: He, C., Amodio, M., Ashenberg, O. et al. Multimodal framework for the joint analysis of single-cell RNA and T cell receptor sequencing data predicts T cell response to cancer immunotherapy. Nat Commun 17, 3840 (2026). https://doi.org/10.1038/s41467-026-70505-0
Nyckelord: cancerimmunterapi, T‑celler, enkelcellssekvensering, maskininlärningsmodell, tumörbiomarkörer