Clear Sky Science · tr
Tek hücre RNA ve T hücresi reseptör dizileme verilerinin ortak analizi için çok modlu çerçeve, T hücresi yanıtını kanser immünoterapisine karşı tahmin ediyor
Bağışıklık yanıtını tahmin etmenin önemi
Kontrol noktası inhibitörleri gibi kanser immünoterapileri, hastanın kendi T hücrelerini tümörlere karşı serbest bırakarak etki gösterir. Yine de yalnızca bazı hastalar fayda görür ve doktorların kimlerin yanıt vereceğini öngörmek için sınırlı araçları vardır. Bu çalışma, kan ve tümörlerdeki T hücrelerinin ayrıntılı tek hücre ölçümlerinden öğrenen TRIM adlı hesaplamalı bir çerçeve sunuyor. Her hücrenin gen aktivitesi ve benzersiz T hücresi reseptörüne ilişkin bilgileri birleştirerek, TRIM tedavi sonrası T hücrelerinin nasıl genişleyeceğini ve değişeceğini tahmin edebiliyor; bu da rutin bir kan örneğinden tedavi başarısını öngörmenin potansiyel bir yolunu sunuyor.
Bireysel T hücrelerinin içini görmek
T hücreleri, belirli moleküler parçaları tanıyan T hücresi reseptörleri aracılığıyla vücudu devriye gezer ve tehlike işaretleri arar. Bir T hücresi kanserle karşılaştığında, birçok neredeyse özdeş hücreden oluşan bir klona çoğalabilir ve aktif tümör öldürücülerden etkinliğini yitirmiş tükenmiş hücrelere kadar farklı rolleri üstlenebilir. Modern tek hücre teknolojileri artık her T hücresi için hem gen ifade profilini (hangi genlerin açık veya kapalı olduğu) hem de reseptör dizisini okuyabiliyor. Yazarlar bu araçları, baş ve boyun, kolorektal ve birkaç başka kanser türünden hastaların binlerce T hücresinde uygulayarak tedavi öncesi ve sonrası hem kanı hem de tümör dokusunu örneklediler.
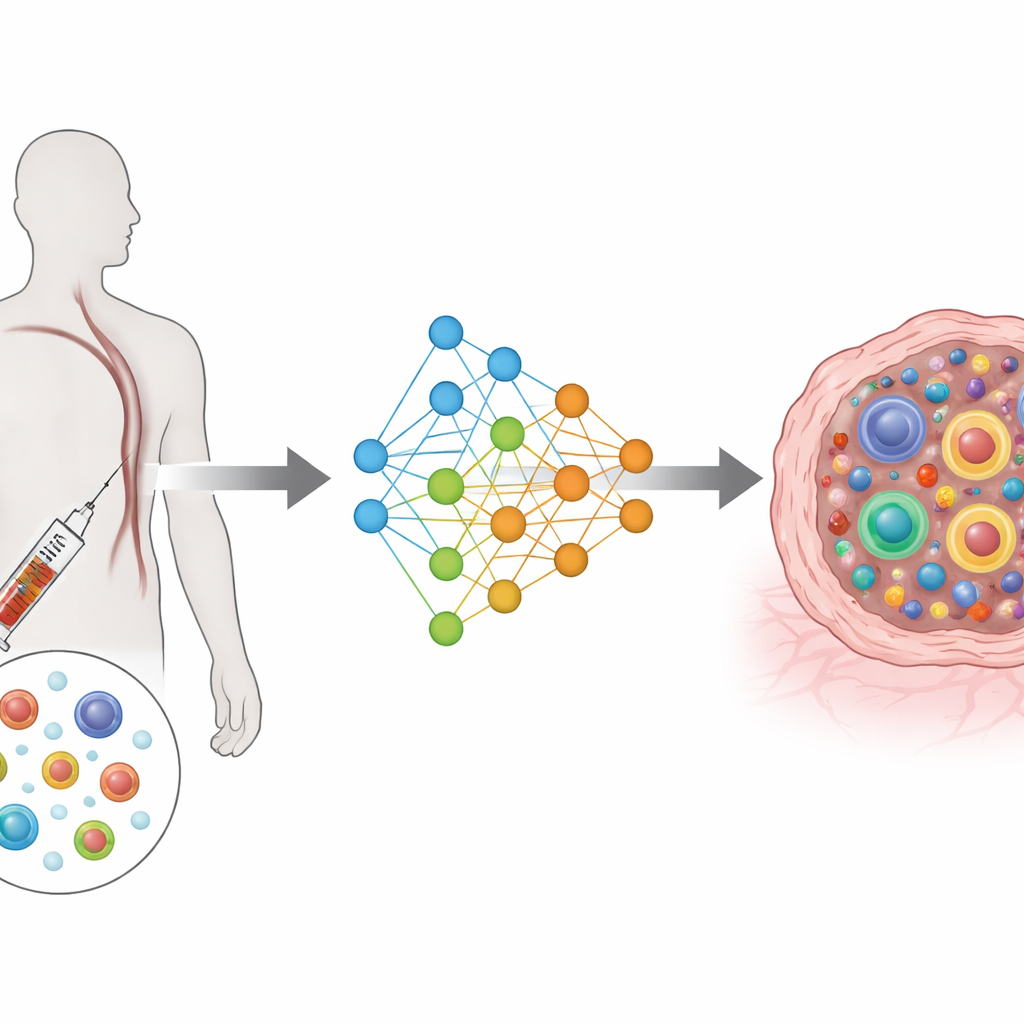
Karmaşık ölçümlerden ortak bir haritaya
TRIM, koşullu varyasyonel otoenkoder olarak bilinen bir tür derin öğrenme mimarisi üzerine kuruludur. Basitçe söylemek gerekirse, her hücrenin genleri ve reseptöründen gelen zengin bilgileri, hastanın kim olduğu, hücrenin nereden geldiği (kan veya tümör) ve ne zaman toplandığı (tedavi öncesi veya sonrası) gibi bilgileri de dikkate alarak paylaşılan düşük boyutlu bir haritada sıkıştırır. Ayrı giriş modülleri gen aktivitesini ve reseptör özelliklerini okur, ayrı çıkış modülleri ise bunları yeniden oluşturmayı dener. Özel bir kayıp işlevi, aynı klona ait hücrelerin bu haritada birbirine yakın oturmasını teşvik ederken farklı klonları ayrı tutar. Bu tasarım modeli biyolojik olarak en önemli olana odaklar: her klonun büyüklüğü ve hücrelerinin fonksiyonel durumlar arasındaki dağılımı.
Reseptörleri, gen aktivitesini ve klonları birbirine bağlayan nedir
Araştırmacılar, reseptör benzerliği ve gen ekspresyonunu birden çok veri kümesi arasında sistematik olarak karşılaştırarak, tam olarak aynı reseptörü paylaşan hücrelerin, özellikle büyük ve genişlemiş klonlarda, rastgele T hücrelerinden gerçekten daha benzer gen aktivitesine sahip olduğunu buldular. Ancak, tam eşleşmelerin ötesinde, reseptör dizisindeki küçük değişiklikler iki hücrenin gen ifadelerinin ne kadar benzer olduğu ile güvenilir şekilde ilişkili değildi. Başka bir deyişle, neredeyse özdeş reseptörlere sahip hücreler, tamamen alakasız reseptörlü hücreler kadar farklı görünebilir. Bu nedenle ekip, reseptör dizisi benzerliğinin ince ayrıntılarından ziyade, reseptör bilgisi ile hücre durumu arasındaki kritik köprü olarak klon kimliğine ve klon büyüklüğüne odaklanmaya karar verdi.
Kandan tümöre bağlı T hücrelerini tahmin etmek
TRIM için merkezi test, yalnızca bir hastanın tedavi öncesi kan verisini alıp o hastanın tedavi sonrası tümördeki ve kandaki T hücreleri için gerçekçi tahminler üretebilmesi oldu. Yazarlar, bir hastayı tutarak geri kalan tüm hastalar üzerinde TRIM'i eğittiler ve ardından tutulan hastayı tahmin etmesini istediler; bunu farklı kohortlar boyunca tekrarladılar. Modelin koşullar arasında T hücre gen durumlarının ve klon çeşitliliğinin genel manzarasını doğru şekilde yakaladığını gösterdiler. Daha da çarpıcı olarak, tedavi öncesi mevcut bireysel reseptör klonları için TRIM, hangi klonların tedavi sonrası genişleyeceğini yüksek doğrulukla tahmin edebildi ve standart makine öğrenmesi yaklaşımlarını belirgin şekilde geride bıraktı. Ayrıca etkin tümör öldürmeye bağlı belirli gen programları ve aktive olup çoğalan CD8 T hücrelerinde artış gibi başarılı yanıtın bilinen imzalarını yeniden üretti.
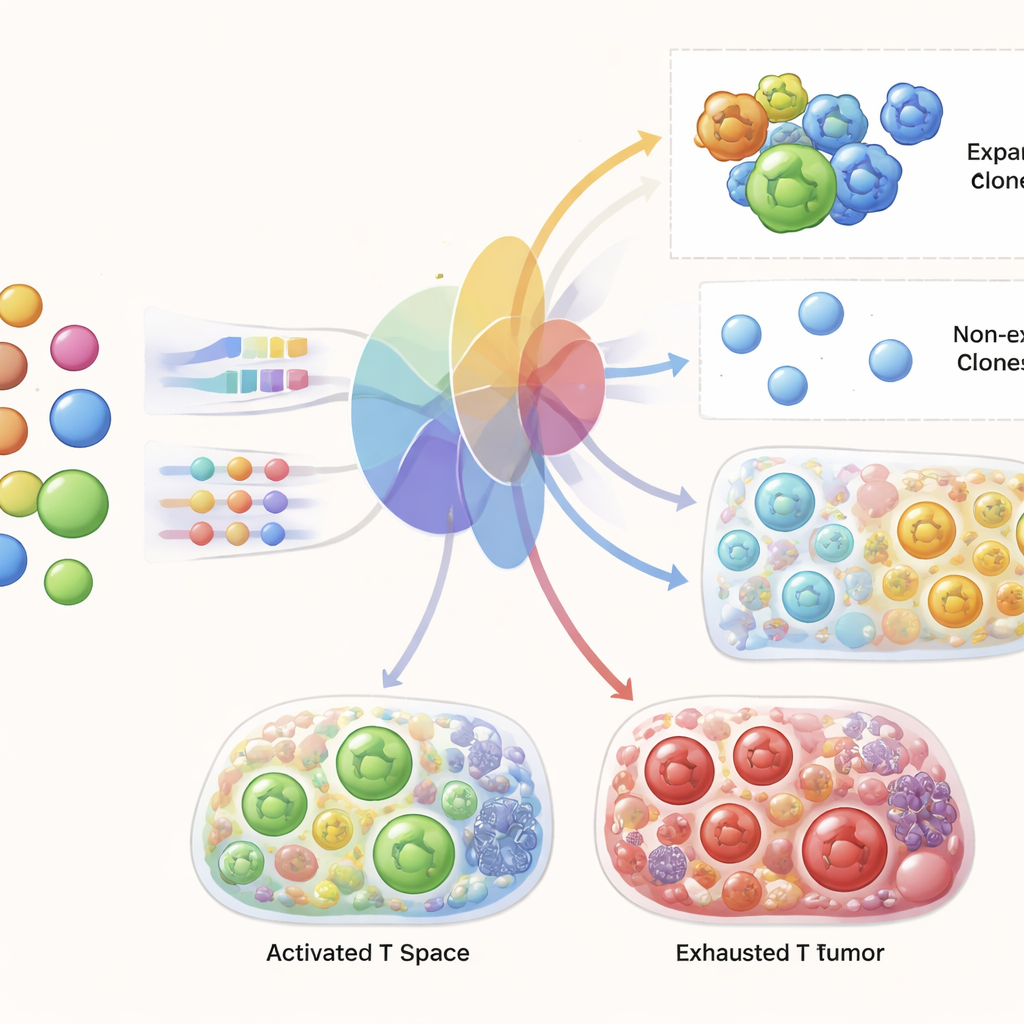
Başarılı genişlemenin arkasındaki genleri ortaya çıkarmak
TRIM, dahili olarak hangi hücrelerin muhtemel olarak genişleyeceğine karar vermek zorunda olduğundan, yazarlar modelin hangi genlere dayandığını inceleyebildiler. TRIM tarafından işaretlenen genler, T hücresi aktivasyonunun çekirdek özellikleriyle örtüşüyor: proliferasyonu kontrol eden hücre döngüsü düzenleyicileri, hedef hücreleri öldürmede rol oynayan moleküller, aktivasyonu ve iletişimi yöneten proteinler ile T hücrelerinin tümörlere girip işlev göstermesine yardımcı olan metabolik ve göçle ilgili faktörler. Önemli olarak, model bu programları sadece tahmin zamanında elde edilen tedavi öncesi kan verisini kullanarak tanımladı; bu da dolaşımdaki T hücrelerindeki erken moleküler farklılıkların, tedavi başladıktan ve hücreler tümör sinyalleriyle karşılaştıktan sonra nasıl yanıt vereceklerini önceden haber verebileceğini gösteriyor.
Bu hastalar için ne anlama geliyor
Özünde bu çalışma, dikkatle tasarlanmış bir modelin çok modlu tek hücre verilerinden öğrenerek bir hastanın T hücrelerinin kanser immünoterapisi sırasında nasıl davranacağını öngörebileceğini gösteriyor. TRIM, tedavi öncesi kan örneklerini kullanarak hangi klonların genişleyeceğini, hangi durumlara gireceklerini ve bu davranışı yönlendirecek gen programlarını, doğrudan örneklemesi zor olan dokularda bile çıkarıyor. Klinik kullanım öncesi daha fazla doğrulama ve daha büyük veri kümeleri gerekse de, yaklaşım onkologların TRIM benzeri modellerle eşleştirilmiş basit bir kan testi kullanarak tedavi yanıtını tahmin edebileceği, hastalığı izleyebileceği ve kişiselleştirilmiş immünoterapi kararlarını yönlendirecek yeni biyobelirteçler keşfedebileceği bir geleceğe işaret ediyor.
Atıf: He, C., Amodio, M., Ashenberg, O. et al. Multimodal framework for the joint analysis of single-cell RNA and T cell receptor sequencing data predicts T cell response to cancer immunotherapy. Nat Commun 17, 3840 (2026). https://doi.org/10.1038/s41467-026-70505-0
Anahtar kelimeler: kanser immünoterapisi, T hücreleri, tek hücre dizileme, makine öğrenmesi modeli, tümör biyobelirteçleri