Clear Sky Science · ar
إطار متعدد الأنماط للتحليل المشترك لتسلسل RNA أحادي الخلية وتسلسل مستقبلات الخلايا التائية يتنبأ باستجابة الخلايا التائية للمناعة ضد السرطان
لماذا يهم التنبؤ بالاستجابة المناعية
تعمل العلاجات المناعية للسرطان، مثل أدوية مثبطات نقاط التفتيش، عن طريق إطلاق قدرة خلايا المريض التائية على مهاجمة الأورام. ومع ذلك لا يستفيد سوى عدد من المرضى، والأطباء حالياً لديهم أدوات محدودة للتنبؤ بمن سيستجيب. تقدم هذه الدراسة إطاراً حسابياً اسمه TRIM يتعلم من قياسات مفصلة على مستوى الخلية الواحدة للخلايا التائية في الدم والأورام. من خلال دمج معلومات نشاط الجينات في كل خلية وتسلسل مستقبل الخلية التائية الفريد، يمكن لـ TRIM التنبؤ بكيفية توسع الخلايا التائية وتغيرها بعد العلاج، مما يقدم طريقة محتملة لتوقع نجاح العلاج من عينة دم روتينية.
نظرة داخل الخلايا التائية الفردية
تجوب الخلايا التائية الجسم بحثاً عن دلائل الخطر باستخدام مستقبلاتها التائية التي تتعرف على شظايا جزيئية محددة. عندما تصادف خلية تائية السرطان، يمكن أن تتكاثر إلى مستعمرة من الخلايا المتشابهة تقريباً وتتولى أدواراً مختلفة، من قاتلات نشطة للأورام إلى خلايا منهكة لم تعد قادرة على القتال بشكل فعال. تتيح تقنيات أحادية الخلية الحديثة الآن قراءة ملف تعبير الجينات لكل خلية (أي أي الجينات مُفعّلة أو مُطفأة) وتسلسل مستقبلها. طبق المؤلفون هذه الأدوات عبر آلاف الخلايا التائية من مرضى مصابين بسرطانات في الرأس والعنق والقولون وأنواع سرطانية أخرى، ما أخذ عينات من الدم ونسيج الورم قبل وبعد العلاج المناعي.
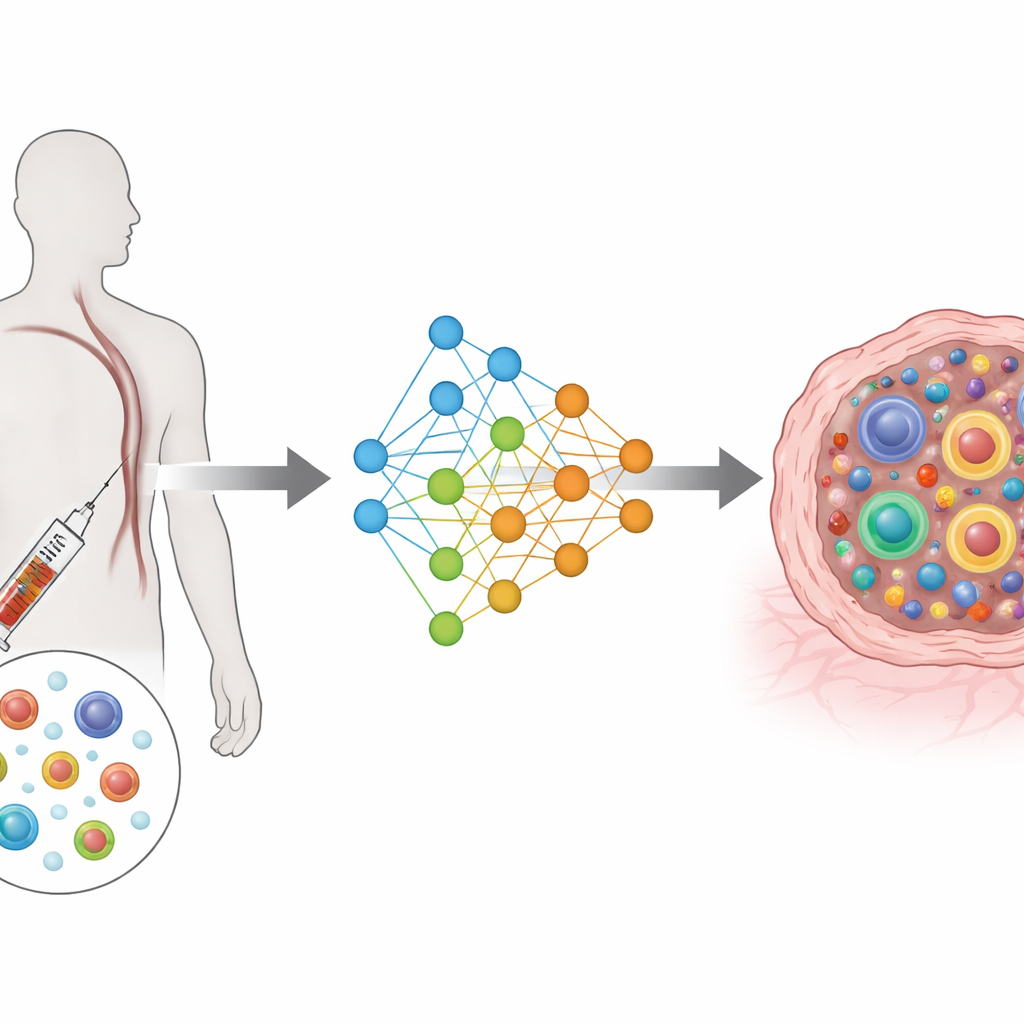
من قياسات معقدة إلى خريطة مشتركة
يبنى TRIM على نوع من بنية التعلم العميق تعرف باسم المشفر التبايني الشرطي. ببساطة، يضغط المعلومات الغنية من جينات كل خلية ومستقبلها إلى خريطة مشتركة منخفضة الأبعاد، مع أخذ هوية المريض ومصدر الخلية (الدم أو الورم) ووقت جمعها (قبل أو بعد العلاج) في الاعتبار. تقرأ وحدات إدخال منفصلة نشاط الجينات وميزات المستقبل، وتحاول وحدات إخراج منفصلة إعادة بنائهما. دالة خسارة خاصة تدفع الخلايا التي تنتمي إلى نفس المستعمرة لتتجمع بالقرب من بعضها في هذه الخريطة، مع إبقاء المستعمرات المختلفة منفصلة. يركز هذا التصميم النموذج على ما يهم بيولوجياً: حجم كل مستعمرة وكيفية توزيع خلاياها عبر الحالات الوظيفية.
ما الذي يربط المستقبلات ونشاط الجينات والمستعمرات
من خلال المقارنة المنهجية بين تشابه المستقبلات وتعبير الجينات عبر مجموعات بيانات متعددة، وجد الباحثون أن الخلايا التي تشترك تماماً في نفس المستقبل تشبه بعضها البعض في نشاط الجينات أكثر من خلايا تائية عشوائية، لا سيما في المستعمرات الكبيرة والمتوسعة. مع ذلك، خارج المطابقات الدقيقة، التغيرات الصغيرة في تسلسل المستقبل لا تتتبع باستمرار مدى تشابه خليتين في تعبيرهما الجيني. بعبارة أخرى، يمكن أن تبدو الخلايا ذات المستقبلات المتطابقة تقريباً مختلفة تماماً مثل خلايا ذات مستقبلات غير مرتبطة. دفع هذا الفريق للتركيز على هوية المستعمرة وحجمها، بدلاً من التشابه الدقيق لتسلسل المستقبل، كالجسر الحاسم بين معلومات المستقبل وحالة الخلية.
التنبؤ بالخلايا التائية المرتبطة بالورم من الدم
الاختبار المحوري لـ TRIM كان ما إذا كان يمكنه الاعتماد على بيانات الدم قبل العلاج فقط من مريض وتوليد توقعات واقعية لخلايا ذلك المريض التائية في الورم وفي الدم بعد العلاج. درّب المؤلفون TRIM على جميع المرضى ما عدا واحد ثم طلبوا منه التنبؤ بالمريض المستثنى، مكررين ذلك عبر مجموعات المرضى. أظهروا أن النموذج يلتقط بدقة المشهد العام لحالات تعبير الجينات وتنوع المستعمرات عبر الحالات. والأكثر لفتاً، بالنسبة للمستعمرات المفردة ذات المستقبلات الموجودة قبل العلاج، استطاع TRIM التنبؤ بتلك التي ستتوسع بعد العلاج بدقة عالية، متفوقاً بوضوح على مناهج التعلم الآلي التقليدية. كما أعاد إنتاج توقيعات معروفة للاستجابة الناجحة، مثل ازدياد الخلايا CD8 النشطة والمنتشرة وبرامج جينية محددة مرتبطة بالقتل الفعال للأورام.
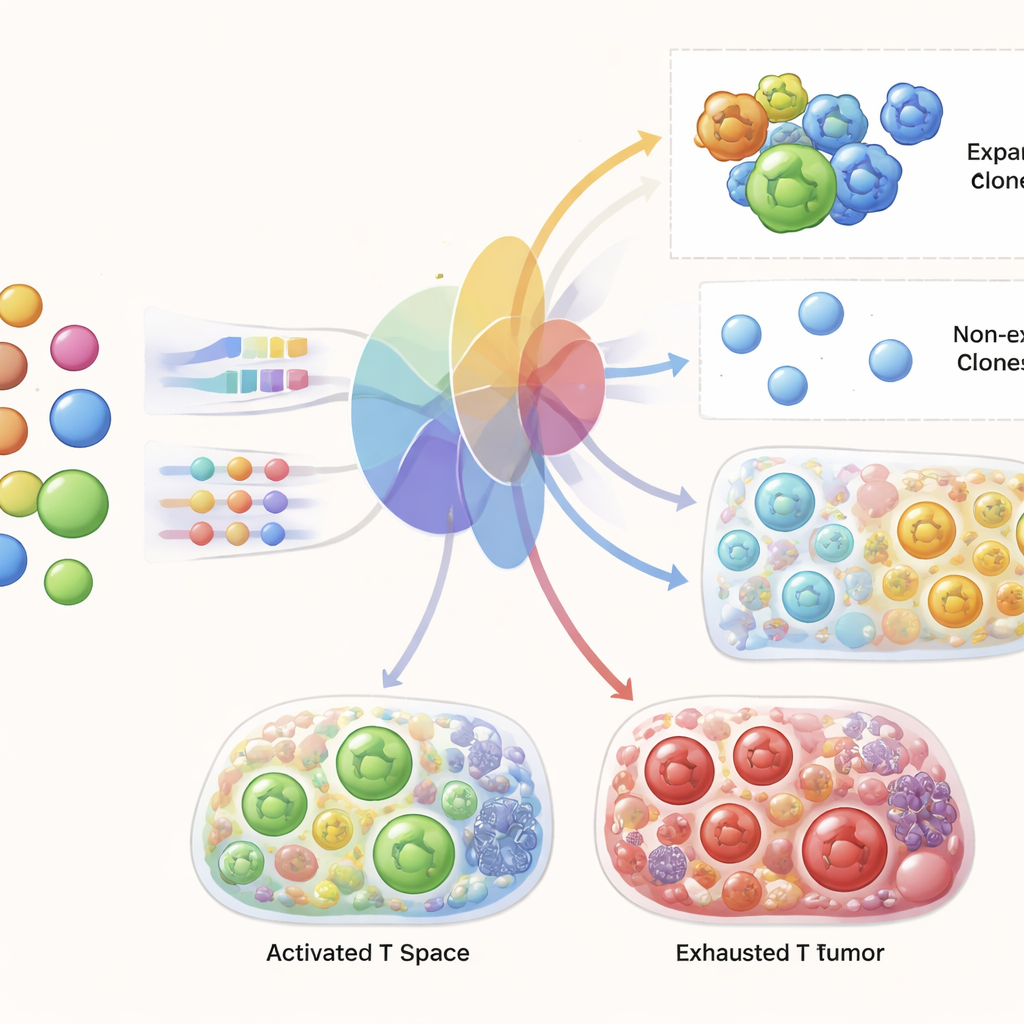
الكشف عن الجينات وراء التوسع الناجح
بما أن TRIM يجب أن يقرر داخلياً أي الخلايا مرجح أن تتوسع، تمكن المؤلفون من فحص النموذج لمعرفة الجينات التي يعتمد عليها. تتوافق الجينات التي أظهرها TRIM مع ميزات أساسية لتنشيط الخلايا التائية: منظمات دورة الخلية التي تتحكم في التكاثر، جزيئات مشاركة في قتل الخلايا الهدف، بروتينات تحكم التنشيط والتواصل، وعوامل أيضية ومتعلقة بالهجرة تساعد الخلايا التائية على الانتقال إلى الأورام والعمل داخلها. والأهم من ذلك، أن النموذج حدَّد هذه البرامج باستخدام بيانات الدم قبل العلاج فقط في وقت التنبؤ، مما يشير إلى أن الفروق الجزيئية المبكرة في الخلايا التائية الدائرة تسبق كيف ستستجيب بمجرد بدء العلاج ومواجهتها لإشارات الورم.
ماذا يعني هذا للمرضى
باختصار، تُظهر هذه العمل أن نموذجاً مصمماً بعناية يمكنه التعلم من بيانات أحادية الخلية متعددة الأنماط للتنبؤ بكيفية تصرف خلايا المريض التائية أثناء العلاج المناعي للسرطان. يستخدم TRIM عينات دم قبل العلاج لاستنتاج أي المستعمرات ستتوسع، وما الحالات التي ستدخلها، وأي البرامج الجينية ستقود هذا السلوك، حتى في الأنسجة التي يصعب أخذ عينات منها مباشرة. وبينما هناك حاجة لتأكيدات إضافية ومجموعات بيانات أكبر قبل الاستخدام السريري، يشير هذا النهج إلى مستقبل قد يستخدم فيه أطباء الأورام اختبار دم بسيط، مقترناً بنماذج مثل TRIM، لتوقع استجابة العلاج، ومراقبة تقدم المرض، واكتشاف مؤشرات حيوية جديدة توجه قرارات العلاج المناعي الشخصية.
الاستشهاد: He, C., Amodio, M., Ashenberg, O. et al. Multimodal framework for the joint analysis of single-cell RNA and T cell receptor sequencing data predicts T cell response to cancer immunotherapy. Nat Commun 17, 3840 (2026). https://doi.org/10.1038/s41467-026-70505-0
الكلمات المفتاحية: العلاج المناعي للسرطان, الخلايا التائية, تسلسل أحادي الخلية, نموذج تعلم آلي, مؤشرات ورمية