Clear Sky Science · zh
通过解离四聚体和活性位点变构由单一抗体残基实现对β-胰蛋白酶的完全抑制
这对过敏和哮喘为何重要
患有哮喘、严重过敏或过敏性休克的人经常受困于组织中某些免疫细胞释放的强效化学物质,这些物质会收缩气道并损伤组织。一个关键罪魁是储存在肥大细胞中并在过敏反应时释放的酶β‑胰蛋白酶。本研究描述了一种经工程改造的抗体,能够以一种新颖的方式将β‑胰蛋白酶完全关闭,或为针对肥大细胞驱动疾病的更好治疗开辟新途径。
肥大细胞内的麻烦制造者
肥大细胞像哨兵一样分布在肺、肠和皮肤等组织中。当它们感知到过敏原、毒液或微生物时,会迅速释放装有组胺、信号蛋白和酶的颗粒。β‑胰蛋白酶是这些酶中最丰富的一种,推动气道收窄、额外的胶原生成以及肺部平滑肌收缩,所有这些都会加剧哮喘和其他炎症性疾病。β‑胰蛋白酶通常组装成一个四聚体环,其活性位点朝向中央孔。这种构型将活性中心对大多数体内天然抑制剂隐藏起来,使β‑胰蛋白酶尤其难以用常规药物阻断。
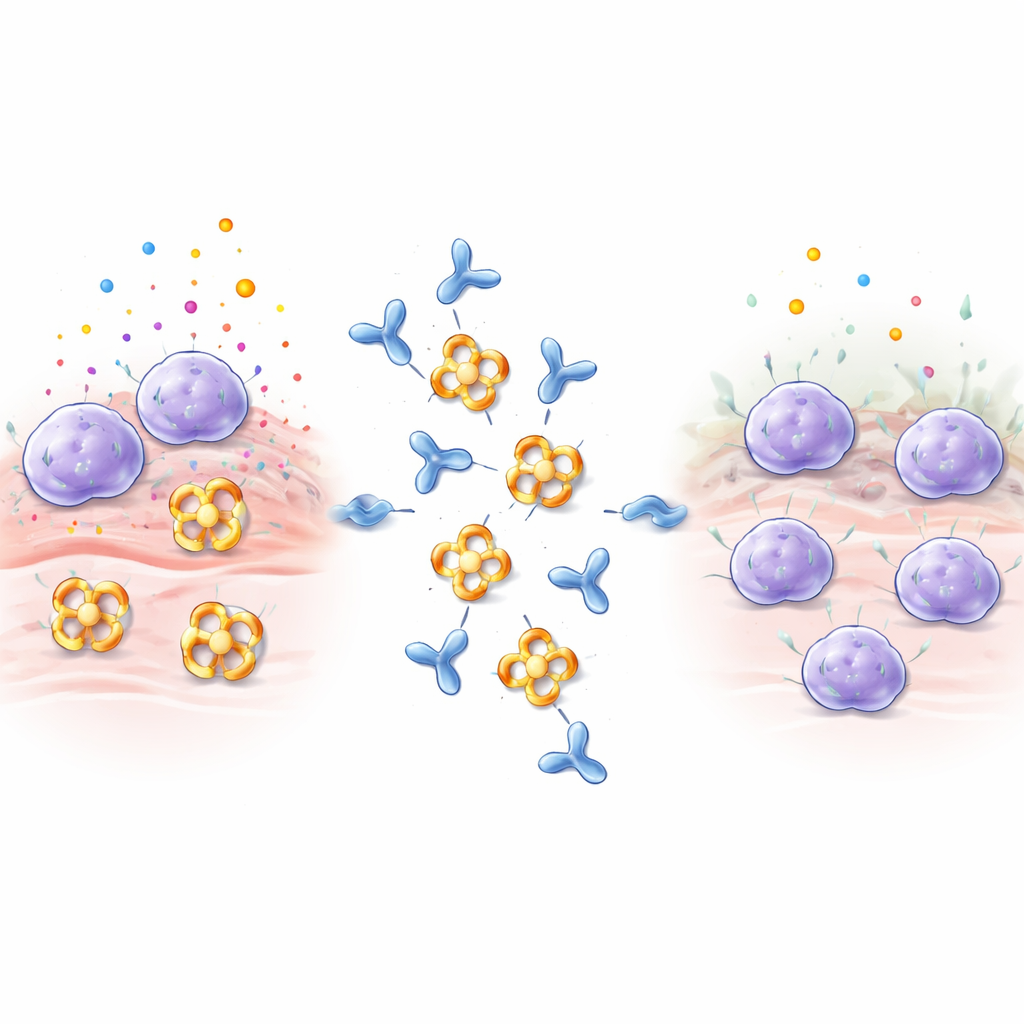
设计一种能关闭酶活性的抗体
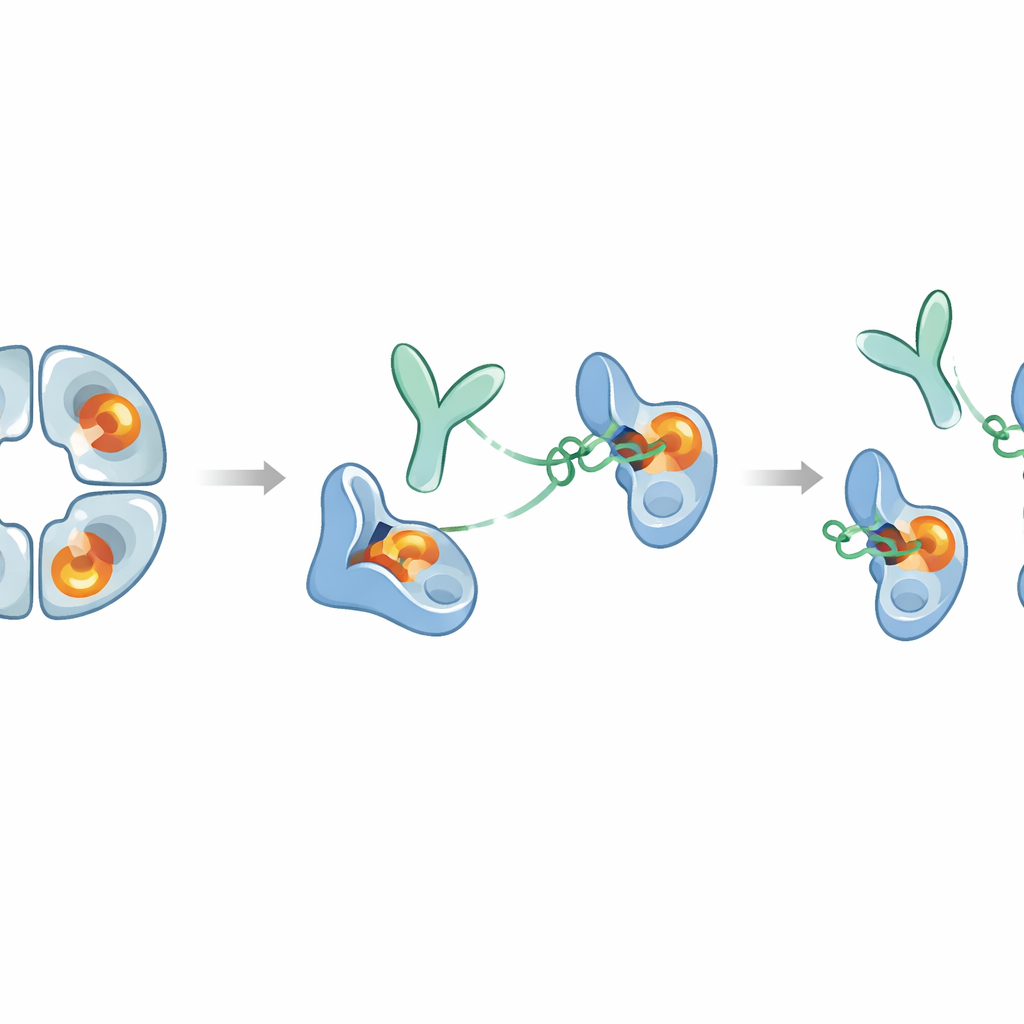
研究人员用人体β‑胰蛋白酶免疫兔子并筛选所得抗体,重点关注一种称为E82.AS的抗体。与先前仅能部分失活酶的抗体不同,E82.AS即便在通常能强烈保持活性的条件下也能抑制β‑胰蛋白酶活性。详细的结合实验显示,全长抗体及其较小片段(Fab)都能紧密结合β‑胰蛋白酶,并呈剂量依赖性抑制。当团队将E82.AS与该四聚体酶混合并通过分离柱时,观察到四聚体解体为与抗体共同迁移的单体,表明E82.AS迫使环状结构解散为单体。
远端抓取触发关闭开关
为理解E82.AS如何如此有效地发挥作用,科学家使用了氢‑氘交换测量和高分辨率冷冻电子显微镜。这些方法揭示该抗体并不与酶的中央孔或催化凹槽结合。相反,它抓住了表面上的一个补片——一个“外位点”,距离化学切割中心相当远。然而,这一远端抓握触发了一连串通过酶的柔性环传递到活性位点的构象变化。在抗体结合的构型中,那些通常稳定切割反应的关键结构特征,例如容纳反应键的小口袋和吸引碱性氨基酸的关键负电荷,被扭曲或移位。因此,活性位点无法再容纳天然蛋白底物或体积较大的蛋白类抑制剂。
单一原子级微调的威力
最引人注目的发现之一是,抗体中单个氨基酸的改变就能将结合与功能解耦。团队在抗体轻链中改变了一个残基——将93位的天冬氨酸改为甘氨酸。这个微小修改几乎不减弱抗体与β‑胰蛋白酶的结合力,但却完全剥夺了其解离四聚体或阻断酶活性的能力。结构分析显示,原始的天冬氨酸侧链会推挤β‑胰蛋白酶的一个环,轻推邻近残基,并通过二硫键将这种形变传入活性位点核心。去除该侧链消除了这种机械推动力,因此尽管抗体存在,酶仍保持聚合并具有活性。相反,通过在重链两处增加正电荷,研究者增强了与酶上负电斑的静电吸引,从而将抑制效力提高了近五倍。
这对未来治疗可能意味着什么
总体来看,这项工作展示了一个罕见的例子:一种抗体通过牵拉远端位点而非堵塞活性中心,完全使一种难以成药的酶沉默。E82.AS既能撬开β‑胰蛋白酶四聚体,又能将每个单体锁定为“前酶样”的不活跃构型,即便在可增强活性的辅助分子肝素存在下亦然。鉴于仅抗体片段即可实现此效应,可能有望设计更小的变体以更好地到达发炎的气道。与此同时,β‑胰蛋白酶在调节免疫信号方面有有益作用,因此任何疗法都需在阻断有害过度活性和避免长期抑制有益功能之间取得平衡。本研究提供了该平衡的详细分子蓝图,并表明类似的变构策略可用于设计针对其他与人类疾病相关酶的高度选择性抑制剂。
引用: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
关键词: 肥大细胞, β-胰蛋白酶, 变构性抗体, 哮喘, 酶抑制