Clear Sky Science · it
Inibizione completa della β-triptasi mediante dissociazione del tetramero e allosteria del sito attivo dovute a una singola residua di un anticorpo
Perché è importante per allergie e asma
Le persone con asma, gravi allergie o anafilassi spesso soffrono perché alcune cellule immunitarie nei tessuti rilasciano potenti sostanze che restringono le vie aeree e danneggiano i tessuti. Uno dei colpevoli principali è un enzima chiamato beta‑triptasi, immagazzinato nei mastociti e rilasciato durante le reazioni allergiche. Questo studio descrive un anticorpo appositamente ingegnerizzato che può spegnere completamente la beta‑triptasi in modo nuovo, aprendo potenzialmente la strada a terapie migliori per le malattie guidate dai mastociti.
Il perturbatore all'interno dei mastociti
I mastociti stazionano come sentinelle in tessuti quali polmoni, intestino e pelle. Quando rilevano allergeni, veleni o microbi, rilasciano rapidamente pacchetti pieni di istamina, proteine segnale ed enzimi. La beta‑triptasi è l’enzima più abbondante di questi e contribuisce al restringimento delle vie aeree, alla produzione extra di collagene e alla contrazione della muscolatura nei polmoni, tutti fattori che peggiorano asma e altre malattie infiammatorie. La beta‑triptasi normalmente si assembla in un anello a quattro subunità, o tetramero, i cui siti attivi sono rivolti verso un poro centrale. Questa architettura nasconde i centri attivi dalla maggior parte degli inibitori naturali presenti nell’organismo, rendendo la beta‑triptasi particolarmente difficile da bloccare con farmaci convenzionali.
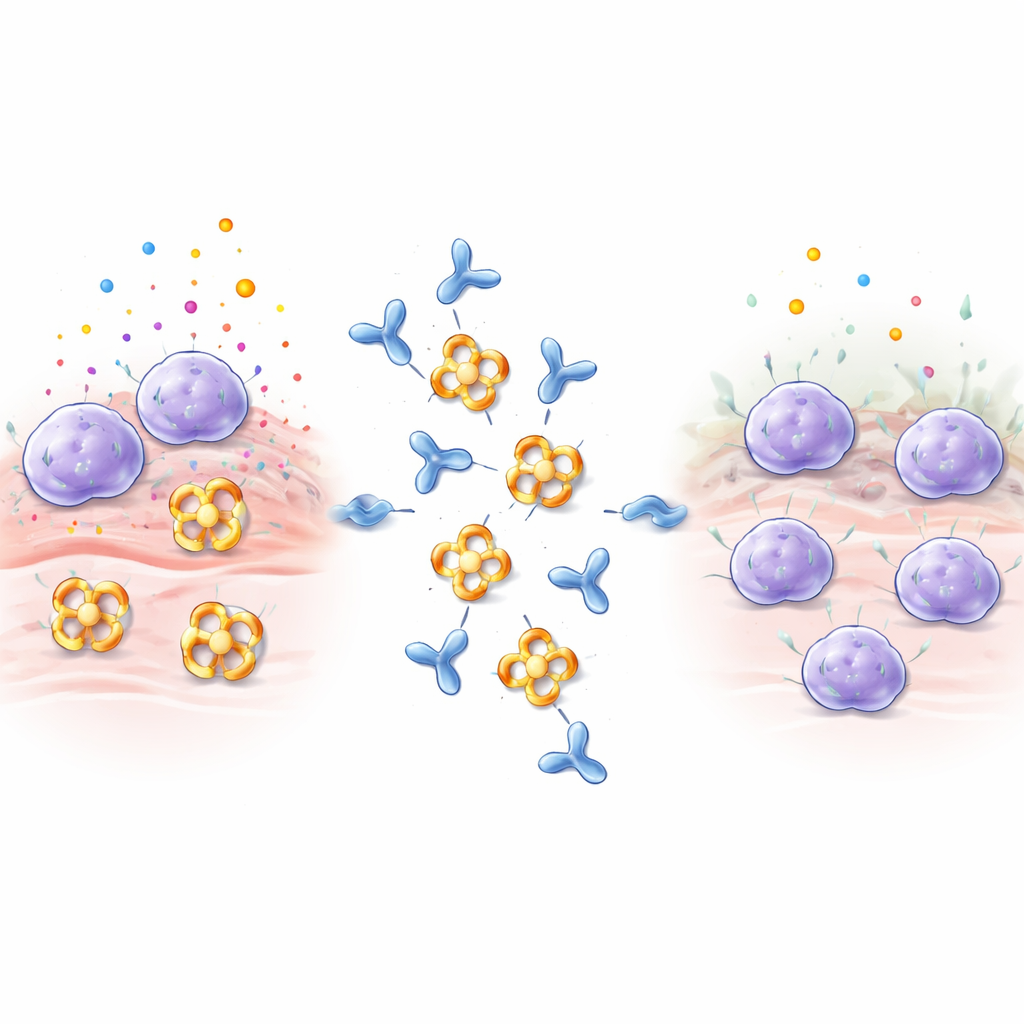
Progettare un anticorpo che spegne l'enzima
I ricercatori hanno immunizzato conigli con beta‑triptasi umana e hanno scremato gli anticorpi ottenuti, concentrandosi su uno chiamato E82.AS. A differenza di anticorpi precedenti che disattivavano solo parzialmente l’enzima, E82.AS è in grado di sopprimere l’attività della beta‑triptasi anche in condizioni che solitamente la mantengono fortemente attiva. Test dettagliati di legame hanno mostrato che sia l’anticorpo a lunghezza intera sia il suo frammento più piccolo (Fab) si legano alla beta‑triptasi con elevata affinità e la inibiscono in modo dipendente dalla dose. Quando il team ha miscelato E82.AS con l’enzima a quattro subunità e lo ha fatto passare attraverso colonne di separazione, ha osservato che il tetramero si disfava in unità singole che viaggiavano insieme all’anticorpo, indicando che E82.AS forza l’anello a smontarsi in monomeri.
Una presa distante che aziona l'interruttore di spegnimento
Per capire come E82.AS agisca con tale efficacia, gli scienziati hanno utilizzato misure di scambio idrogeno‑deuterio e microscopia crio‑elettronica ad alta risoluzione. Questi approcci hanno rivelato che l’anticorpo non si lega nel poro centrale o nella gola catalitica dell’enzima. Invece, afferra una patch sulla superficie — un “esosite” — piuttosto distante dal centro chimico di taglio. Eppure questa presa remota innesca una cascata di cambiamenti conformazionali che si propagano attraverso anse flessibili dell’enzima fino al sito attivo stesso. Nella forma legata all’anticorpo, caratteristiche strutturali critiche che normalmente stabilizzano la reazione di taglio, come una piccola tasca che ospita il legame reattivo e una carica negativa chiave che attira amminoacidi basici, risultano distorte o spostate. Di conseguenza, il sito attivo non può più accogliere né i substrati proteici naturali né inibitori proteici voluminosi.
La potenza di una singola modifica a livello atomico
Una delle scoperte più sorprendenti è che una singola variazione di amminoacido nell’anticorpo può disaccoppiare il legame dalla funzione. Il team ha modificato una residua nella catena leggera dell’anticorpo — cambiando un aspartato in glicina alla posizione 93. Questa minima modifica ha appena indebolito l’affinità di legame dell’anticorpo per la beta‑triptasi, ma ha completamente abolito la sua capacità di dissociare il tetramero o bloccare l’attività enzimatica. L’analisi strutturale mostra che la catena laterale dell’aspartato originale spinge contro un’ansa nella beta‑triptasi, spostando una residua vicina e, attraverso un ponte disolfuro, trasmettendo la distorsione nel cuore del sito attivo. La rimozione di quella catena laterale elimina la spinta meccanica, così l’enzima rimane assemblato e attivo nonostante la presenza dell’anticorpo. Al contrario, aggiungendo cariche positive in due posizioni nella catena pesante, i ricercatori hanno rafforzato l’attrazione elettrostatica verso una patch caricata negativamente sull’enzima e migliorato la potenza inibitoria fino a quasi cinque volte.
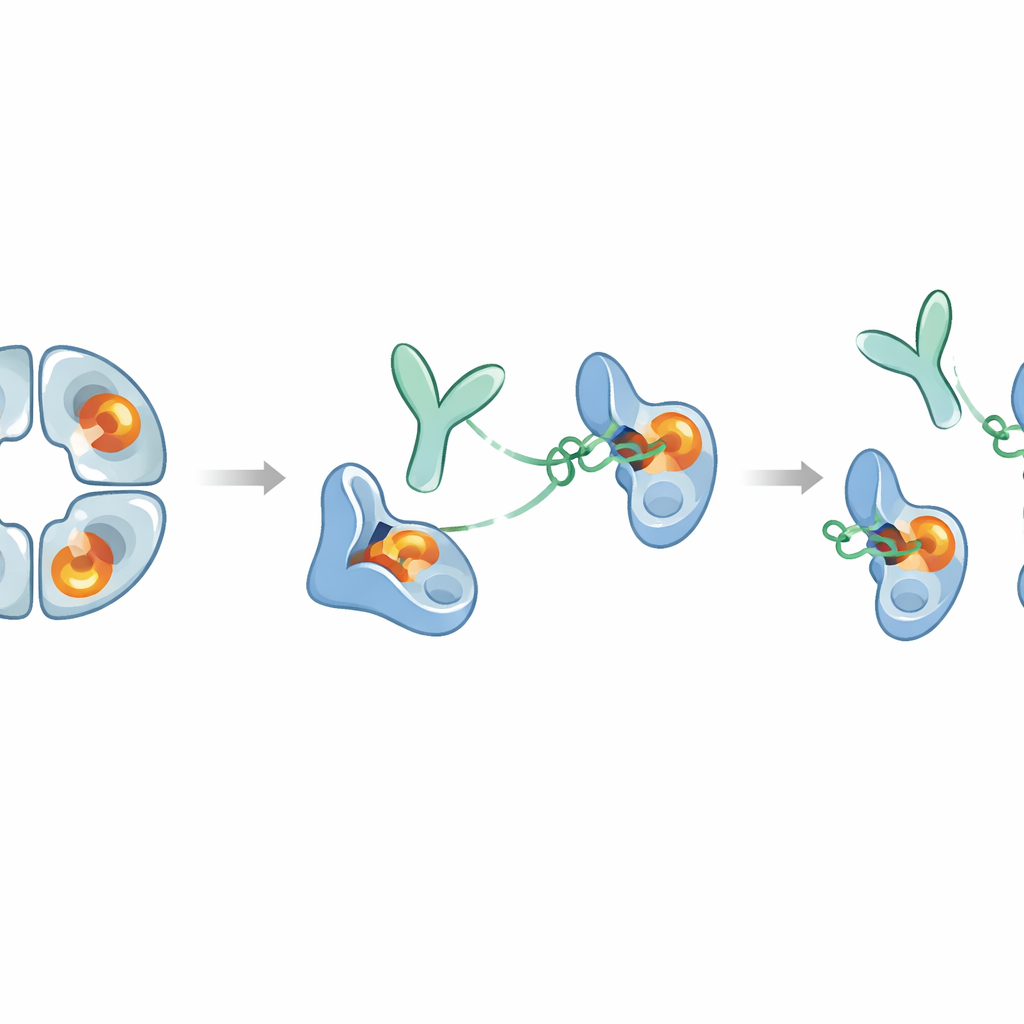
Cosa potrebbe significare per terapie future
Nel complesso, il lavoro rivela un raro esempio di anticorpo che silenzia completamente un enzima difficile da colpire farmacologicamente tirando su un sito remoto invece di tappare il centro attivo. E82.AS sia scardina il tetramero della beta‑triptasi sia blocca ogni monomero in una forma inattiva “simile a uno zimogeno”, anche quando una molecola ausiliaria chiamata eparina è presente per aumentare l’attività. Poiché il frammento dell’anticorpo da solo può ottenere questo effetto, potrebbe essere possibile progettare versioni più piccole meglio adatte a raggiungere le vie aeree infiammate. Allo stesso tempo, la beta‑triptasi ha ruoli benefici nella regolazione dei segnali immunitari, quindi qualunque terapia dovrà bilanciare il blocco dell’eccessiva attività dannosa senza sopprimere troppo a lungo le funzioni utili. Questo studio offre un progetto molecolare dettagliato per tale bilanciamento e suggerisce che strategie allosteriche simili potrebbero essere usate per progettare inibitori altamente selettivi per altri enzimi coinvolti nelle malattie umane.
Citazione: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
Parole chiave: mastociti, beta-triptasi, anticorpo allosterico, asma, inibizione enzimatica