Clear Sky Science · tr
Tek bir antikor kalitesinin tetramer ayrışması ve aktif bölge allosteri yoluyla β-triptazın tam inhibisyonu
Alerji ve astım açısından neden önemli
Astım, şiddetli alerjiler veya anafilaksi yaşayan kişiler, dokulardaki belirli bağışıklık hücrelerinin hava yollarını daraltan ve dokuya zarar veren güçlü kimyasallar salması nedeniyle sıkıntı yaşar. Başlıca suçlulardan biri, mast hücrelerinde depolanan ve alerjik reaksiyonlar sırasında açığa çıkan beta‑triptaz adlı bir enzimdir. Bu çalışma, beta‑triptazı yeni bir yolla tamamen kapatabilen özel olarak tasarlanmış bir antikoru tanımlıyor; bu da mast hücre kaynaklı hastalıklar için daha iyi tedavilere kapı aralayabilir.
Mast hücrelerinin içindeki sorun yaratan
Mast hücreleri, akciğerler, bağırsak ve deri gibi dokularda bekçi olarak bulunur. Alerjenleri, zehirleri veya mikropları algıladıklarında, histamin, sinyal proteinleri ve enzimler içeren kesecikleri hızla boşaltırlar. Beta‑triptaz bu enzimlerin en bol olanıdır ve hava yollarının daralması, artmış kollajen üretimi ve akciğerlerde kas kasılması gibi süreçleri tetikleyerek astım ve diğer iltihabi hastalıkları kötüleştirir. Beta‑triptaz genellikle aktif bölgelerinin merkezi bir gözüke doğru baktığı dört parçalı bir halka, yani tetramer halinde toplanır. Bu yapı, aktif merkezleri vücuttaki çoğu doğal inhibitörden gizleyerek beta‑triptazı konvansiyonel ilaçlarla engellemeyi özellikle zorlaştırır.
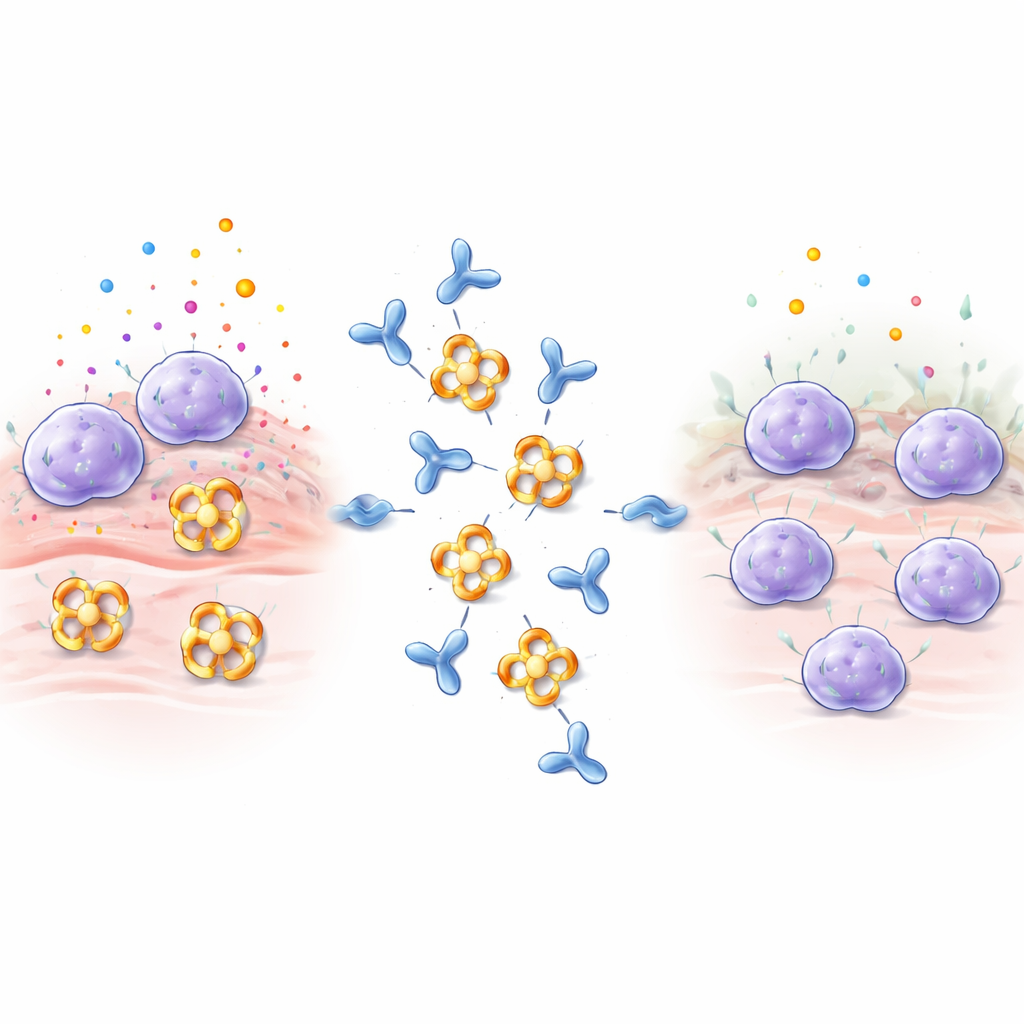
Enzimi kapatan bir antikor tasarlamak
Araştırmacılar insan beta‑triptaz ile tavşanları immünize etti ve ortaya çıkan antikorları tarayarak E82.AS adındaki bir antikora odaklandı. Sadece kısmen etkisizleştiren önceki antikorlardan farklı olarak, E82.AS genellikle güçlü biçimde aktif tuttuğu koşullar altında bile beta‑triptaz aktivitesini baskılayabildi. Ayrıntılı bağlanma testleri, hem tam uzunluktaki antikorun hem de daha küçük parçacığı (Fab) nın beta‑triptazla çok sıkı bağlandığını ve doz bağımlı olarak inhibe ettiğini gösterdi. Ekip E82.AS ile dört parçalı enzimi karıştırıp ayırma kolonlarından geçirdiğinde, tetramerin tek birimlere ayrılarak antikorla birlikte hareket ettiğini gördü; bu da E82.AS'nin halkayı monomerlere ayrılmaya zorladığını gösteriyor.
Uzak bir tutuşun kapatma düğmesini çevirmesi
E82.AS'nin neden bu kadar etkili çalıştığını anlamak için bilim insanları hidrojen–döteryum değişim ölçümleri ve yüksek çözünürlüklü kriyo‑elektron mikroskopi kullandı. Bu yaklaşımlar antikorun enzimin merkezi gözükenine veya katalitik oluğuna bağlanmadığını ortaya koydu. Bunun yerine, enzim yüzeyinde — aktif kesimden oldukça uzakta — bir yamayı, bir “eksitopl”u kavrıyor. Yine de bu uzak tutuş, esnek döngüler aracılığıyla aktif bölgeye ulaşan bir dizi şekil değişikliğini tetikliyor. Antikor bağlandığında, reaksiyonu normalde stabilize eden küçük reaksiyon cebini ve bazik aminoasitleri çeken anahtar negatif yük gibi kritik yapısal özellikler bozuluyor veya yer değiştiriyor. Sonuç olarak, aktif bölge artık ne doğal protein substratlarını ne de hacimli protein‑temelli inhibitörleri kabul edebiliyor.
Tek bir atom düzeyinde ayarın gücü
En çarpıcı bulgulardan biri, antikordaki tek bir amino asit değişikliğinin bağlanmayı işlevden ayırabilmesi oldu. Ekip, antikorun hafif zincirinde bir rezidüyü değiştirerek 93. pozisyondaki bir aspartatı glisine çevirdi. Bu küçük değişiklik antikorun beta‑triptaza ne kadar iyi bağlandığını yalnızca biraz zayıflatsa da, tetrameri parçalama veya enzimatik aktiviteyi engelleme yeteneğini tamamen ortadan kaldırdı. Yapısal analiz, orijinal aspartat yan zincirinin beta‑triptazdaki bir döngüye bastırdığını, yakındaki bir rezidüyü iterek ve bir disülfit bağı yoluyla bu bozulmayı aktif bölgenin merkezine ilettiğini gösteriyor. Bu yan zincirin kaldırılması mekanik itişi ortadan kaldırıyor, böylece antikorun varlığına rağmen enzim birleşik ve aktif kalıyor. Buna karşılık, ağır zincirdeki iki pozisyona pozitif yükler ekleyerek araştırmacılar enzimin negatif yüklü bir yamasına elektrostatik çekimi güçlendirdiler ve inhibe edici etkiyi neredeyse beş kata kadar artırdılar.
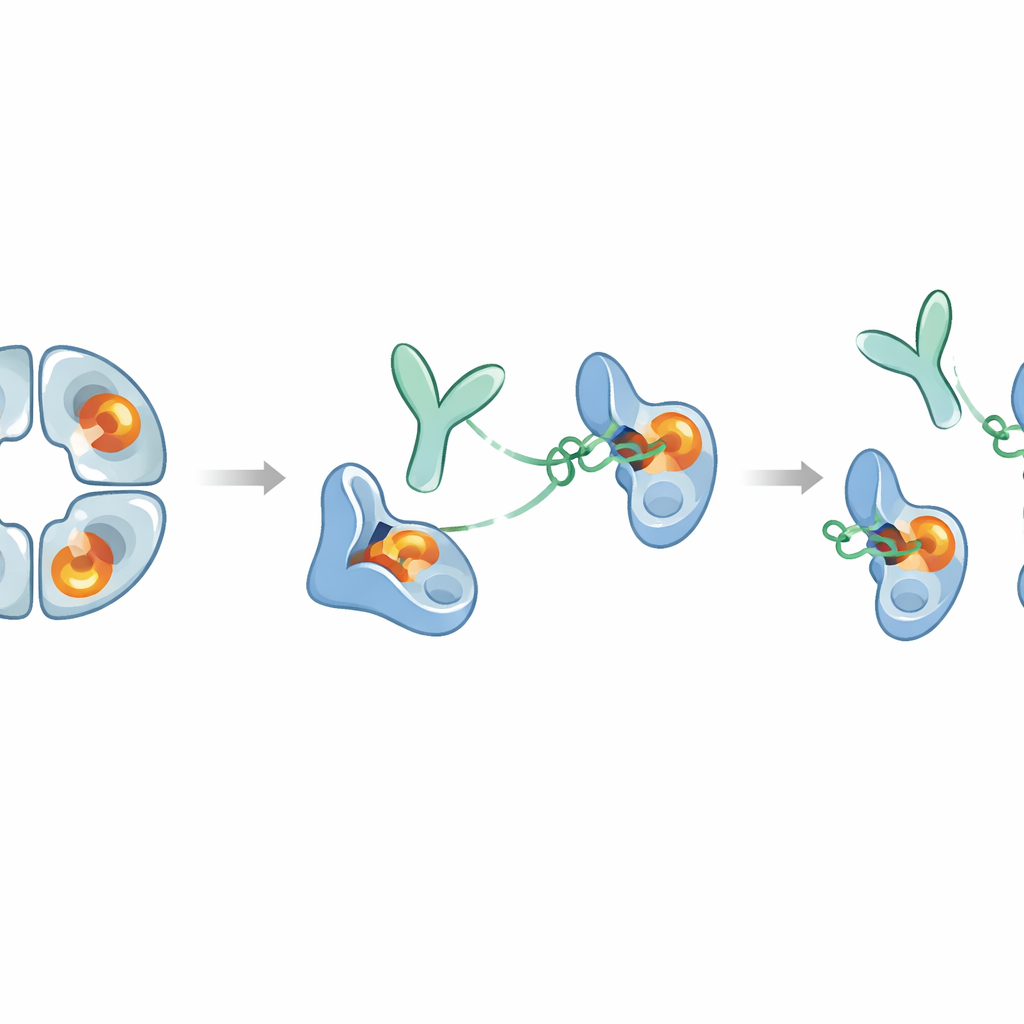
Gelecekteki tedaviler için olası çıkarımlar
Bir araya getirildiğinde, bu çalışma aktif merkezi tıkamaktansa uzak bir bölgeyi çekerek ilaç geliştirmesi zor bir enzimi tamamen sessize alan nadir bir antikor örneğini ortaya koyuyor. E82.AS hem beta‑triptaz tetramerini ayırıyor hem de her monomeri heparin gibi aktiviteyi artıran yardımcı bir molekülün varlığında bile “zimogen‑benzeri” inaktif bir şekle kilitliyor. Antikor fragmentinin tek başına bunu yapabilmesi, iltihaplı hava yollarına ulaşmaya daha uygun daha küçük versiyonların tasarlanmasının mümkün olabileceğini gösteriyor. Aynı zamanda beta‑triptazın bağışıklık sinyallerini düzenlemede faydalı rolleri olduğundan, herhangi bir tedavi zararlı aşırı aktiviteleri engellerken faydalı işlevleri çok uzun süre baskılamamak üzere dengelenmelidir. Bu çalışma bu denge için ayrıntılı bir moleküler şablon sunuyor ve benzer allosterik stratejilerin insan hastalıklarında rol oynayan diğer enzimler için son derece seçici inhibitörler tasarlamada kullanılabileceğini öne sürüyor.
Atıf: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
Anahtar kelimeler: mast hücreleri, beta-triptaz, allosterik antikor, astım, enzim inhibisyonu