Clear Sky Science · pt
Inibição completa da β-triptase por dissociação do tetrâmero e alosteria do sítio ativo devido a um único resíduo de anticorpo
Por que isso importa para alergias e asma
Pessoas com asma, alergias graves ou anafilaxia frequentemente sofrem porque certas células imunes nos tecidos liberam substâncias potentes que contraem as vias aéreas e danificam os tecidos. Um dos culpados principais é uma enzima chamada beta‑triptase, armazenada em mastócitos e liberada durante reações alérgicas. Este estudo descreve um anticorpo especialmente projetado que pode desligar completamente a beta‑triptase de uma nova forma, potencialmente abrindo caminho para tratamentos melhores de doenças mediadas por mastócitos.
O causador dentro dos mastócitos
Os mastócitos atuam como sentinelas em tecidos como pulmões, intestino e pele. Quando detectam alérgenos, venenos ou micróbios, liberam rapidamente grânulos cheios de histamina, proteínas sinalizadoras e enzimas. A beta‑triptase é a mais abundante dessas enzimas e contribui para o estreitamento das vias aéreas, aumento da produção de colágeno e contração muscular nos pulmões, todos fatores que pioram a asma e outras doenças inflamatórias. A beta‑triptase normalmente se monta em um anel de quatro partes, ou tetrâmero, cujos sítios ativos apontam para um poro central. Essa arquitetura oculta os centros ativos da maioria dos inibidores naturais do organismo, tornando a beta‑triptase especialmente difícil de bloquear com fármacos convencionais.
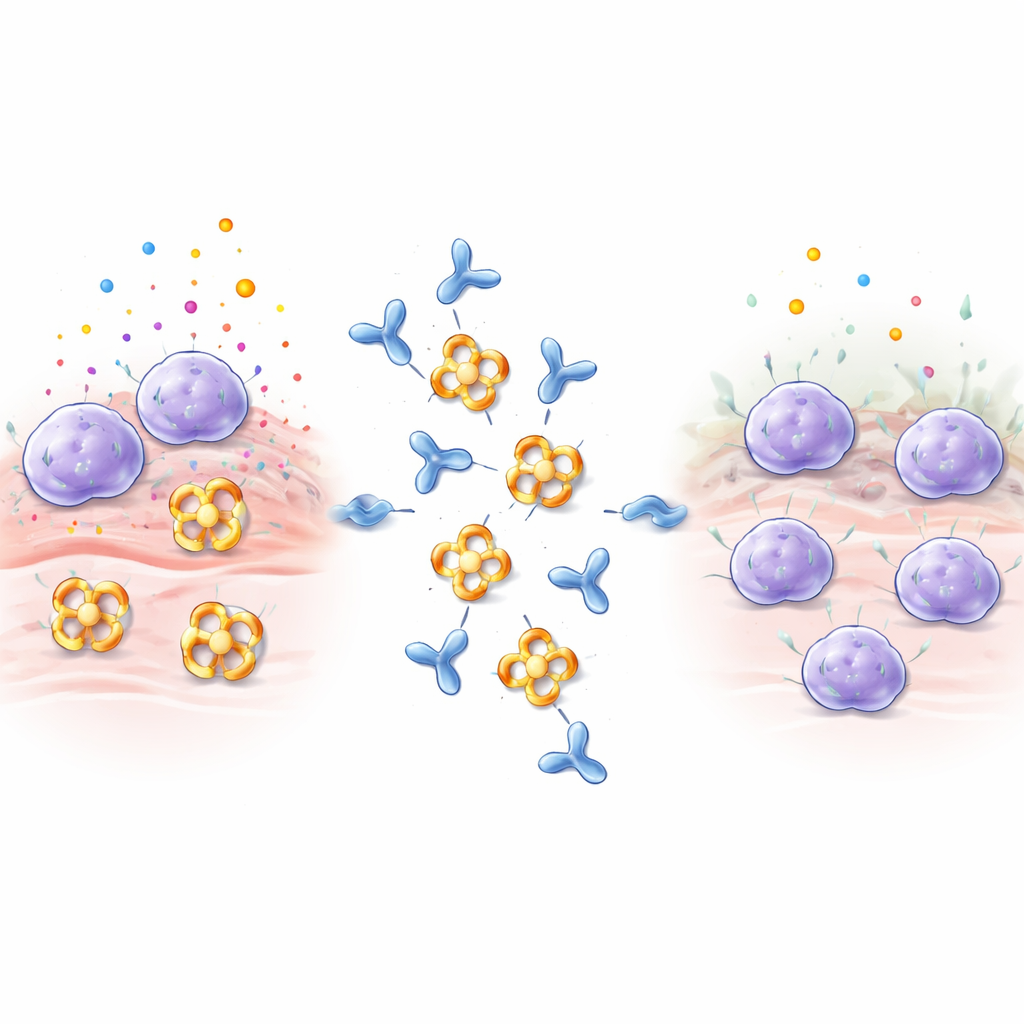
Projetando um anticorpo que desliga a enzima
Os pesquisadores imunizaram coelhos com beta‑triptase humana e triaram os anticorpos resultantes, focando em um chamado E82.AS. Ao contrário de anticorpos anteriores que apenas desativavam a enzima parcialmente, E82.AS pôde suprimir a atividade da beta‑triptase mesmo em condições que normalmente a mantêm fortemente ativa. Testes detalhados de ligação mostraram que tanto o anticorpo de comprimento total quanto seu fragmento menor (Fab) se ligam fortemente à beta‑triptase e a inibem de maneira dependente da dose. Quando a equipe misturou E82.AS com a enzima tetramérica e a passou por colunas de separação, observaram que o tetrâmero se desfazia em unidades simples que viajaram juntamente com o anticorpo, indicando que E82.AS força o anel a se romper em monômeros.
Uma pegada distante que aciona o botão de desligar
Para entender como E82.AS atua com tanta eficiência, os cientistas usaram medidas de troca hidrogênio‑deutério e criomicroscopia eletrônica de alta resolução. Essas abordagens revelaram que o anticorpo não se liga ao poro central da enzima nem à fenda catalítica. Em vez disso, ele agarra uma mancha na superfície — um “exosite” — bastante distante do centro químico de clivagem. Ainda assim, essa pegada remota desencadeia uma cascata de mudanças de forma que se propagam por loops flexíveis da enzima até o próprio sítio ativo. Na forma ligada ao anticorpo, características estruturais críticas que normalmente estabilizam a reação de clivagem, como um pequeno bolso que acomoda a ligação reativa e uma carga negativa chave que atrai aminoácidos básicos, ficam distorcidas ou deslocadas. Como resultado, o sítio ativo deixa de acomodar tanto substratos proteicos naturais quanto inibidores proteicos volumosos.
O poder de uma única modificação ao nível atômico
Uma das descobertas mais marcantes é que uma única mudança de aminoácido no anticorpo pode desacoplar ligação de função. A equipe alterou um resíduo na cadeia leve do anticorpo — trocando um ácido aspártico por glicina na posição 93. Essa modificação minúscula quase não enfraqueceu a afinidade do anticorpo pela beta‑triptase, mas aboliu completamente sua capacidade de dissociar o tetrâmero ou bloquear a atividade enzimática. Análise estrutural mostra que a cadeia lateral do aspártico original empurra contra um loop na beta‑triptase, deslocando um resíduo próximo e, por meio de uma ligação dissulfeto, transmitindo a distorção para o coração do sítio ativo. Remover essa cadeia lateral elimina o impulso mecânico, de modo que a enzima permanece montada e ativa apesar da presença do anticorpo. Por outro lado, ao adicionar cargas positivas em duas posições da cadeia pesada, os pesquisadores reforçaram a atração eletrostática por uma região negativamente carregada da enzima e melhoraram a potência inibitória em quase cinco vezes.
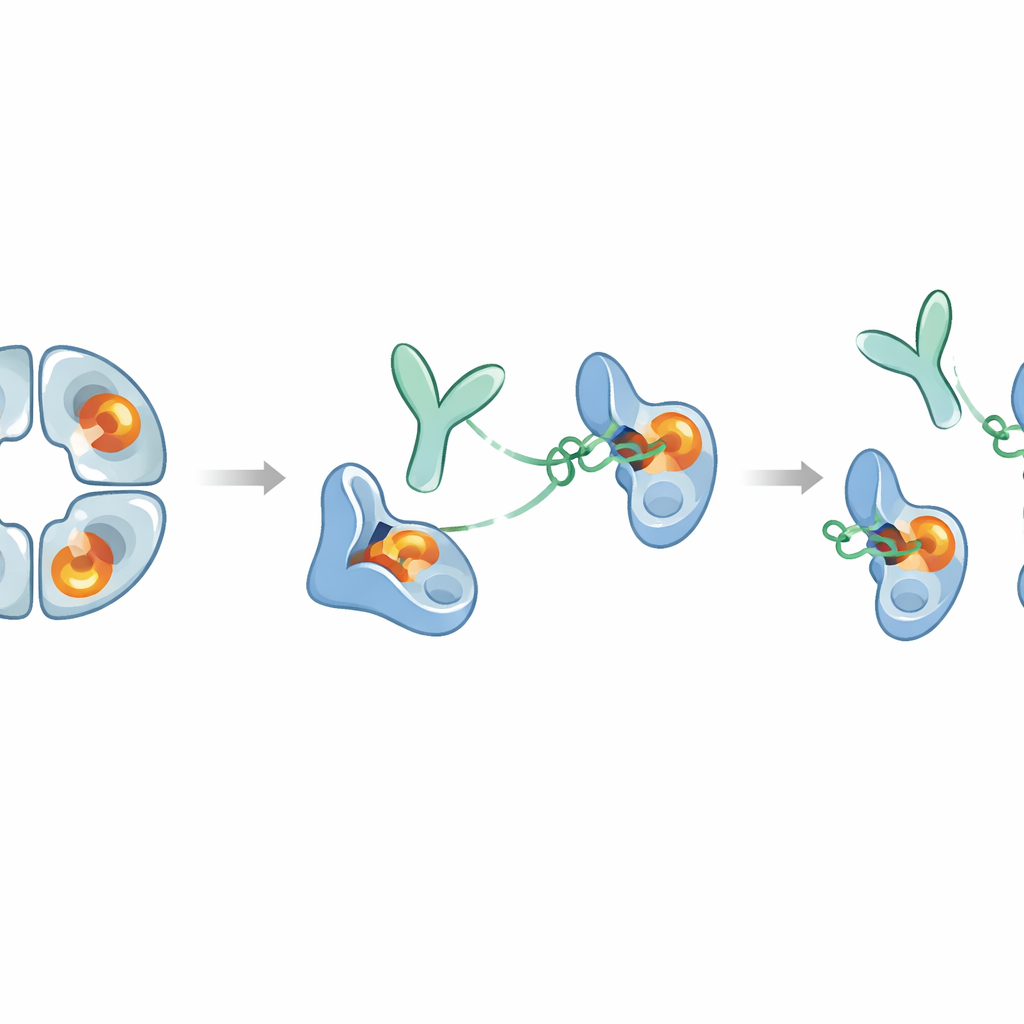
O que isso pode significar para tratamentos futuros
Em conjunto, o trabalho revela um exemplo raro de anticorpo que silencia completamente uma enzima difícil de drugar ao puxar um sítio remoto em vez de tamponar o centro ativo. E82.AS tanto desdobra o tetrâmero de beta‑triptase quanto trava cada monômero em uma conformação inativa “semelhante a zimógeno”, mesmo quando uma molécula auxiliar chamada heparina está presente para aumentar a atividade. Como o fragmento do anticorpo por si só pode fazer isso, pode ser possível projetar versões menores mais adequadas para alcançar vias aéreas inflamadas. Ao mesmo tempo, a beta‑triptase tem papéis benéficos na regulação de sinais imunes, de modo que qualquer terapia precisará equilibrar o bloqueio de uma atividade prejudicial exagerada sem suprimir funções úteis por tempo excessivo. Este estudo oferece um roteiro molecular detalhado para esse equilíbrio e sugere que estratégias alostéricas semelhantes poderiam ser usadas para projetar inibidores altamente seletivos para outras enzimas envolvidas em doenças humanas.
Citação: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
Palavras-chave: células mastocitárias, beta-triptase, anticorpo alostérico, asma, inibição enzimática