Clear Sky Science · sv
Fullständig hämning av β-tryptas genom tetramerdissociation och allosteri i det aktiva sätet orsakad av en enda antikroppsrest
Varför detta är viktigt för allergier och astma
Personer med astma, svåra allergier eller anafylaxi har ofta problem eftersom vissa immunceller i vävnaderna frigör kraftfulla kemikalier som drar ihop luftvägarna och skadar vävnad. En av huvudboven är ett enzym kallat beta‑tryptas, som lagras i mastceller och frigörs vid allergiska reaktioner. Denna studie beskriver en specialkonstruerad antikropp som kan slå av beta‑tryptas fullständigt på ett nytt sätt, vilket potentiellt öppnar dörren för bättre behandlingar av sjukdomar drivna av mastceller.
Problembäraren inne i mastcellerna
Mastceller fungerar som vakter i vävnader som lungor, tarm och hud. När de känner av allergener, gifter eller mikrober tömmer de snabbt ut paket fyllda med histamin, signalmolekyler och enzymer. Beta‑tryptas är det mest rikliga av dessa enzymer och bidrar till luftvägsförträngning, ökad kollagenproduktion och muskelsammandragning i lungorna, vilket förvärrar astma och andra inflammatoriska sjukdomar. Beta‑tryptas bildar normalt en ring av fyra delar, ett tetramer, där de aktiva ytorna pekar in mot en central por. Denna arkitektur döljer de aktiva centra för de flesta naturliga hämmare i kroppen, vilket gör beta‑tryptas särskilt svårt att blockera med konventionella läkemedel.
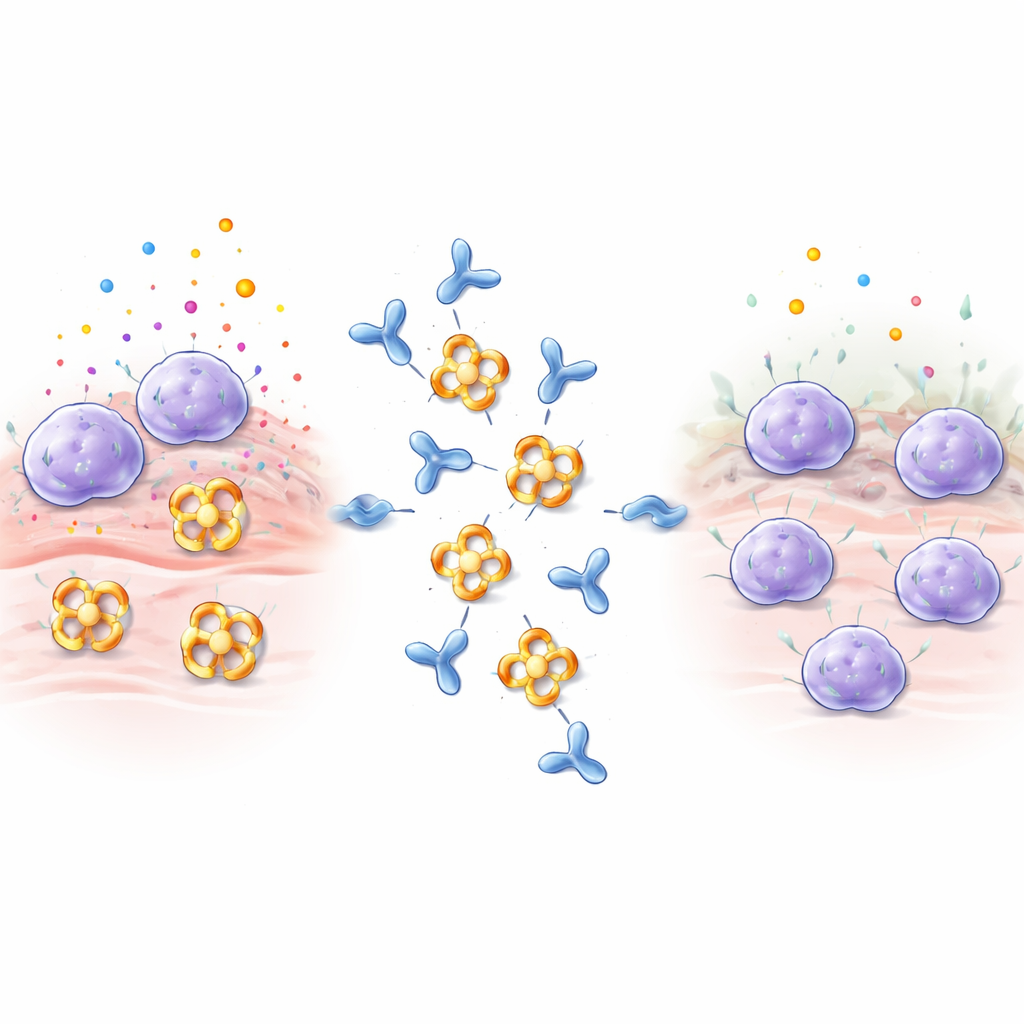
Att designa en antikropp som stänger ner enzymet
Forskarna immuniserade kaniner med human beta‑tryptas och screenade de framkomna antikropparna, med fokus på en som kallades E82.AS. Till skillnad från tidigare antikroppar som bara delvis inaktiverade enzymet kunde E82.AS undertrycka beta‑tryptasaktivitet även under förhållanden som normalt håller det starkt aktivt. Detaljerade bindningstester visade att både hela antikroppen och dess mindre fragment (Fab) fäster mycket tätt till beta‑tryptas och hämmar det i dosberoende grad. När teamet blandade E82.AS med fyrdelarsenzymet och körde det genom separationskolonner såg de att tetramern föll isär till enheter som reste tillsammans med antikroppen, vilket indikerar att E82.AS tvingar ringen att dela upp sig i monomerer.
Ett avlägset grepp som vrider avstängningsknappen
För att förstå hur E82.AS fungerar så effektivt använde forskarna väte–deuterium‑utbyte och högupplöst kryoelektronmikroskopi. Dessa metoder visade att antikroppen inte binder i enzymets centrala por eller katalytiska spår. Istället griper den ett område på ytan—en så kallad exosite—ganska långt från det kemiska klyvningscentret. Ändå utlöser detta avlägsna grepp en kaskad av formförändringar som förs genom flexibla slingor i enzymet till det aktiva sätet. I den antikroppsbundna formen är kritiska strukturella element som normalt stabiliserar klyvningsreaktionen, såsom en liten ficka som håller den reagerande bindningen och en viktig negativ laddning som attraherar basiska aminosyror, förvrängda eller förflyttade. Som ett resultat kan det aktiva sätet inte längre rymma vare sig naturliga proteinsubstrat eller skrymmande proteinbaserade hämmare.
Kraften i ett enda atomnivå‑justerat steg
En av de mest påfallande fynden är att en enda aminosyraförändring i antikroppen kan koppla loss bindning från funktion. Teamet ändrade en rest i antikroppens lätta kedja—bytte en aspartat mot glycin vid position 93. Denna lilla modifiering försvagade knappt hur väl antikroppen band till beta‑tryptas, men den eliminerade helt dess förmåga att dela upp tetramern eller blockera enzymaktiviteten. Strukturanalys visar att den ursprungliga aspartatsidokedjan pressar mot en slinga i beta‑tryptas, knuffar en närliggande rest och, genom en disulfidbindning, överför förvrängningen in i det aktiva sätets kärna. Att ta bort den sidokedjan eliminerar den mekaniska knuffen, så enzymet förblir sammanfogat och aktivt trots antikroppens närvaro. Motsatt förbättrade forskarna den inhibitoriska potentialen nästan femfaldigt genom att lägga till positiva laddningar på två positioner i den tunga kedjan, vilket stärkte elektrostatisk attraktion till en negativt laddad yta på enzymet.
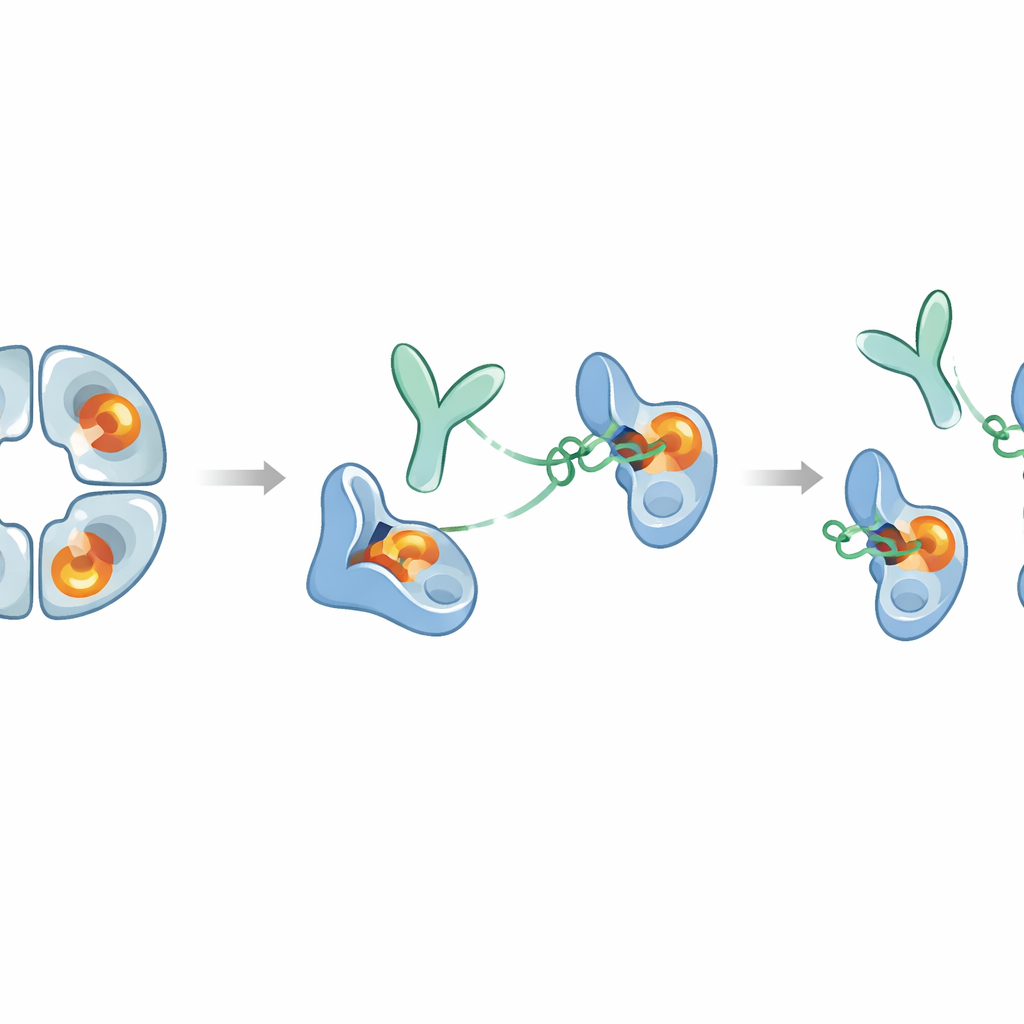
Vad detta kan betyda för framtida behandlingar
Sammantaget visar arbetet ett sällsynt exempel på en antikropp som fullständigt tystar ett svårt‑att‑läkemedelsätt enzym genom att dra i en avlägsen yta istället för att stoppa det aktiva centret. E82.AS både bryter isär beta‑tryptas‑tetramern och låser varje monomer i en zymogenliknande inaktiv form, även när en hjälpande molekyl kallad heparin är närvarande och ökar aktiviteten. Eftersom antikroppsfragmentet ensamt kan åstadkomma detta kan det vara möjligt att designa mindre varianter bättre lämpade att nå inflammerade luftvägar. Samtidigt har beta‑tryptas fördelaktiga roller i reglering av immunsignaler, så eventuell terapi måste balansera att blockera skadlig överaktivitet utan att undertrycka nyttiga funktioner för länge. Denna studie erbjuder en detaljerad molekylär ritning för den balansen och antyder att liknande allosteriska strategier kan användas för att designa högselektiva hämmare för andra enzymer involverade i mänsklig sjukdom.
Citering: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
Nyckelord: mastceller, beta-tryptas, allosterisk antikropp, astma, enzymhämning