Clear Sky Science · de
Vollständige Hemmung von β-Tryptase durch Tetramer-Dissoziation und Allosterie der aktiven Stelle aufgrund einer einzelnen Antikörper-Restgruppe
Warum das für Allergien und Asthma wichtig ist
Menschen mit Asthma, schweren Allergien oder Anaphylaxie haben häufig Probleme, weil bestimmte Immunzellen in ihrem Gewebe starke Substanzen freisetzen, die die Atemwege verengen und Gewebe schädigen. Einer der wichtigsten Täter ist ein Enzym namens Beta‑Tryptase, das in Mastzellen gespeichert ist und während allergischer Reaktionen freigesetzt wird. Diese Studie beschreibt einen speziell entwickelten Antikörper, der Beta‑Tryptase auf eine neue Weise vollständig ausschalten kann und damit möglicherweise den Weg für bessere Therapien gegen mastzellgetriebene Erkrankungen öffnet.
Der Übeltäter in den Mastzellen
Mastzellen liegen als Wächter in Geweben wie Lunge, Darm und Haut. Wenn sie Allergene, Gifte oder Mikroben wahrnehmen, entleeren sie schnell Vesikel, die Histamin, Signalproteine und Enzyme enthalten. Beta‑Tryptase ist das am stärksten vertretene dieser Enzyme und trägt zur Verengung der Atemwege, zu vermehrter Kollagenbildung und zur Muskelkontraktion in der Lunge bei – alles Faktoren, die Asthma und andere Entzündungskrankheiten verschlimmern. Beta‑Tryptase bildet normalerweise einen vierteiligen Ring, ein Tetramer, dessen aktive Zentren in eine zentrale Pore zeigen. Diese Architektur verbirgt die aktiven Zentren vor den meisten natürlichen Inhibitoren im Körper und macht Beta‑Tryptase besonders schwer mit konventionellen Wirkstoffen angreifbar.
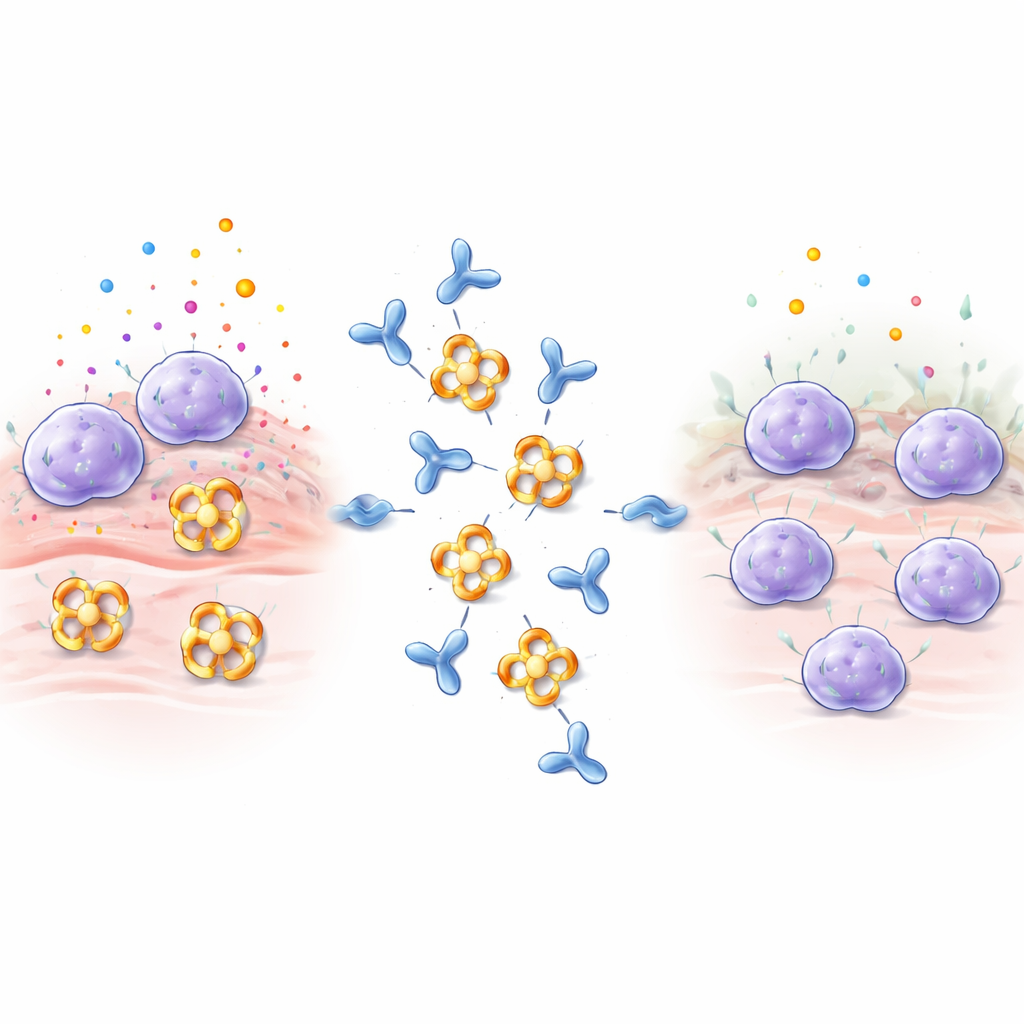
Entwurf eines Antikörpers, der das Enzym ausschaltet
Die Forschenden immunisierten Kaninchen mit humaner Beta‑Tryptase und screenten die resultierenden Antikörper, wobei sie sich auf einen mit der Bezeichnung E82.AS konzentrierten. Im Gegensatz zu früheren Antikörpern, die das Enzym nur teilweise deaktivierten, konnte E82.AS die Aktivität der Beta‑Tryptase selbst unter Bedingungen unterdrücken, die das Enzym normalerweise stark aktiv halten. Detaillierte Bindungstests zeigten, dass sowohl der vollständige Antikörper als auch sein kleineres Fragment (Fab) sehr fest an Beta‑Tryptase binden und diese dosisabhängig hemmen. Als das Team E82.AS mit dem vierteiligen Enzym mischte und durch Trennsäulen laufen ließ, beobachteten sie, dass das Tetramer in Einzeleinheiten zerfiel, die zusammen mit dem Antikörper wanderten – ein Hinweis darauf, dass E82.AS den Ring zur Dissoziation in Monomere zwingt.
Ein entfernter Griff, der den Ausschaltknopf betätigt
Um zu verstehen, wie E82.AS so effektiv wirkt, nutzten die Wissenschaftler Wasserstoff–Deuterium‑Austauschmessungen und hochauflösende Kryo‑Elektronenmikroskopie. Diese Methoden zeigten, dass der Antikörper nicht in die zentrale Pore oder die katalytische Grube des Enzyms bindet. Stattdessen greift er eine Fläche an der Oberfläche – ein sogenanntes „Exosite“ – relativ weit entfernt vom eigentlichen katalytischen Zentrum. Trotzdem löst dieser entfernte Griff eine Kaskade von Strukturveränderungen aus, die durch flexible Schleifen des Enzyms bis zur aktiven Stelle weitergeleitet werden. In der Antikörper‑gebundenen Form sind kritische strukturelle Merkmale, die normalerweise die Schnittreaktion stabilisieren – etwa eine kleine Tasche, die die reagierende Bindung hält, und eine wichtige negative Ladung, die basische Aminosäuren anzieht – verzerrt oder verschoben. Dadurch kann die aktive Stelle weder natürliche Protein‑Substrate noch sperrige proteinbasierte Inhibitoren aufnehmen.
Die Wirkung einer einzelnen atomaren Anpassung
Eines der auffälligsten Ergebnisse ist, dass schon eine einzige Aminosäureänderung im Antikörper Bindung und Funktion entkoppeln kann. Das Team veränderte einen Rest in der leichten Kette des Antikörpers – eine Aspartat‑ zu Glycin‑Substitution an Position 93. Diese winzige Modifikation schwächte die Bindungsstärke an Beta‑Tryptase nur minimal, zerstörte jedoch völlig die Fähigkeit, das Tetramer zu zerlegen oder die enzymatische Aktivität zu blockieren. Die Strukturanalyse zeigt, dass die ursprüngliche Aspartat‑Seitenkette gegen eine Schleife in der Beta‑Tryptase drückt, einen benachbarten Rest verschiebt und über eine Disulfidbindung die Verzerrung bis ins Zentrum der aktiven Stelle überträgt. Entfernt man diese Seitenkette, entfällt den mechanischen Druck, sodass das Enzym trotz Anwesenheit des Antikörpers zusammengebaut und aktiv bleibt. Umgekehrt verstärkten die Forschenden durch das Einfügen positiver Ladungen an zwei Stellen der schweren Kette die elektrostatische Anziehung zu einem negativ geladenen Bereich des Enzyms und erhöhten so die hemmende Potenz um fast das Fünffache.
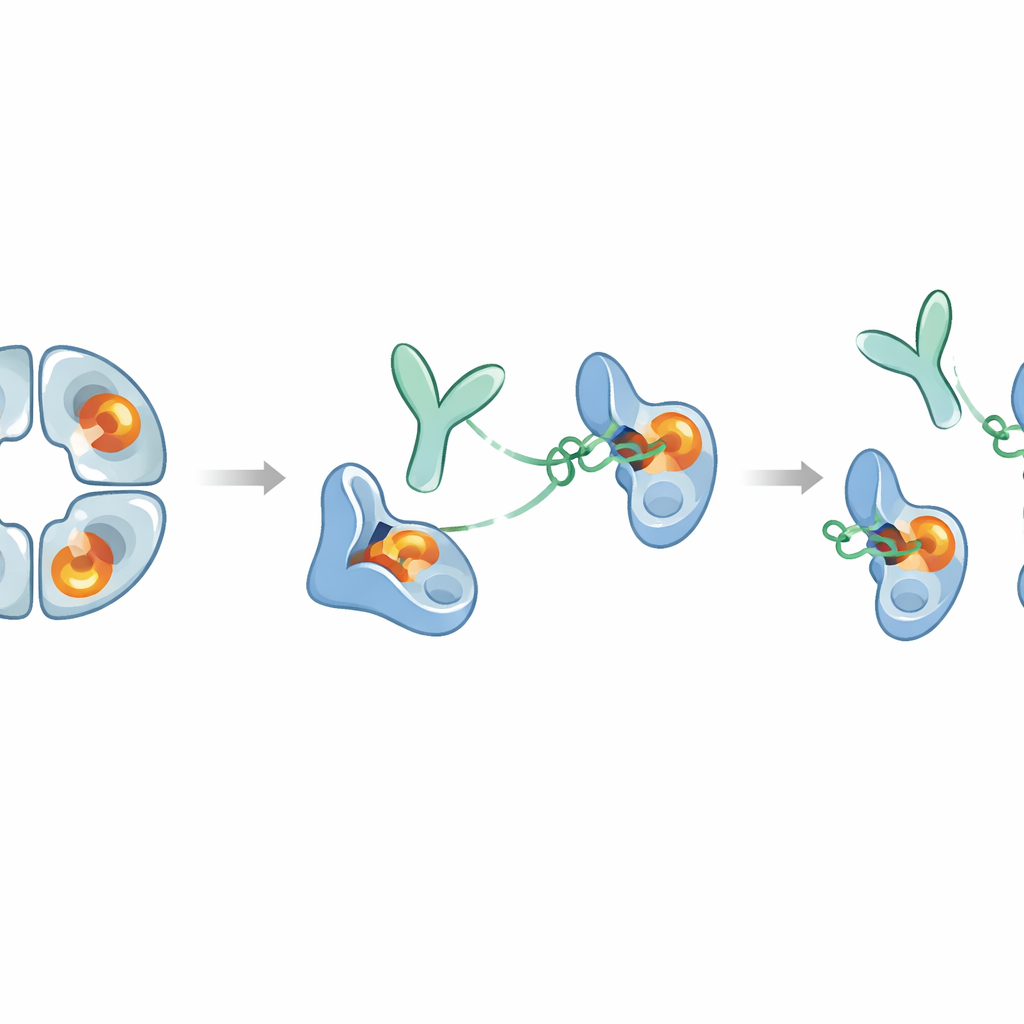
Wie sich das auf künftige Therapien auswirken könnte
In der Summe zeigt die Arbeit ein seltenes Beispiel für einen Antikörper, der ein schwer angreifbares Enzym vollständig stummschaltet, indem er an einer entfernten Stelle zieht, anstatt das aktive Zentrum zu blockieren. E82.AS trennt das Beta‑Tryptase‑Tetramer auseinander und sperrt jedes Monomer in eine „Zymogen‑ähnliche“ inaktive Gestalt, selbst wenn ein Helfermolekül wie Heparin die Aktivität verstärkt. Da bereits das Antikörperfragment dies bewirken kann, könnte es möglich sein, kleinere Versionen zu entwerfen, die besser geeignet sind, entzündete Atemwege zu erreichen. Gleichzeitig erfüllt Beta‑Tryptase nützliche Funktionen bei der Regulation immuner Signale, sodass jede Therapie das schädliche Übermaß an Aktivität dämpfen muss, ohne nützliche Funktionen zu lange zu unterdrücken. Diese Studie liefert einen detaillierten molekularen Bauplan für dieses Gleichgewicht und legt nahe, dass ähnliche allosterische Strategien genutzt werden könnten, um hochselektive Inhibitoren gegen andere an menschlichen Krankheiten beteiligte Enzyme zu entwickeln.
Zitation: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
Schlüsselwörter: Mastzellen, Beta-Tryptase, allosterischer Antikörper, Asthma, Enzymhemmung