Clear Sky Science · pl
Całkowita inhibicja β-tryptazy poprzez dysocjację tetrameru i allosterię miejsca czynnego wywołana pojedynczym resztem przeciwciała
Dlaczego to ma znaczenie dla alergii i astmy
Osoby z astmą, ciężkimi alergiami lub anafilaksją często mają problemy, ponieważ niektóre komórki układu odpornościowego w tkankach uwalniają silne związki, które zwężają drogi oddechowe i uszkadzają tkanki. Jednym z głównych sprawców jest enzym zwany beta‑tryptazą, magazynowany w komórkach tucznych i uwalniany podczas reakcji alergicznych. W tym badaniu opisano specjalnie zaprojektowane przeciwciało, które potrafi całkowicie wyłączyć beta‑tryptazę w nowy sposób, co potencjalnie otwiera drogę do lepszych terapii chorób związanych z aktywnością komórek tucznych.
Sprawca wewnątrz komórek tucznych
Komórki tuczne pełnią funkcję strażników w tkankach takich jak płuca, jelita i skóra. Gdy wykryją alergeny, jad żmii lub drobnoustroje, szybko uwalniają pęcherzyki zawierające histaminę, białka sygnalizacyjne i enzymy. Beta‑tryptaza jest najobficiej występującym z tych enzymów i przyczynia się do zwężania dróg oddechowych, nadmiernej produkcji kolagenu i skurczu mięśni w płucach — wszystkie te procesy pogarszają astmę i inne choroby zapalne. Beta‑tryptaza zwykle składa się w czteroczęściowy pierścień, tetramer, którego miejsca aktywne skierowane są do centralnego kanału. Ta architektura ukrywa centra czynne przed większością naturalnych inhibitorów w organizmie, co sprawia, że beta‑tryptaza jest szczególnie trudna do zablokowania tradycyjnymi lekami.
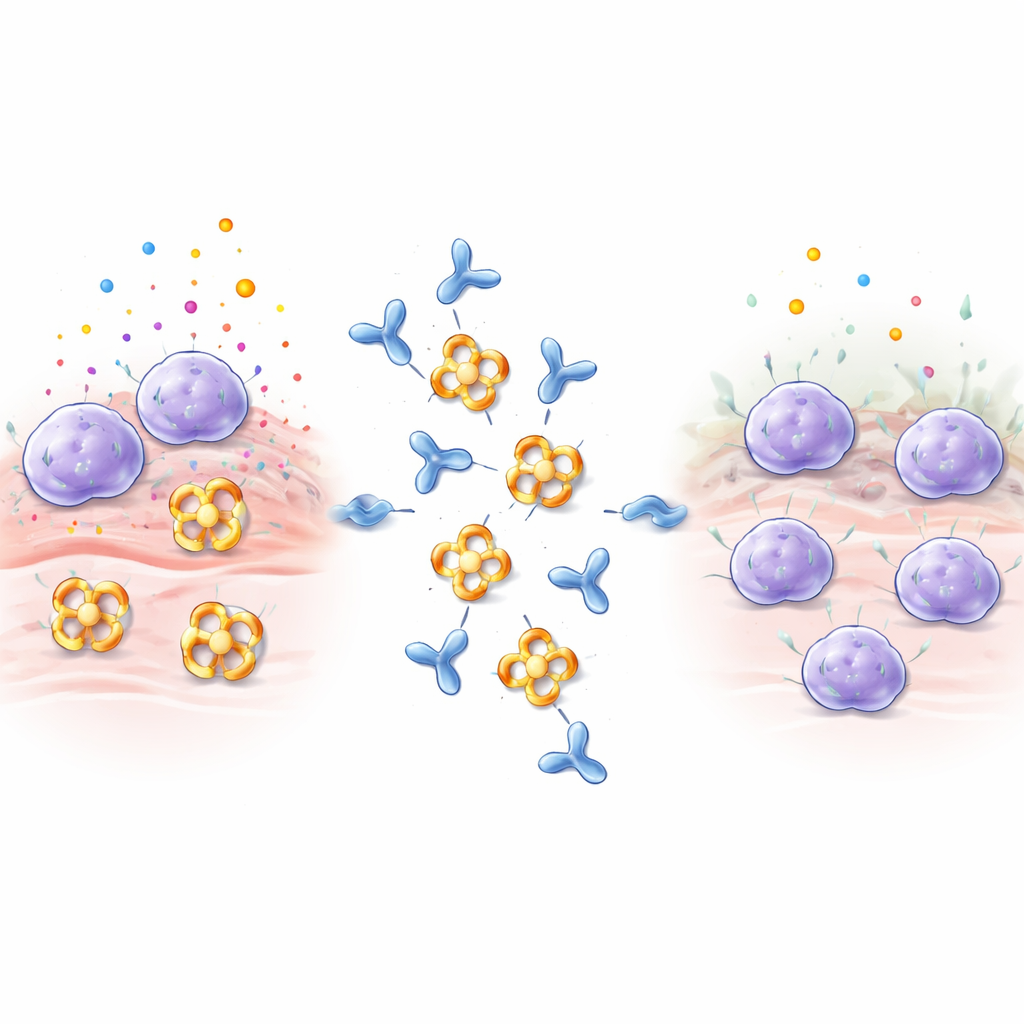
Projektowanie przeciwciała, które wyłącza enzym
Naukowcy imunizowali króliki ludzką beta‑tryptazą i przeanalizowali powstałe przeciwciała, skupiając się na jednym oznaczonym E82.AS. W przeciwieństwie do wcześniejszych przeciwciał, które jedynie częściowo hamowały enzym, E82.AS potrafiła tłumić aktywność beta‑tryptazy nawet w warunkach, które zwykle utrzymują ją w silnie aktywnej formie. Szczegółowe testy wiązania wykazały, że zarówno pełnej długości przeciwciało, jak i jego mniejszy fragment (Fab) wiążą się z beta‑tryptazą bardzo ściśle i hamują ją w zależności od dawki. Gdy zespół zmieszał E82.AS z czteroczęściowym enzymem i przepuścił próbkę przez kolumny separacyjne, zaobserwowano, że tetramer rozpada się na pojedyncze jednostki, które współtowarzyszą przeciwciału, co wskazuje, że E82.AS wymusza rozpad pierścienia na monomery.
Distantny chwyt, który przełącza wyłącznik
Aby zrozumieć, jak E82.AS działa tak efektywnie, badacze użyli pomiarów wymiany wodór–deuter i wysokorozdzielczej krio‑mikroskopii elektronowej. Podejścia te ujawniły, że przeciwciało nie wiąże się w centralnym kanale enzymu ani w bruzdzie katalitycznej. Zamiast tego chwyta fragment na powierzchni — „egzosit” — dość daleko od chemicznego centrum tnącego. Tym niemniej ten odległy chwyt wywołuje kaskadę zmian konformacyjnych przenoszących się przez elastyczne pętle enzymu do samego miejsca aktywnego. W formie związanej z przeciwciałem krytyczne elementy strukturalne, które normalnie stabilizują reakcję cięcia, takie jak mała kieszeń mieszcząca reagujące wiązanie oraz kluczowy ujemny ładunek przyciągający zasadowe aminokwasy, są zniekształcone lub przesunięte. W rezultacie miejsce aktywne nie może już przyjmować ani naturalnych substratów białkowych, ani masywnych inhibitorów białkowych.
Moc pojedynczej modyfikacji na poziomie atomowym
Jednym z najbardziej uderzających odkryć jest to, że pojedyncza zmiana aminokwasu w przeciwciele może rozdzielić wiązanie od funkcji. Zespół zmienił jeden resztę w łańcuchu lekkim przeciwciała — zastępując asparaginian glicyną na pozycji 93. Ta drobna modyfikacja ledwo osłabiła siłę wiązania przeciwciała z beta‑tryptazą, ale całkowicie zniszczyła jego zdolność do rozpadu tetrameru lub blokowania aktywności enzymatycznej. Analiza strukturalna pokazuje, że pierwotny łańcuch boczny asparaginianu naciska na pętlę w beta‑tryptazie, popychając pobliską resztę i przez wiązanie disiarczkowe przekazując zniekształcenie do centrum miejsca aktywnego. Usunięcie tego łańcucha bocznego eliminuje mechaniczny nacisk, więc enzym pozostaje złożony i aktywny pomimo obecności przeciwciała. Natomiast poprzez dodanie ładunków dodatnich w dwóch pozycjach w łańcuchu ciężkim badacze wzmocnili przyciąganie elektrostatyczne do ujemnie naładowanej plamy na enzymie i poprawili moc hamującą niemal pięciokrotnie.
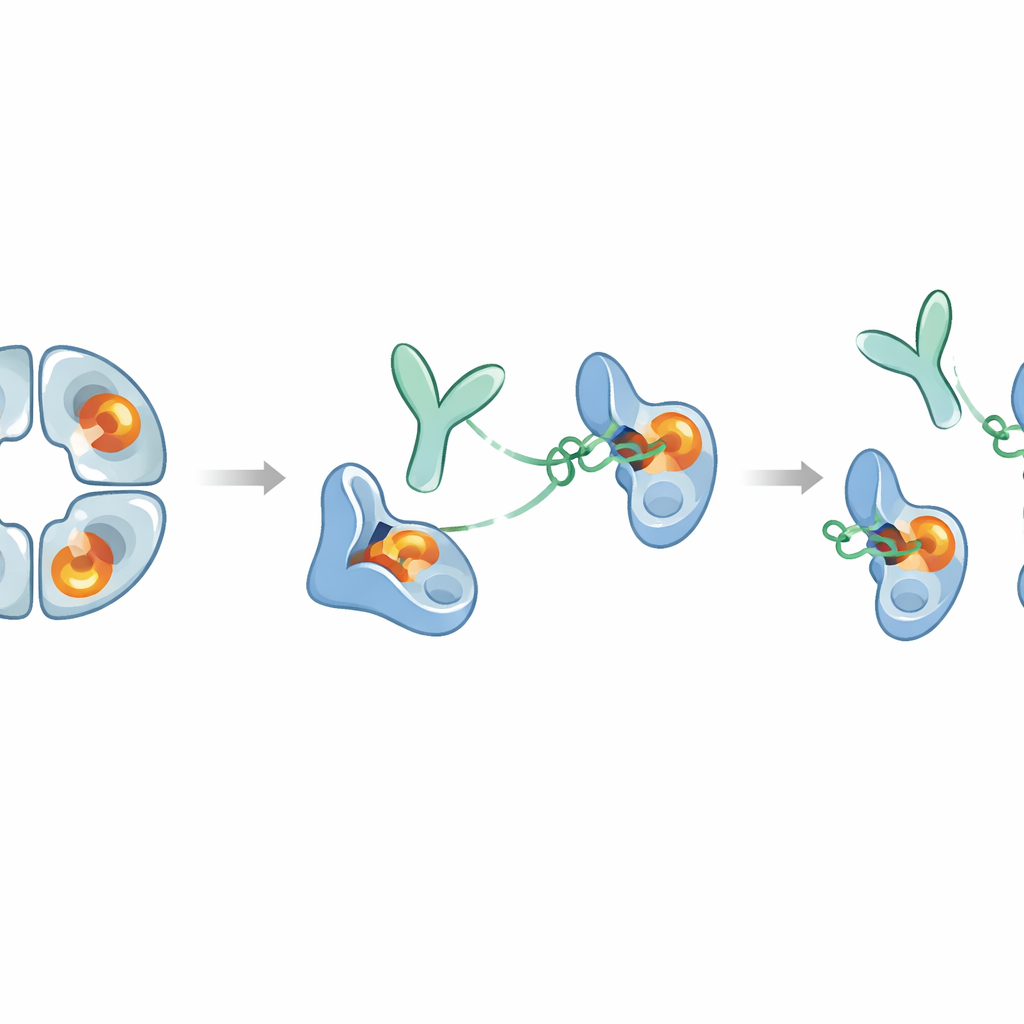
Co to może oznaczać dla przyszłych terapii
Podsumowując, praca ujawnia rzadki przykład przeciwciała, które całkowicie wycisza trudny do zaadresowania enzym, ciągnąc za odległe miejsce zamiast zatykać centrum aktywne. E82.AS zarówno rozbija tetramer beta‑tryptazy, jak i blokuje każdy monomer w „zymogenopodobnej” nieaktywnej konformacji, nawet gdy obecna jest heparyna — cząsteczka wspomagająca aktywność. Ponieważ sam fragment przeciwciała potrafi to osiągnąć, możliwe może być zaprojektowanie mniejszych wersji lepiej nadających się do dotarcia do zapalnych dróg oddechowych. Jednocześnie beta‑tryptaza pełni pożyteczne role w regulacji sygnałów immunologicznych, więc każda terapia będzie musiała wyważć blokowanie szkodliwej nadaktywności bez nadmiernego tłumienia przydatnych funkcji. To badanie dostarcza szczegółowego, molekularnego planu takiego kompromisu i sugeruje, że podobne allosteryczne strategie można wykorzystać do zaprojektowania wysoce selektywnych inhibitorów dla innych enzymów zaangażowanych w choroby człowieka.
Cytowanie: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
Słowa kluczowe: komórki tuczne, beta-tryptaza, przeciwciało allosteryczne, astma, inhibicja enzymu