Clear Sky Science · he
עיכוב מוחלט של β‑טריפטאז על ידי פירוק הטטראמר ואלוסטריה של אתר הפעילות עקב חומצת אמינו אחת בנוגדן
מדוע זה חשוב לאלרגיות ולאסטמה
אנשים עם אסטמה, אלרגיות קשות או אנפילקסיס נתקלים לעתים קרובות בקשיים כי תאי מערכת החיסון ברקמות משחררים מולקולות חזקות שמצמצמות את דרכי הנשימה ופוגעות ברקמה. אחד האשמים המרכזיים הוא אנזים הנקרא בטא‑טריפטאז, המאוחסן בתאי מאסט ומשתחרר בזמן תגובות אלרגיות. המחקר מתאר נוגדן מהונדס שיכול לכבות את בטא‑טריפטאז באופן מלא בדרך חדשה, מה שעשוי לפתוח דלת לטיפולים משופרים במחלות המונעות על‑ידי תאי מאסט.
המעורר צרות בתוך תאי המאסט
תאי מאסט יושבים כשומרים ברקמות כמו הריאות, המעי והעור. כשזהים אלרגנים, ארס או מיקרובים, הם משחררים במהירות חבילות שמכילות היסטמין, חלבוני איתות ואנזימים. בטא‑טריפטאז הוא הנפוץ מבין האנזימים הללו ותורם להצרות דרכי הנשימה, לייצור מוגבר של קולגן ולהתכווצויות שריר בריאות — כל אלה מחמירים אסטמה ומחלות דלקתיות אחרות. בדרך כלל בטא‑טריפטאז מרכיב טבעת ארבע‑חלקית, או טטראמר, כאשר אתרי הפעילות פונים לפתח מרכזי. מבנה זה מסתיר את מרכזי הפעילות מרוב המעכבים הטבעיים בגוף, מה שהופך את בטא‑טריפטאז לקשה במיוחד לחסימה על‑ידי תרופות מסורתיות.
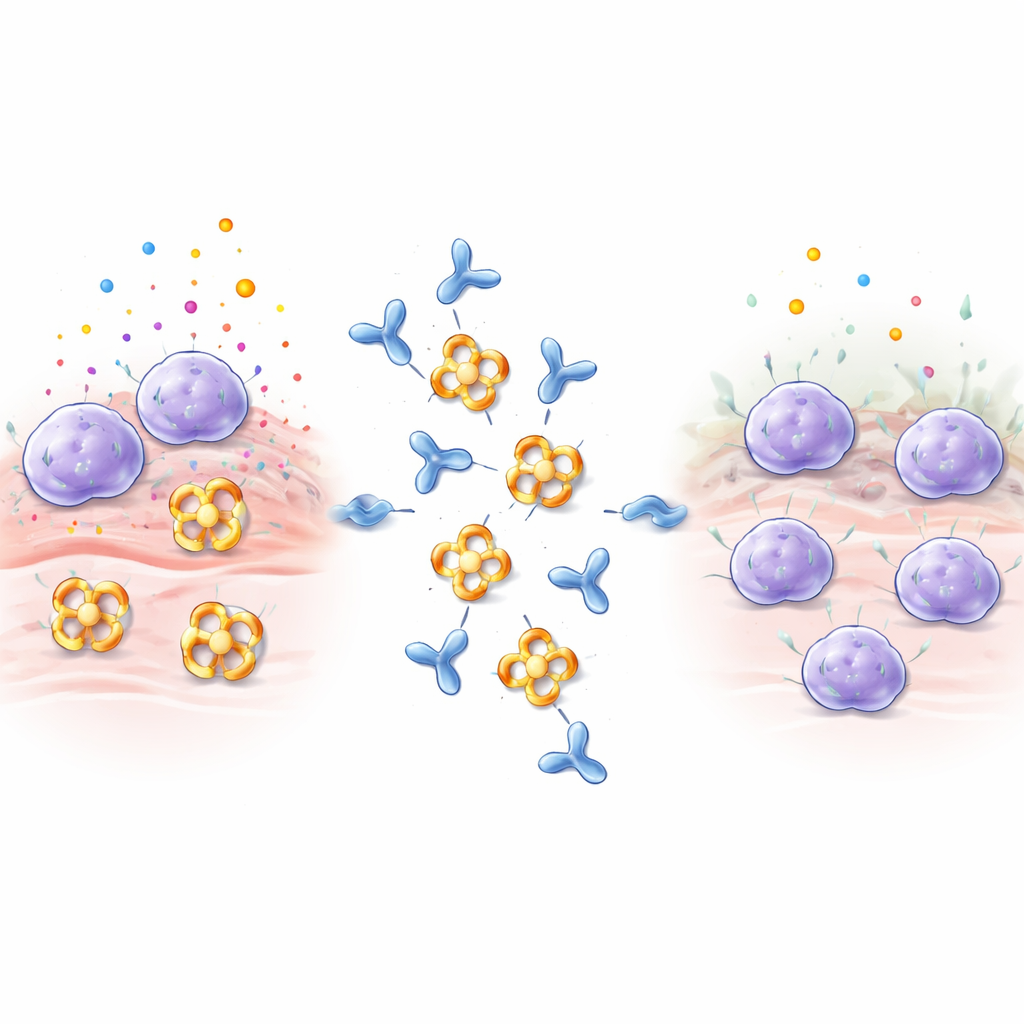
עיצוב נוגדן שמכבה את האנזים
החוקרים חיסנו ארנבות בבטא‑טריפטאז אנושי וסקרו את הנוגדנים שהתקבלו, עם התמקדות בנוגדן אחד שנקרא E82.AS. שלא כמו נוגדנים קודמים שנעו רק בהחלשת פעילות האנזים, E82.AS יכול לדכא את פעילות בטא‑טריפטאז גם בתנאים שבדרך כלל שומרים עליו פעיל מאוד. בדיקות קשירה מפורטות הראו שגם הנוגדן המלא וגם קטעו הקטן יותר (Fab) נקשרים לבטא‑טריפטאז בחוזקה ומעכבים אותו במינון‑תלוי. כשצוות החוקרים ערבב E82.AS עם האנזים הארבע‑חלקי ועבר בעמודות הפרדה, נצפה שהטטראמר נשבר ליחידות בודדות שנעו יחד עם הנוגדן, מה שמעיד כי E82.AS כופה על הטבעת להתפרק למונומרים.
תפיסה מרוחקת שמהפכת את מתג הכיבוי
כדי להבין מדוע E82.AS עובד ביעילות כה גדולה, השתמשו המדענים במדידות חילוף מימן‑דאוטריום ובמיקרוסקופיה אלקטרונית קריוגנית ברזולוציה גבוהה. שיטות אלה חשפו שהנוגדן אינו נקשר בפתח המרכזי של האנזים או בשקע הקטליטי. במקום זאת, הוא תופס מתחם על המשטח — "אתר חוץ" — רחוק יחסית ממרכז החיתוך הכימי. עם זאת, תפיסה מרוחקת זו גורמת לשרשרת של שינויים מבניים שנמשכות דרך לולאות גמישות של האנזים אל תוך אתר הפעילות עצמו. במצב המקובע על‑ידי הנוגדן, תכונות מבניות קריטיות שמייצבות בדרך כלל את תגובת החיתוך, כמו כיס קטן שמחזיק את הקשר המגיב וטעינה שלילית מרכזית שמושכת חומצות אמינו בסיסיות, מעוותות או זזות. כתוצאה מכך אתר הפעילות אינו יכול עוד להכיל את המצעונים החלבוניים הטבעיים או את המעכבים החלבוניים המגושמים.
כוחה של התאמה יחידה ברמת האטום
אחת הממצאים המפתיעים ביותר היא ששינוי של חומצת אמינו אחת בנוגדן יכול לנתק את הקשירה מהפונקציה. הצוות שינה שייר אחד בשרשרת הקלה של הנוגדן — החלפת אספרטט בגליצין במיקום 93. שינוי זעיר זה החליש בקושי את מידת קשירת הנוגדן לבטא‑טריפטאז, אך ביטל לחלוטין את יכולתו לפרק את הטטראמר או לחסום את הפעילות האנזימטית. ניתוח מבני מראה כי צד הציד של האספרטט המקורי דוחף כנגד לולאה בבטא‑טריפטאז, דוחף שייר סמוך ובאמצעות קשר דיסולפידי שמעביר את העיוות אל לב אתר הפעילות. הסרת שרשרת הצד הזו מבטלת את הדחיפה המכנית, כך שהאנזים נשאר מורכב ופעיל למרות נוכחות הנוגדן. מנגד, על‑ידי הוספת מטענים חיוביים בשתי עמדות בשרשרת הכבדה, החוקרים חיזקו את המשיכה האלקטרוסטטית למכתש טעון שלילית באנזים ושיפרו את עוצמת העיכוב עד כמעט פי חמש.
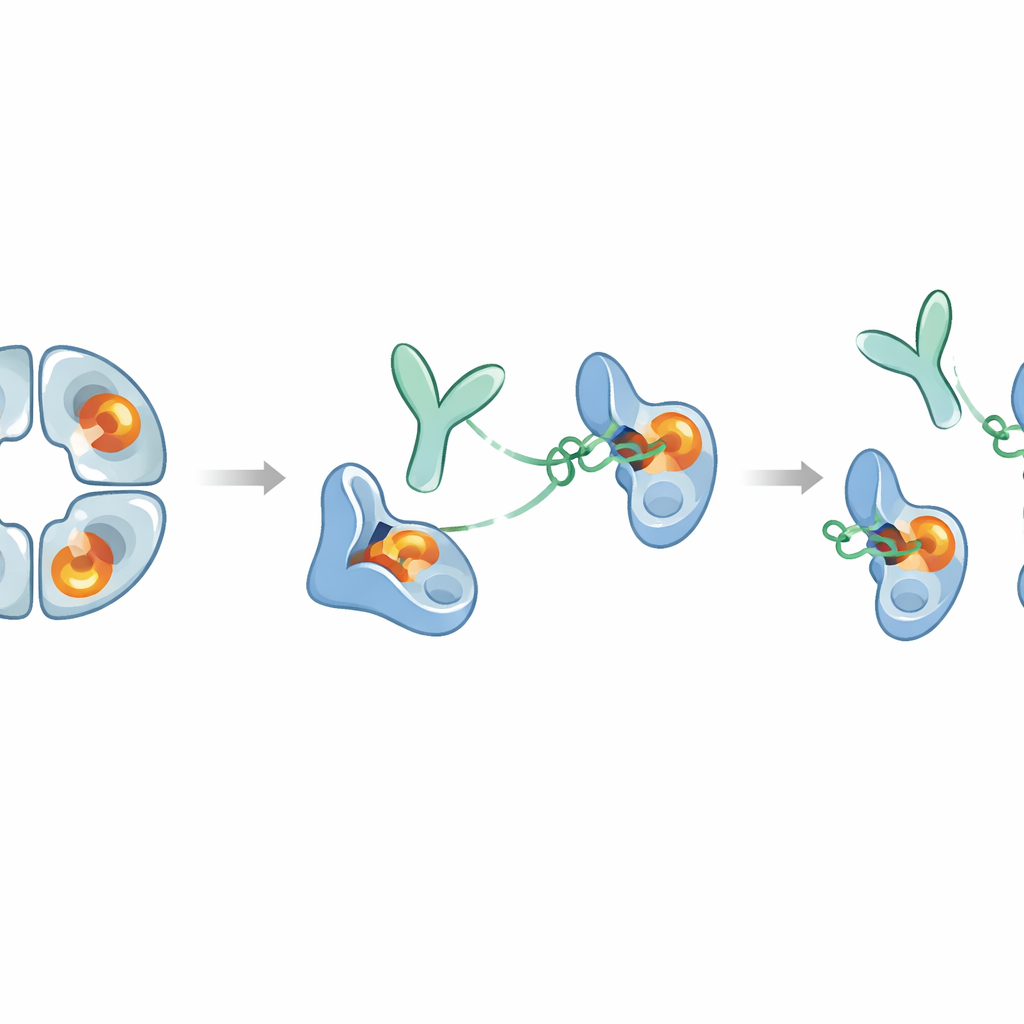
מה זה עשוי להביא לטיפולים עתידיים
במבט כולל, העבודה חושפת דוגמה נדירה של נוגדן שמשקיט לחלוטין אנזים שקשה לתרופף אותו על‑ידי משיכה באתר מרוחק במקום חסימת מרכז הפעילות. E82.AS גם מפרקת את הטטראמר של בטא‑טריפטאז וגם נועלת כל מונומר למבנה "כמו-זימוגן" לא פעיל, אפילו כשהמולקולה המסייעת הפואנדרית הנקראת הלפרין נוכחת ומגבירה פעילות. מאחר שקטע הנוגדן בלבד מסוגל לעשות זאת, ייתכן שניתן לעצב וריאנטים קטנים יותר המתאימים יותר להגעה לדרכי הנשימה הדלקתיות. יחד עם זאת, לבטא‑טריפטאז יש תפקידים מועילים בוויסות אותות החיסון, ולכן כל טיפול יצטרך לאזן חסימת פעילות מופרזת מזיקה מבלי לדכא יתר על המידה פונקציות מועילות לזמן ארוך. מחקר זה מציע מפת דרכים מולקולרית מפורטת לאיזון כזה ומרמז שאסטרטגיות אלוסטריות דומות יכולות לשמש לעיצוב מעכבים בררניים מאוד לאנזימים אחרים המעורבים במחלות אנושיות.
ציטוט: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
מילות מפתח: תאי מאסט, בטא‑טריפטאז, נוגדן אלוסטרי, אסטמה, עיכוב אנזימטי