Clear Sky Science · ar
إيقاف كامل لبِتا-تربتاز عن طريق تفكك الرباعي والالستيرية في الموقع النشط نتيجة لمخلوف واحد في الجسم المضاد
لماذا هذا مهم للحساسية والربو
يعاني الأشخاص المصابون بالربو أو الحساسية الشديدة أو التأقن غالبًا لأن خلايا مناعية معينة في أنسجتهم تطلق مواد قوية تسبب ضيق المجاري التنفسية وتلحق أذى بالأنسجة. أحد المسببات الرئيسية هو إنزيم يُدعى بيتا-تربتاز، مخزون في خلايا البدينة ويُفرَج أثناء التفاعلات التحسسية. تصف هذه الدراسة جسمًا مضادًا مُهندسًا بشكل خاص يمكنه إيقاف بيتا-تربتاز تمامًا بطريقة جديدة، ما قد يفتح الباب لعلاجات أفضل للأمراض المدفوعة بخلايا البدينة.
المسبب داخل خلايا البدينة
تجلس خلايا البدينة كحراس في أنسجة مثل الرئتين والأمعاء والجلد. عند استشعارها لمسببات الحساسية أو سموم الأفاعي أو الميكروبات، تفرغ بسرعة حويصلات مليئة بالهيستامين وبروتينات إشارية وإنزيمات. يُعد بيتا-تربتاز أكثر هذه الإنزيمات وفرة ويسهم في تضييق الشعب الهوائية وزيادة إنتاج الكولاجين وانقباض العضلات في الرئتين، وكلها عوامل تزيد من سوء الربو والأمراض الالتهابية الأخرى. عادةً ما يتجمع بيتا-تربتاز ليكوّن حلقة رباعية أو تيترايمر، تتجه مواقعها النشطة نحو مسام داخلية مركزية. هذا التركيب يخفي المراكز النشطة من معظم المثبطات الطبيعية في الجسم، مما يجعل بيتا-تربتاز صعبًا على نحو خاص في الاستهداف بالأدوية التقليدية.
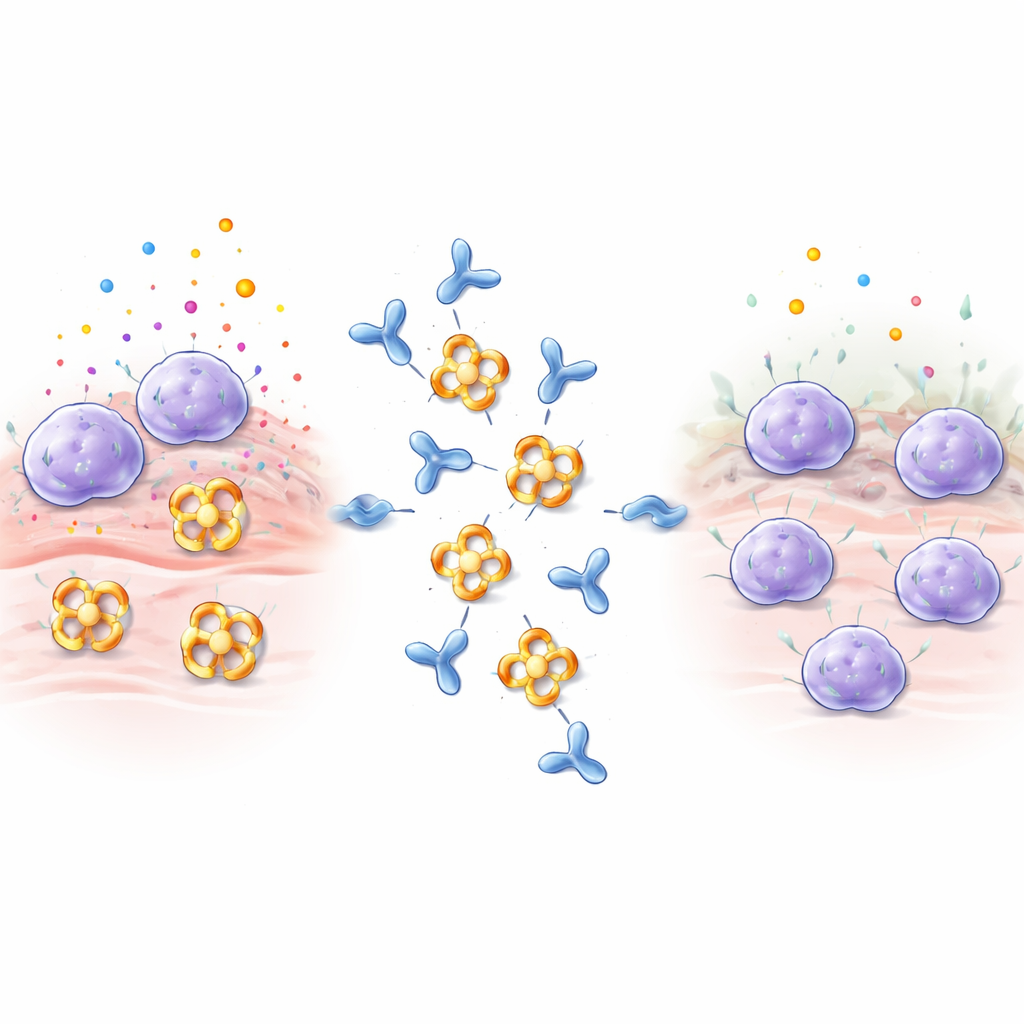
تصميم جسم مضاد يُعطّل الإنزيم
لقّح الباحثون أرانبًا ببيتا-تربتاز البشري وفحصوا الأجسام المضادة الناتجة، مع التركيز على واحد يسمى E82.AS. على خلاف الأجسام المضادة السابقة التي عطّلت الإنزيم جزئيًا فقط، استطاع E82.AS أن يكبت نشاط بيتا-تربتاز حتى في ظروف تحافظ عادةً على نشاطه القوي. أظهرت اختبارات الارتباط التفصيلية أن الجسم المضاد الكامل وقطعه الصغيرة (Fab) يرتبطان ببيتا-تربتاز بقوة ويثبطانه بطريقة تعتمد على الجرعة. عندما خلط الفريق E82.AS مع الإنزيم الرباعي ومرروه عبر أعمدة فصل، رأوا أن التيترايمر انقسم إلى وحدات مفردة ترافقت مع الجسم المضاد، مما يدل على أن E82.AS يجبر الحلقة على الانفصال إلى أحاديات.
قبضة بعيدة تقلب مفتاح الإيقاف
لفهم كيفية عمل E82.AS بفعالية عالية، استخدم العلماء قياسات تبادل الهيدروجين-الديوتيريوم والمجهر الإلكتروني البارد عالي الدقة. كشفت هذه الأساليب أن الجسم المضاد لا يرتبط في المسام المركزية للإنزيم أو في الأخدود الحفّاز. بدلًا من ذلك، يمسك ببقعة على السطح—"موقع خارجي"—بعيدة إلى حد ما عن مركز القطع الكيميائي. مع ذلك، تُطلق هذه القطبة البعيدة سلسلة من التغييرات الشكلية التي تنتقل عبر حلقات مرنة في الإنزيم إلى الموقع النشط نفسه. في الشكل المرتبط بالجسم المضاد، تتشوّه أو تتحرك ميزات هيكلية حاسمة عادةً تثبّت تفاعل القطع، مثل جيب صغير يحمل الرابطة المتفاعلة وشحنة سالبة رئيسية تجذب الأحماض الأمينية القاعدية. نتيجة لذلك، لم يعد الموقع النشط قادرًا على استيعاب أيًا من الركائز البروتينية الطبيعية أو المثبطات البروتينية الضخمة.
قوة تعديل على مستوى ذرة واحدة
إحدى النتائج اللافتة أن تغيير حمض أميني واحد في الجسم المضاد يمكن أن يفصل الارتباط عن الوظيفة. عدّل الفريق مخلوفًا واحدًا في السلسلة الخفيفة للجسم المضاد—بتغيير حمض الأسبارتيك إلى جلايسين في الموضع 93. هذا التعديل الضئيل أضعف قليلًا فقط مدى ارتباط الجسم المضاد ببيتا-تربتاز، لكنه ألغى تمامًا قدرته على تفكيك التيترايمر أو حجب النشاط الإنزيمي. تُظهر التحليلات الهيكلية أن ذيل الأسبارتيك الأصلي يدفع ضد حلقة في بيتا-تربتاز، دافعًا مخلوفًا مجاورًا ومن خلال رابطة ثنائية الكبريتيد، ناقلًا التشويه إلى قلب الموقع النشط. إزالة ذلك الذيل تُلغي الدفع الميكانيكي، فتظل الوحدة الإنزيمية مجمعة ونشطة على الرغم من وجود الجسم المضاد. على النقيض من ذلك، بإضافة شحنتين موجبتين في موضعين بالسلسلة الثقيلة، عزز الباحثون الجذب الكهروستاتيكي لبقعة سالبة الشحنة على الإنزيم وحسّنوا الفعالية المثبطة بما يصل تقريبًا إلى خمس مرات.
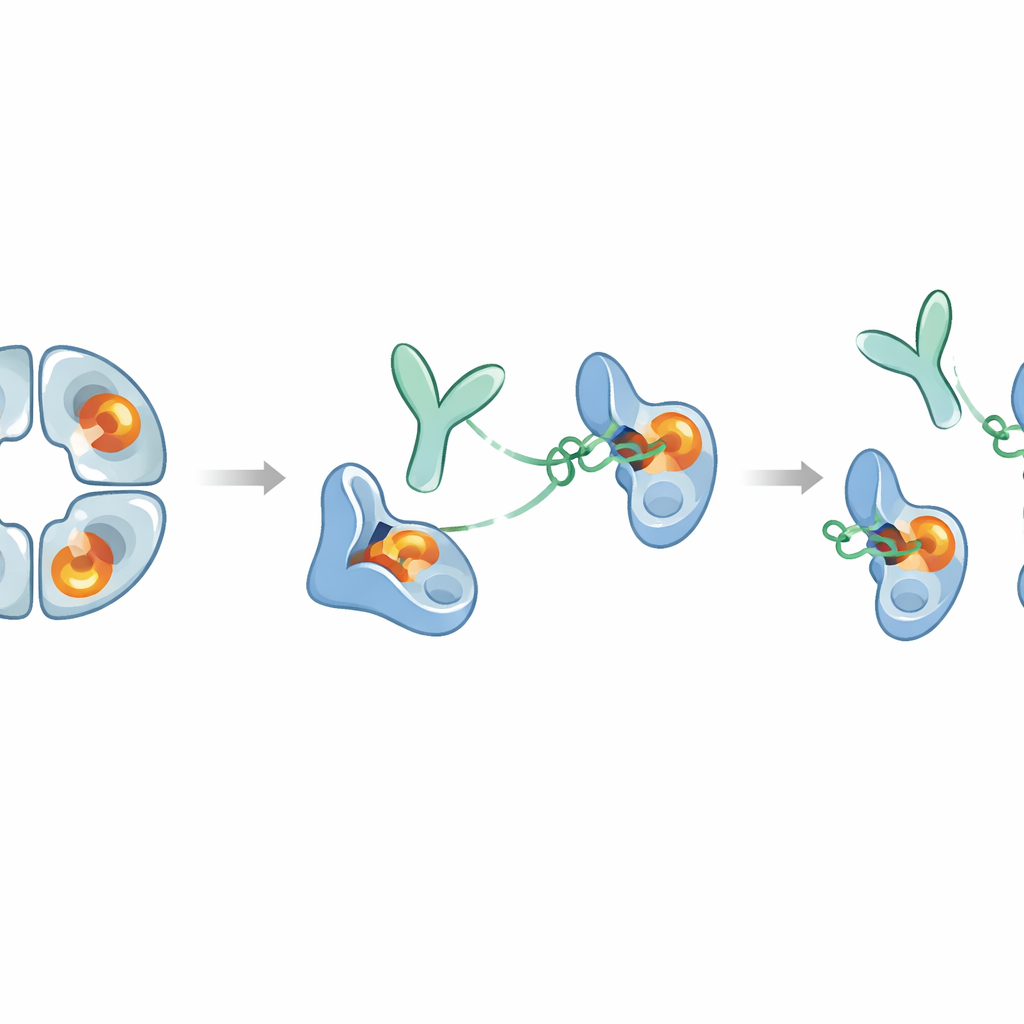
ما الذي قد يعنيه هذا للعلاجات المستقبلية
تظهر النتائج معًا مثالًا نادرًا لجسم مضاد يصمّت إنزيمًا يصعب استهدافه تمامًا عن طريق سحب موقع بعيد بدلًا من سد المركز النشط. يقوم E82.AS بتفكيك تيترايمر بيتا-تربتاز ويقفل كل أحادي في شكل غير نشط شبيه بالزيموجين، حتى عند وجود جزيء مساعد مثل الهيبارين الذي يعزز النشاط. وبما أن جزء الجسم المضاد وحده قادر على القيام بذلك، فقد يكون من الممكن تصميم نسخ أصغر تصل إلى الممرات الهوائية الملتهبة بصورة أفضل. في الوقت نفسه، يلعب بيتا-تربتاز أدوارًا مفيدة في تنظيم الإشارات المناعية، لذا ستحتاج أي معالجة إلى موازنة حجب النشاط المفرط الضار دون كبت الوظائف المفيدة لفترة طويلة. تقدم هذه الدراسة مخططًا جزيئيًا مفصّلًا لتلك الموازنة وتقترح أن استراتيجيات آلستيرية مماثلة يمكن أن تُستخدم لتصميم مثبطات انتقائية عالية لأنزيمات أخرى مشاركة في الأمراض البشرية.
الاستشهاد: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
الكلمات المفتاحية: خلايا البدينة, بيتا-تربتاز, جسم مضاد آلستيري, الربو, تثبيط الإنزيم