Clear Sky Science · ru
Полная ингибиция β-триптазы через диссоциацию тетрамера и аллостерию активного центра, вызванную одной остаточной аминокислотой антитела
Почему это важно для аллергии и астмы
У людей с астмой, тяжелыми аллергиями или анафилаксией часто возникают проблемы, потому что определенные иммунные клетки в тканях высвобождают мощные химические медиаторы, которые сужают дыхательные пути и повреждают ткани. Одним из ключевых виновников является фермент под названием бета‑триптаза, запасаемый в тучных клетках и высвобождаемый при аллергических реакциях. В этом исследовании описано специально сконструированное антитело, которое способно в новом режиме полностью выключать бета‑триптазу, что потенциально открывает путь к лучшим методам лечения заболеваний, обусловленных активностью тучных клеток.
Злодей внутри тучных клеток
Тучные клетки размещаются по всему организму в тканях, таких как легкие, кишечник и кожа. При контакте с аллергенами, ядами или микроорганизмами они быстро выбрасывают гранулы, наполненные гистамином, сигнальными белками и ферментами. Бета‑триптаза — самый обильный из этих ферментов и способствует сужению дыхательных путей, повышенному образованию коллагена и сокращению мышц в легких, что усугубляет астму и другие воспалительные заболевания. Бета‑триптаза обычно собирается в четырехчастное кольцо, или тетрамер, активные центры которого обращены во внутренний канал. Такая архитектура скрывает каталитические центры от большинства природных ингибиторов в организме, что делает бета‑триптазу особенно трудно блокируемой традиционными препаратами.
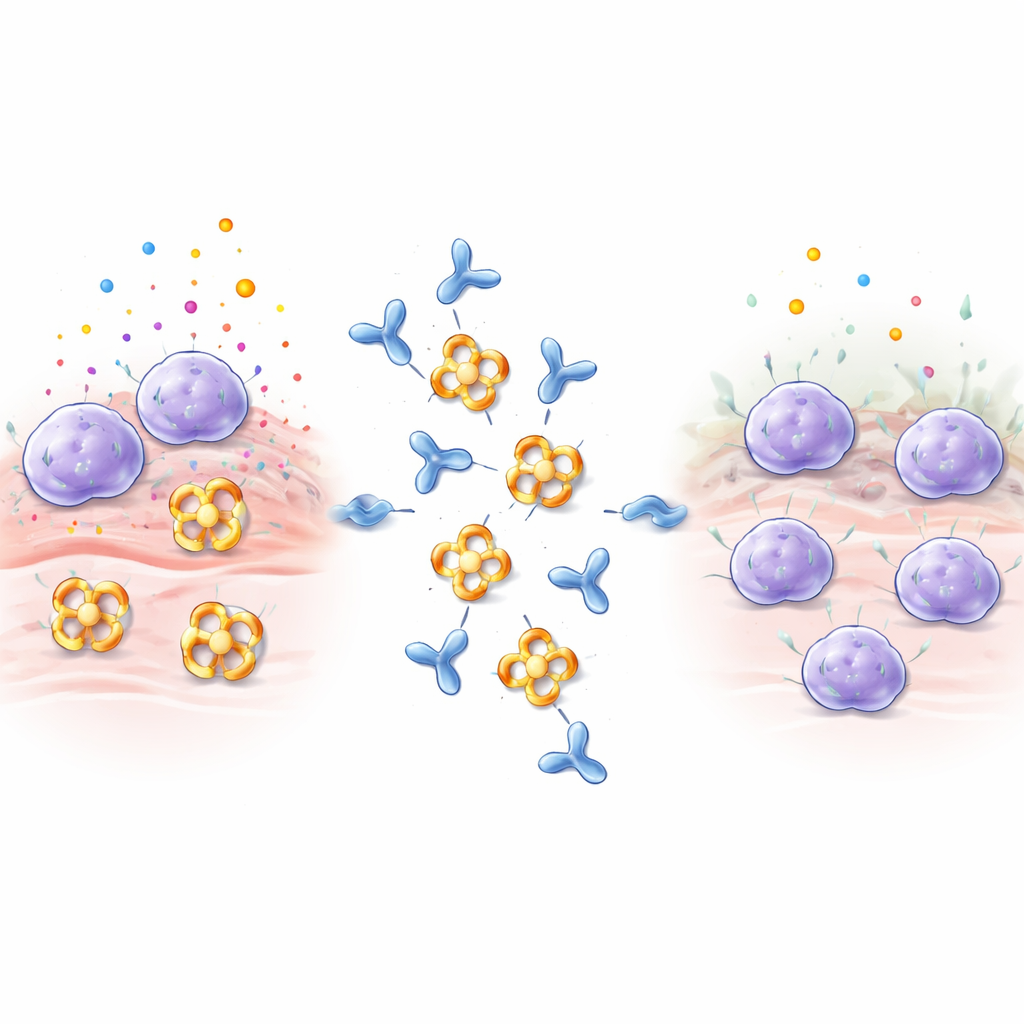
Проектирование антитела, которое выключает фермент
Исследователи иммунизировали кроликов человеческой бета‑триптазой и просеяли полученные антитела, сосредоточив внимание на одном, обозначенном E82.AS. В отличие от прежних антител, которые лишь частично ослабляли фермент, E82.AS мог подавлять активность бета‑триптазы даже в условиях, обычно сохраняющих ее высокую активность. Подробные эксперименты по связыванию показали, что и полная форма антитела, и его меньший фрагмент (Fab) прочно прикрепляются к бета‑триптазе и ингибируют ее в дозозависимой манере. При смешивании E82.AS с четырехчастным ферментом и пропускании через колонки разделения наблюдали, что тетрамер распадался на одиночные мономеры, которые шли в комплексе с антителом, что указывает на то, что E82.AS заставляет кольцо распадаться на мономеры.
Далекий захват, который включает выключатель
Чтобы понять, почему E82.AS работает так эффективно, ученые использовали измерения водород‑дейтериевого обмена и метод высокоразрешающей криоэлектронной микроскопии. Эти подходы показали, что антитело не связывается в центральном канале фермента или в каталитической борозде. Вместо этого оно захватывает участок на поверхности — «экзосайт» — достаточно далеко от химического режущего центра. Тем не менее, этот далёкий захват запускает каскад конформационных изменений, которые проходят через гибкие петли фермента и доходят до активного центра. В антителозависимой форме критические структурные элементы, которые обычно стабилизируют реакцию расщепления — такие как небольшой карман, удерживающий разрывающуюся связь, и ключевой отрицательно заряженный участок, привлекающий основные аминокислоты — искажены или смещены. В результате активный центр больше не может размещать ни естественные белковые субстраты, ни громоздкие белковые ингибиторы.
Сила тонкой атомной правки
Одно из наиболее поразительных открытий состоит в том, что одно изменение аминокислоты в антителе может разъединить связывание и функциональную активность. Команда изменила один остаток в легкой цепи антитела — заменив аспартат на глицин в позиции 93. Эта крошечная модификация едва ослабила сродство антитела к бета‑триптазе, но полностью лишила его способности разрывать тетрамер или блокировать ферментативную активность. Структурный анализ показывает, что оригинальный боковой цепной фрагмент аспартата давит на одну петлю в бета‑триптазе, подталкивая соседний остаток и через дисульфидную связь передавая искажение в сердце активного центра. Удаление этой боковой цепи устраняет механическое воздействие, поэтому фермент остается собранным и активным несмотря на присутствие антитела. Напротив, добавление положительных зарядов в двух позициях тяжелой цепи усиливало электростатическое притяжение к отрицательно заряженному участку фермента и повышало ингибирующую силу почти в пять раз.
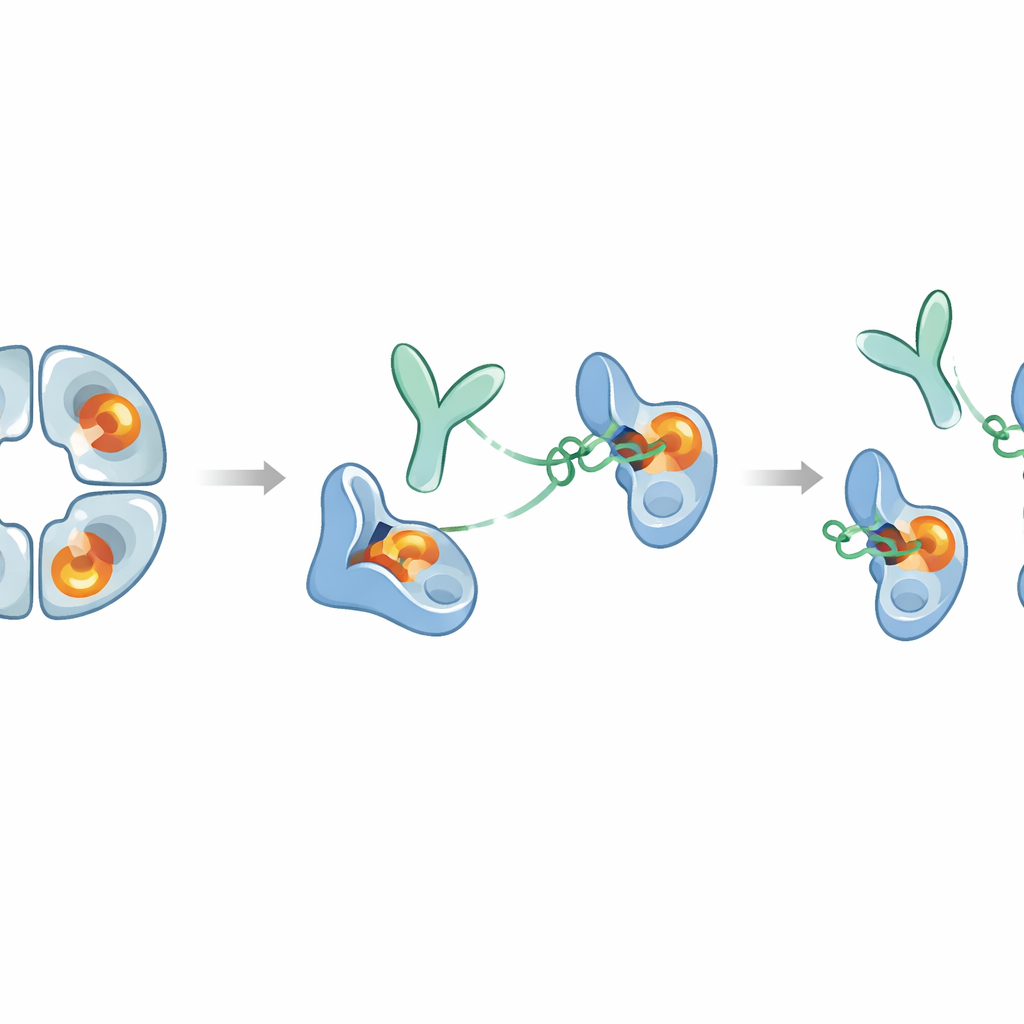
Что это может значить для будущих препаратов
В сумме работа демонстрирует редкий пример антитела, которое полностью заглушает трудно поддающийся лекарственной атаке фермент, воздействуя на удалённый участок вместо того, чтобы закрывать активный центр. E82.AS одновременно разъединяет тетрамер бета‑триптазы и фиксирует каждый мономер в «зимогеноподобной» неактивной форме, даже при наличии связующего активность вспомогательного молекулы — гепарина. Поскольку фрагмент антитела сам по себе способен на это, возможно создание уменьшенных версий, лучше подходящих для доставки в воспалённые дыхательные пути. В то же время бета‑триптаза играет полезную роль в регуляции иммунных сигналов, поэтому любая терапия должна будет уравновешивать блокирование вредной гиперактивности без чрезмерного подавления полезных функций в течение длительного времени. Это исследование предоставляет детальную молекулярную схему для такого баланса и указывает, что аналогичные аллостерические стратегии можно применять для разработки высокоселективных ингибиторов других ферментов, вовлеченных в болезни человека.
Цитирование: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
Ключевые слова: тучные клетки, бета-триптаза, аллостерическое антитело, астма, ингибирование ферментов