Clear Sky Science · nl
Volledige remming van β-tryptase door dissociatie van het tetramer en allosterie van het actieve centrum door één antistofresidu
Waarom dit belangrijk is voor allergieën en astma
Mensen met astma, ernstige allergieën of anafylaxie hebben vaak problemen omdat bepaalde immuuncellen in hun weefsels krachtige stoffen afgeven die de luchtwegen vernauwen en weefsel beschadigen. Een van de belangrijkste boosdoeners is een enzym genaamd beta‑tryptase, opgeslagen in mastcellen en vrijgegeven tijdens allergische reacties. Deze studie beschrijft een speciaal ontworpen antistof die beta‑tryptase op een nieuwe manier volledig kan uitschakelen, wat mogelijk de weg vrijmaakt voor betere behandelingen van ziekten die door mastcellen worden aangedreven.
De veroorzaker binnen mastcellen
Mastcellen fungeren als wachters in weefsels zoals longen, darm en huid. Wanneer ze allergenen, gifstoffen of microben detecteren, scheiden ze snel blaasjes uit gevuld met histamine, signaalproteïnen en enzymen. Beta‑tryptase is het meest overvloedige van deze enzymen en draagt bij aan luchtwegvernauwing, extra collageenproductie en spiercontractie in de longen, wat astma en andere ontstekingsziekten verergert. Beta‑tryptase assembleert normaal gesproken tot een ring van vier onderdelen, een tetramer, waarvan de actieve centra naar een centrale pore wijzen. Deze architectuur verbergt de actieve centra voor de meeste natuurlijke remmers in het lichaam, waardoor beta‑tryptase bijzonder moeilijk te blokkeren is met conventionele geneesmiddelen.
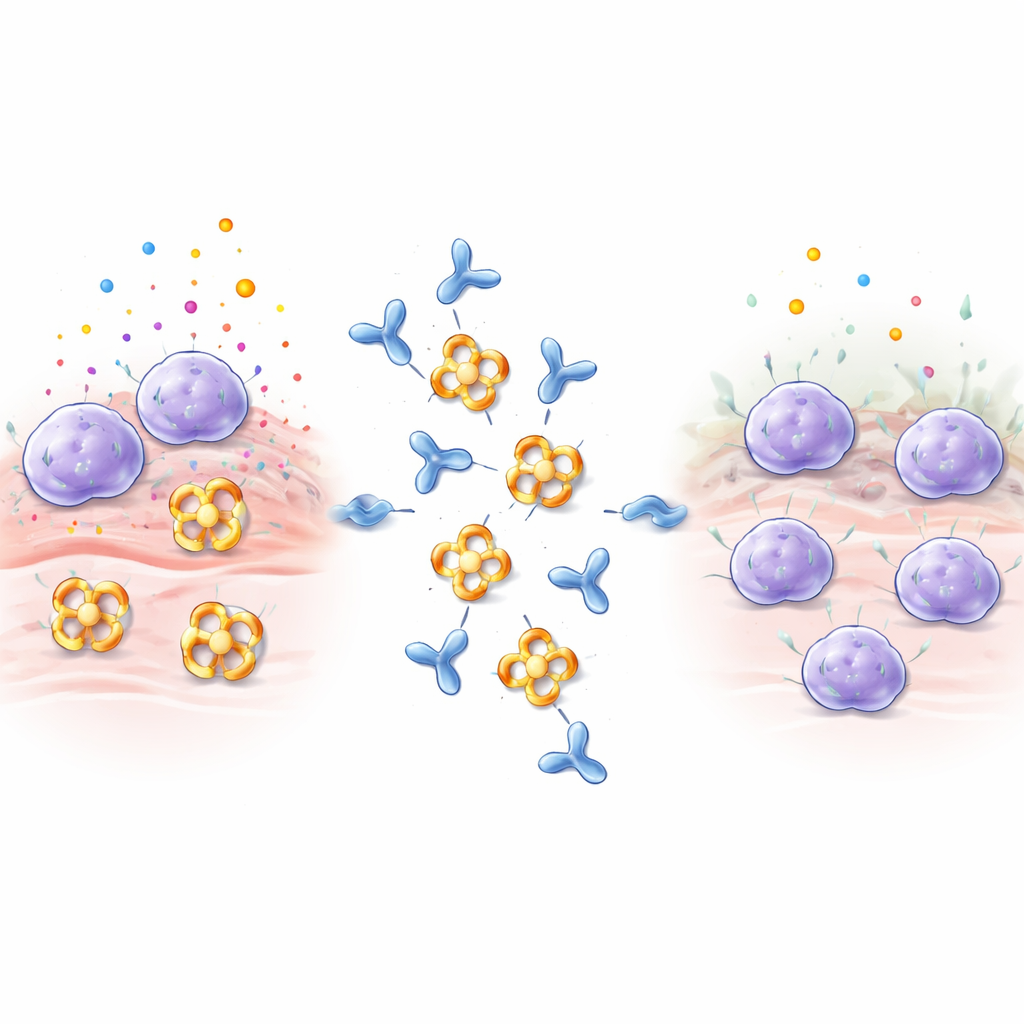
Ontwerpen van een antistof die het enzym uitschakelt
De onderzoekers immuniseerden konijnen met menselijke beta‑tryptase en screenden de resulterende antistoffen, met de focus op één antistof genaamd E82.AS. In tegenstelling tot eerdere antistoffen die het enzym slechts gedeeltelijk inactiveren, kon E82.AS de activiteit van beta‑tryptase onderdrukken zelfs onder omstandigheden die het normaal sterk actief houden. Gedetailleerde bindingsmetingen toonden aan dat zowel het volledige antistofmolecuul als het kleinere fragment (Fab) zeer strak aan beta‑tryptase binden en het remmen in een dosisafhankelijke manier. Wanneer het team E82.AS met het vierdelige enzym mengde en door scheidingskolommen liet lopen, zagen ze dat het tetramer uiteenviel in enkele eenheden die samen met de antistof migreerden, wat aangeeft dat E82.AS de ring dwingt uiteen te vallen tot monomeren.
Een verre greep die de uitschakelaar omzet
Om te begrijpen waarom E82.AS zo effectief werkt, gebruikten de wetenschappers waterstof–deuteriumuitwisseling en hoogresolutie cryo-elektronenmicroscopie. Deze benaderingen toonden aan dat de antistof niet bindt in de centrale pore of het katalytische groefje van het enzym. In plaats daarvan grijpt hij een oppervlakpatroon vast—een “exosite”—dat behoorlijk ver van het chemische snijcentrum ligt. Toch zet deze verre greep een cascade van vormveranderingen in gang die via flexibele lussen van het enzym naar het actieve centrum reizen. In de antistofgebonden vorm zijn cruciale structurele kenmerken die normaal gesproken de knipreactie stabiliseren, zoals een klein pocket dat de reagerende binding vasthoudt en een belangrijke negatieve lading die basische aminozuren aantrekt, vervormd of verplaatst. Daardoor kan het actieve centrum noch natuurlijke eiwitsubstraten noch omvangrijke eiwitgebaseerde remmers herbergen.
De kracht van een wijziging op atoomniveau
Een van de meest opvallende bevindingen is dat een enkele aminozuurverandering in de antistof binden en functie kan ontkoppelen. Het team veranderde één residu in de lichte keten van de antistof—vervanging van een aspartraat door glycine op positie 93. Deze kleine wijziging verzwakte nauwelijks hoe goed de antistof aan beta‑tryptase bond, maar maakte zijn vermogen om het tetramer uiteen te trekken of enzymatische activiteit te blokken volledig ongedaan. Structurele analyse laat zien dat de oorspronkelijke aspartraatzijdeketen tegen een lus in beta‑tryptase duwt, een nabijgelegen residu aanstoort en via een disulfidebrug de vervorming naar het hart van het actieve centrum overbrengt. Het verwijderen van die zijdeketen elimineert de mechanische duw, zodat het enzym geassembleerd en actief blijft ondanks de aanwezigheid van de antistof. Omgekeerd versterkten de onderzoekers door positieve ladingen op twee posities in de zware keten toe te voegen de elektrostatische aantrekking naar een negatief geladen oppervlak op het enzym en verbeterden ze de remkracht bijna tot vijf keer.
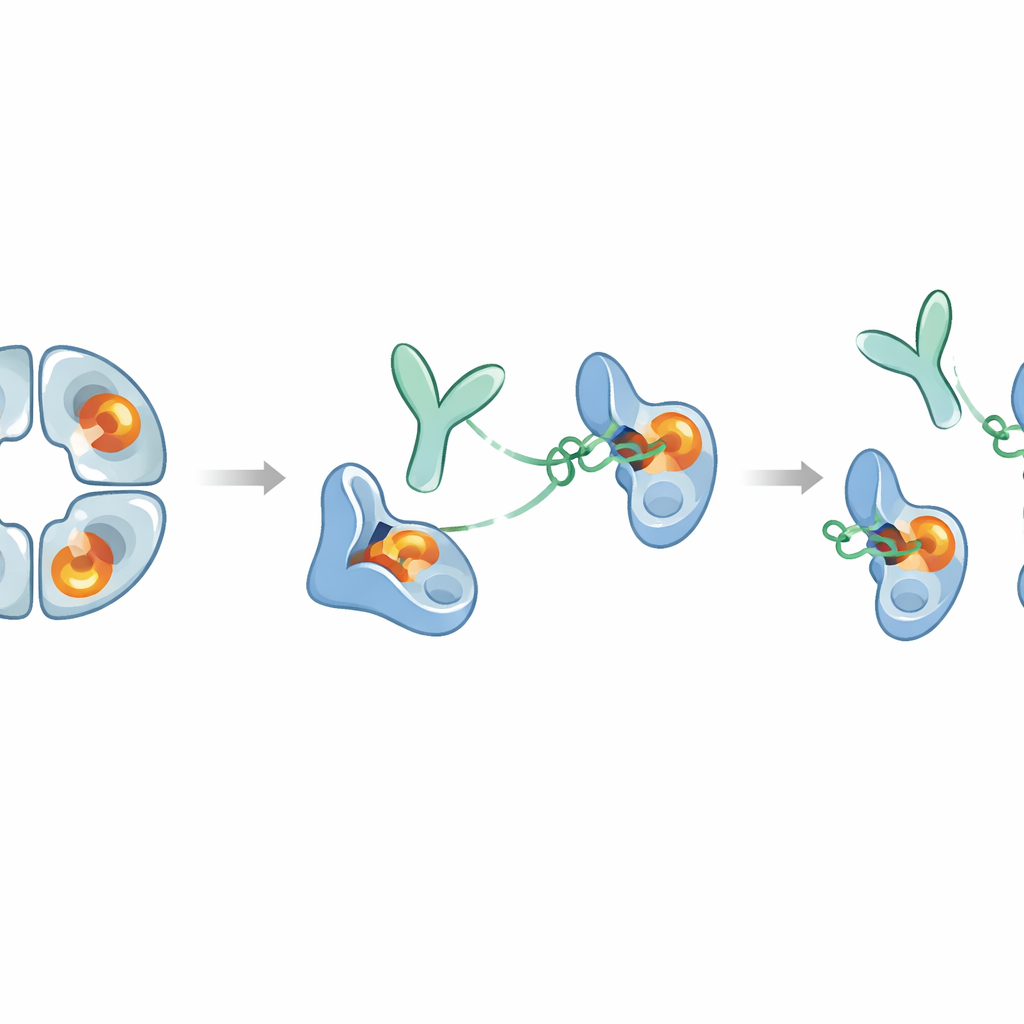
Wat dit kan betekenen voor toekomstige behandelingen
Alles bij elkaar onthult het werk een zeldzaam voorbeeld van een antistof die een moeilijk te behandelen enzym volledig stillegt door aan een ver verwijderd oppervlak te trekken in plaats van het actieve centrum te blokkeren. E82.AS prikt zowel het beta‑tryptase‑tetramer uit elkaar als vergrendelt elk monomeer in een “zymogeen‑achtige” inactieve vorm, zelfs wanneer een hulpstof genaamd heparine aanwezig is om de activiteit te versterken. Omdat het antistoffragment alleen dit effect kan bereiken, kan het mogelijk zijn kleinere versies te ontwerpen die beter geschikt zijn om ontstoken luchtwegen te bereiken. Tegelijkertijd heeft beta‑tryptase nuttige rollen in de regulatie van immuunsignalen, dus elke therapie zal een balans moeten vinden tussen het blokkeren van schadelijke overactiviteit en het niet te lang onderdrukken van nuttige functies. Deze studie biedt een gedetailleerd moleculair stappenplan voor die balans en suggereert dat soortgelijke allosterische strategieën gebruikt kunnen worden om zeer selectieve remmers te ontwerpen voor andere enzymen die bij menselijke ziekten betrokken zijn.
Bronvermelding: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
Trefwoorden: mastcellen, beta-tryptase, allosterisch antistof, astma, enzymremming