Clear Sky Science · fr
Inhibition complète de la β‑tryptase par dissociation du tétramère et allostérie du site actif due à un seul résidu d’anticorps
Pourquoi cela compte pour les allergies et l’asthme
Les personnes souffrant d’asthme, d’allergies sévères ou d’anaphylaxie ont souvent des difficultés parce que certains globules immunitaires présents dans les tissus libèrent des substances puissantes qui resserrent les voies respiratoires et endommagent les tissus. L’un des principaux coupables est une enzyme appelée β‑tryptase, stockée dans les mastocytes et libérée lors des réactions allergiques. Cette étude décrit un anticorps spécialement conçu capable d’éteindre complètement la β‑tryptase d’une nouvelle manière, ouvrant potentiellement la voie à de meilleurs traitements des maladies liées aux mastocytes.
Le fauteur de troubles à l’intérieur des mastocytes
Les mastocytes jouent le rôle de sentinelles dans des tissus comme les poumons, l’intestin et la peau. Lorsqu’ils détectent des allergènes, des venins ou des microbes, ils déversent rapidement des granules remplis d’histamine, de protéines de signalisation et d’enzymes. La β‑tryptase est l’enzyme la plus abondante de ces composants et contribue au rétrécissement des voies aériennes, à une production accrue de collagène et à la contraction musculaire dans les poumons, aggravant l’asthme et d’autres maladies inflammatoires. La β‑tryptase s’assemble normalement en un anneau à quatre unités, ou tétramère, dont les sites actifs sont orientés vers un pore central. Cette architecture masque les centres actifs à la plupart des inhibiteurs naturels de l’organisme, rendant la β‑tryptase particulièrement difficile à bloquer avec des médicaments conventionnels.
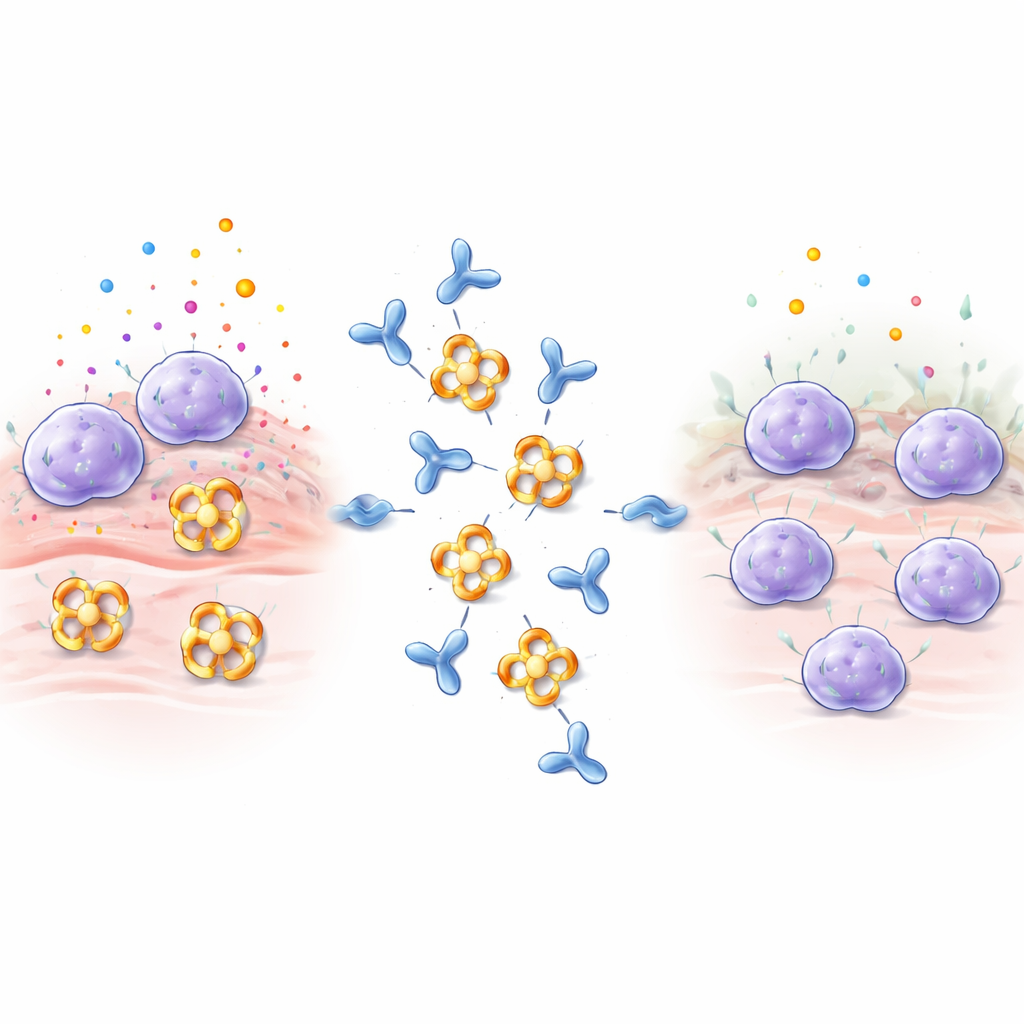
Concevoir un anticorps qui met l’enzyme hors d’état de nuire
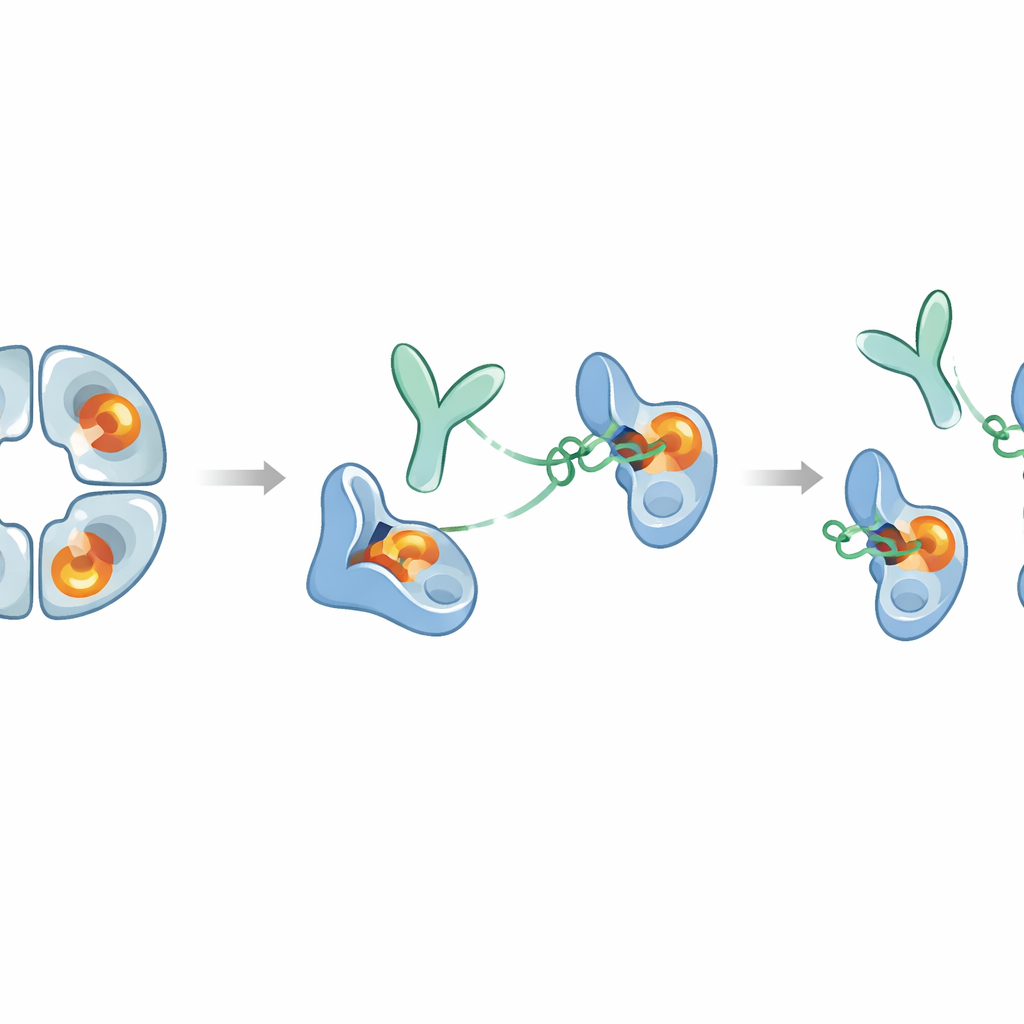
Les chercheurs ont immunisé des lapins avec de la β‑tryptase humaine et ont criblé les anticorps obtenus, en se concentrant sur un anticorps appelé E82.AS. Contrairement à des anticorps antérieurs qui ne désactivaient l’enzyme que partiellement, E82.AS pouvait supprimer l’activité de la β‑tryptase même dans des conditions qui la maintiennent généralement fortement active. Des tests de liaison détaillés ont montré que l’anticorps entier et son fragment plus petit (Fab) se fixent très fortement à la β‑tryptase et l’inhibent de façon dépendante de la dose. Lorsque l’équipe a mélangé E82.AS avec l’enzyme tétramérique et l’a fait passer sur des colonnes de séparation, ils ont observé que le tétramère se dissociait en unités individuelles qui migraient avec l’anticorps, indiquant que E82.AS force l’anneau à se décomposer en monomères.
Une prise lointaine qui déclenche l’interrupteur d’arrêt
Pour comprendre pourquoi E82.AS est si efficace, les scientifiques ont utilisé des mesures d’échange hydrogène–deutérium et la cryo‑microscopie électronique à haute résolution. Ces approches ont révélé que l’anticorps ne se lie pas dans le pore central ni dans la gouttière catalytique de l’enzyme. Au lieu de cela, il saisit une zone en surface — une « exosite » — située assez loin du centre de coupure chimique. Pourtant, cette prise distante déclenche une cascade de changements conformationnels qui se propagent à travers des boucles flexibles de l’enzyme jusqu’au site actif lui‑même. Dans la forme liée à l’anticorps, des éléments structuraux critiques qui stabilisent normalement la réaction de clivage, comme une petite poche qui accueille la liaison en cours de réaction et une charge négative clé qui attire les acides aminés basiques, sont déformés ou déplacés. En conséquence, le site actif ne peut plus accepter ni les substrats protéiques naturels ni les inhibiteurs volumineux à base de protéines.
La puissance d’un ajustement au niveau atomique
Une des découvertes les plus frappantes est qu’un seul changement d’acide aminé dans l’anticorps peut découpler la liaison de la fonction. L’équipe a modifié un résidu dans la chaîne légère de l’anticorps — remplaçant un aspartate par une glycine en position 93. Cette minuscule modification n’a quasiment pas affaibli l’affinité de liaison pour la β‑tryptase, mais a complètement annihilé sa capacité à dissocier le tétramère ou à bloquer l’activité enzymatique. L’analyse structurale montre que la chaîne latérale d’aspartate d’origine pousse contre une boucle de la β‑tryptase, poussant un résidu voisin et, via une liaison disulfure, transmettant la distorsion au cœur du site actif. La suppression de cette chaîne latérale élimine la poussée mécanique, de sorte que l’enzyme reste assemblée et active malgré la présence de l’anticorps. À l’inverse, en ajoutant des charges positives à deux positions de la chaîne lourde, les chercheurs ont renforcé l’attraction électrostatique vers une zone chargée négativement sur l’enzyme et amélioré la puissance inhibitrice jusqu’à près de cinq fois.
Ce que cela pourrait signifier pour les traitements futurs
Pris dans leur ensemble, ces travaux révèlent un exemple rare d’anticorps qui éteint complètement une enzyme difficile à cibler en tirant sur un site distant plutôt qu’en bouchant le centre actif. E82.AS écarte le tétramère de la β‑tryptase et verrouille chaque monomère dans une conformation inactive de type « zymogène », même lorsque la molécule auxiliaire héparine est présente pour augmenter l’activité. Parce que le fragment d’anticorps seul peut produire cet effet, il pourrait être possible de concevoir des versions plus petites mieux adaptées à l’atteinte des voies respiratoires enflammées. En même temps, la β‑tryptase joue des rôles bénéfiques dans la régulation des signaux immunitaires, si bien que toute thérapie devra équilibrer le blocage d’une suractivité nuisible sans supprimer trop longtemps des fonctions utiles. Cette étude fournit une feuille de route moléculaire détaillée pour cet équilibre et suggère que des stratégies allostériques similaires pourraient être employées pour concevoir des inhibiteurs hautement sélectifs d’autres enzymes impliquées dans des maladies humaines.
Citation: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
Mots-clés: mastocytes, β‑tryptase, anticorps allostérique, asthme, inhibition enzymatique