Clear Sky Science · es
Inhibición completa de la β-triptasa por disociación del tetrámero y alosteria del sitio activo debida a un único residuo de un anticuerpo
Por qué importa para las alergias y el asma
Las personas con asma, alergias graves o anafilaxia a menudo tienen problemas porque ciertas células inmunitarias en sus tejidos liberan sustancias potentes que constriñen las vías respiratorias y dañan el tejido. Uno de los culpables clave es una enzima llamada beta‑triptasa, almacenada en las células cebadas y liberada durante las reacciones alérgicas. Este estudio describe un anticuerpo especialmente diseñado que puede apagar completamente la beta‑triptasa de una manera nueva, lo que potencialmente abre la puerta a mejores tratamientos para enfermedades impulsadas por células cebadas.
El alborotador dentro de las células cebadas
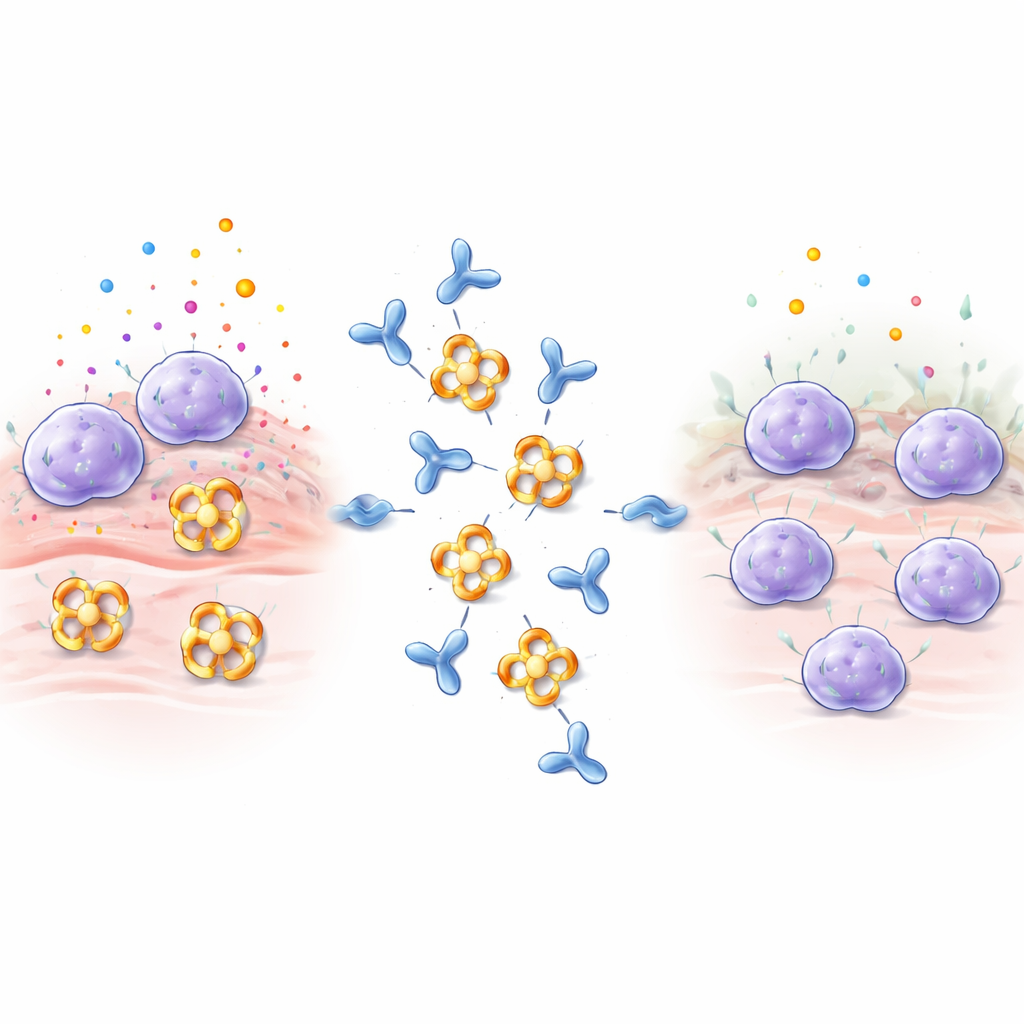
Las células cebadas actúan como centinelas en tejidos como los pulmones, el intestino y la piel. Cuando detectan alérgenos, venenos o microbios, liberan rápidamente gránulos llenos de histamina, proteínas señalizadoras y enzimas. La beta‑triptasa es la más abundante de estas enzimas y contribuye al estrechamiento de las vías respiratorias, al aumento de la producción de colágeno y a la contracción muscular en los pulmones, todo lo cual agrava el asma y otras enfermedades inflamatorias. Normalmente, la beta‑triptasa se ensambla en un anillo de cuatro unidades, o tetrámero, cuyos sitios activos apuntan hacia un poro central. Esta arquitectura oculta los centros activos a la mayoría de los inhibidores naturales del cuerpo, lo que hace que la beta‑triptasa sea especialmente difícil de bloquear con fármacos convencionales.
Diseñar un anticuerpo que apague la enzima
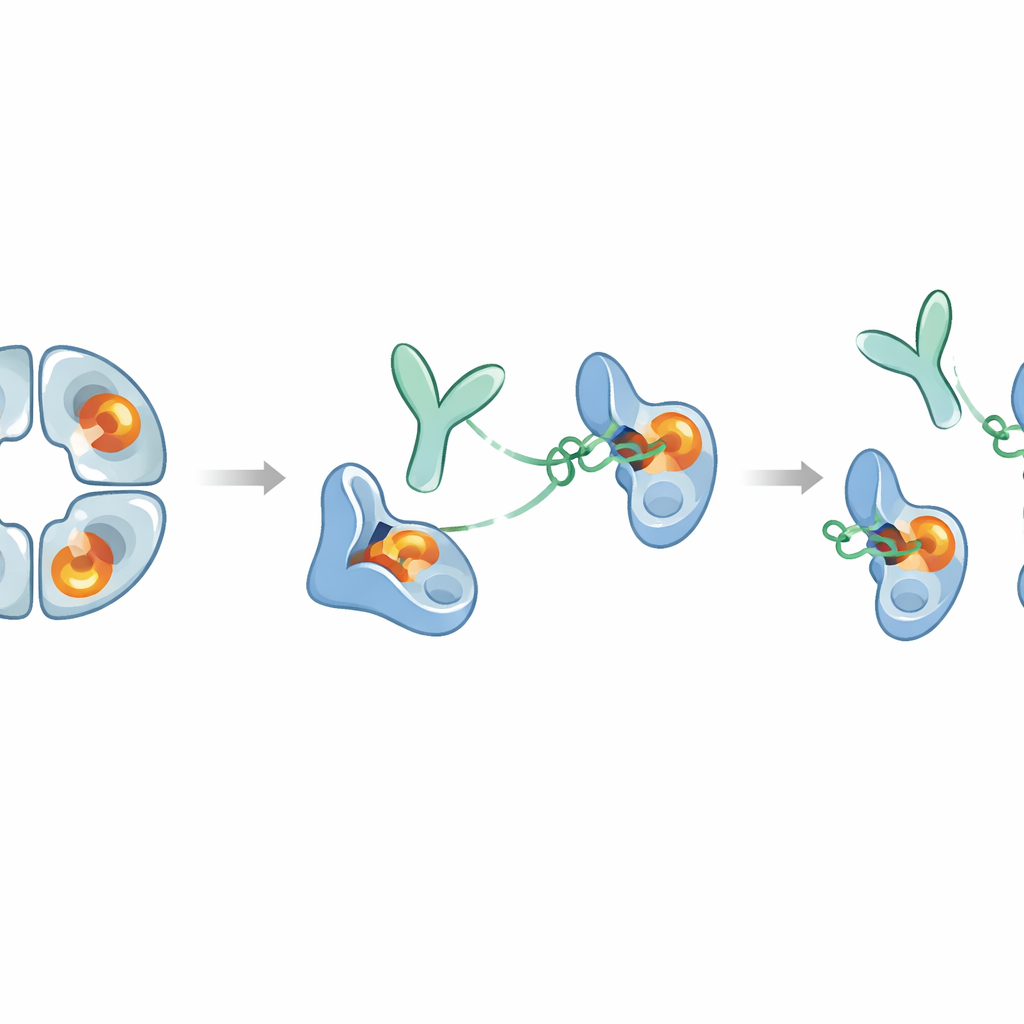
Los investigadores inmunizaron conejos con beta‑triptasa humana y cribaron los anticuerpos resultantes, concentrándose en uno llamado E82.AS. A diferencia de anticuerpos anteriores que solo desactivaban parcialmente la enzima, E82.AS pudo suprimir la actividad de la beta‑triptasa incluso en condiciones que normalmente la mantienen muy activa. Pruebas detalladas de unión mostraron que tanto el anticuerpo de longitud completa como su fragmento más pequeño (Fab) se fijan a la beta‑triptasa con gran afinidad e la inhiben de forma dependiente de la dosis. Cuando el equipo mezcló E82.AS con la enzima tetramérica y lo pasó por columnas de separación, observaron que el tetrámero se disociaba en unidades individuales que viajaban junto al anticuerpo, lo que indica que E82.AS fuerza al anillo a deshacerse en monómeros.
Un agarre distante que activa el interruptor de apagado
Para entender cómo E82.AS funciona con tanta eficacia, los científicos usaron medidas de intercambio hidrógeno‑deuterio y microscopía crioelectrónica de alta resolución. Estos enfoques revelaron que el anticuerpo no se une en el poro central de la enzima ni en la hendidura catalítica. En su lugar, se agarra a un parche en la superficie—un “exosito”—bastante alejado del centro químico de corte. Sin embargo, este agarre distante desencadena una cascada de cambios de forma que viajan a través de bucles flexibles de la enzima hasta el propio sitio activo. En la forma unida al anticuerpo, características estructurales críticas que normalmente estabilizan la reacción de corte, como una pequeña cavidad que aloja el enlace reaccionante y una carga negativa clave que atrae aminoácidos básicos, quedan distorsionadas o desplazadas. Como resultado, el sitio activo ya no puede acomodar ni los sustratos proteicos naturales ni inhibidores proteicos voluminosos.
El poder de una modificación a nivel atómico
Uno de los hallazgos más llamativos es que un solo cambio de aminoácido en el anticuerpo puede desacoplar la unión de la función. El equipo alteró un residuo en la cadena ligera del anticuerpo—cambiando una aspartato por una glicina en la posición 93. Esta mínima modificación debilitó apenas la afinidad con la que el anticuerpo se unía a la beta‑triptasa, pero abolió por completo su capacidad para deshacer el tetrámero o bloquear la actividad enzimática. El análisis estructural muestra que la cadena lateral del aspartato original empuja contra un bucle en la beta‑triptasa, desplazando un residuo cercano y, a través de un enlace disulfuro, transmitiendo la distorsión hasta el corazón del sitio activo. Eliminar esa cadena lateral elimina el empuje mecánico, de modo que la enzima permanece ensamblada y activa a pesar de la presencia del anticuerpo. Por el contrario, al añadir cargas positivas en dos posiciones de la cadena pesada, los investigadores reforzaron la atracción electrostática hacia un parche cargado negativamente en la enzima y mejoraron la potencia inhibitoria hasta casi cinco veces.
Qué podría significar para tratamientos futuros
En conjunto, el trabajo revela un raro ejemplo de un anticuerpo que silencia completamente una enzima difícil de tratar tirando de un sitio remoto en vez de tapar el centro activo. E82.AS tanto separa el tetrámero de beta‑triptasa como bloquea cada monómero en una conformación inactiva «tipo zimógeno», incluso cuando una molécula auxiliar llamada heparina está presente para potenciar la actividad. Dado que el fragmento del anticuerpo por sí solo puede hacer esto, podría ser posible diseñar versiones más pequeñas mejor adaptadas para alcanzar las vías respiratorias inflamadas. Al mismo tiempo, la beta‑triptasa tiene funciones beneficiosas en la regulación de señales inmunitarias, por lo que cualquier terapia deberá equilibrar el bloqueo de la sobreactividad dañina sin suprimir funciones útiles por demasiado tiempo. Este estudio ofrece un plano molecular detallado para ese equilibrio y sugiere que estrategias alostéricas similares podrían usarse para diseñar inhibidores altamente selectivos para otras enzimas implicadas en enfermedades humanas.
Cita: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
Palabras clave: células cebadas, beta-triptasa, anticuerpo alostérico, asma, inhibición enzimática