Clear Sky Science · ja
単一抗体残基による四量体解離と活性部位アロステリーによるβ-トリプターゼの完全阻害
アレルギーと喘息にとってなぜ重要か
喘息、重度のアレルギー、アナフィラキシーを持つ人々は、組織内の特定の免疫細胞が気道を収縮させ組織を損傷する強力な化学物質を放出するために問題を抱えがちです。その主要な原因の一つが、肥満細胞に蓄えられアレルギー反応時に放出される酵素β‑トリプターゼです。本研究は、β‑トリプターゼを新しい仕方で完全にオフにできるように設計された抗体を記述しており、肥満細胞が関与する疾患に対するより良い治療の可能性を開くものです。
肥満細胞内のトラブルメーカー
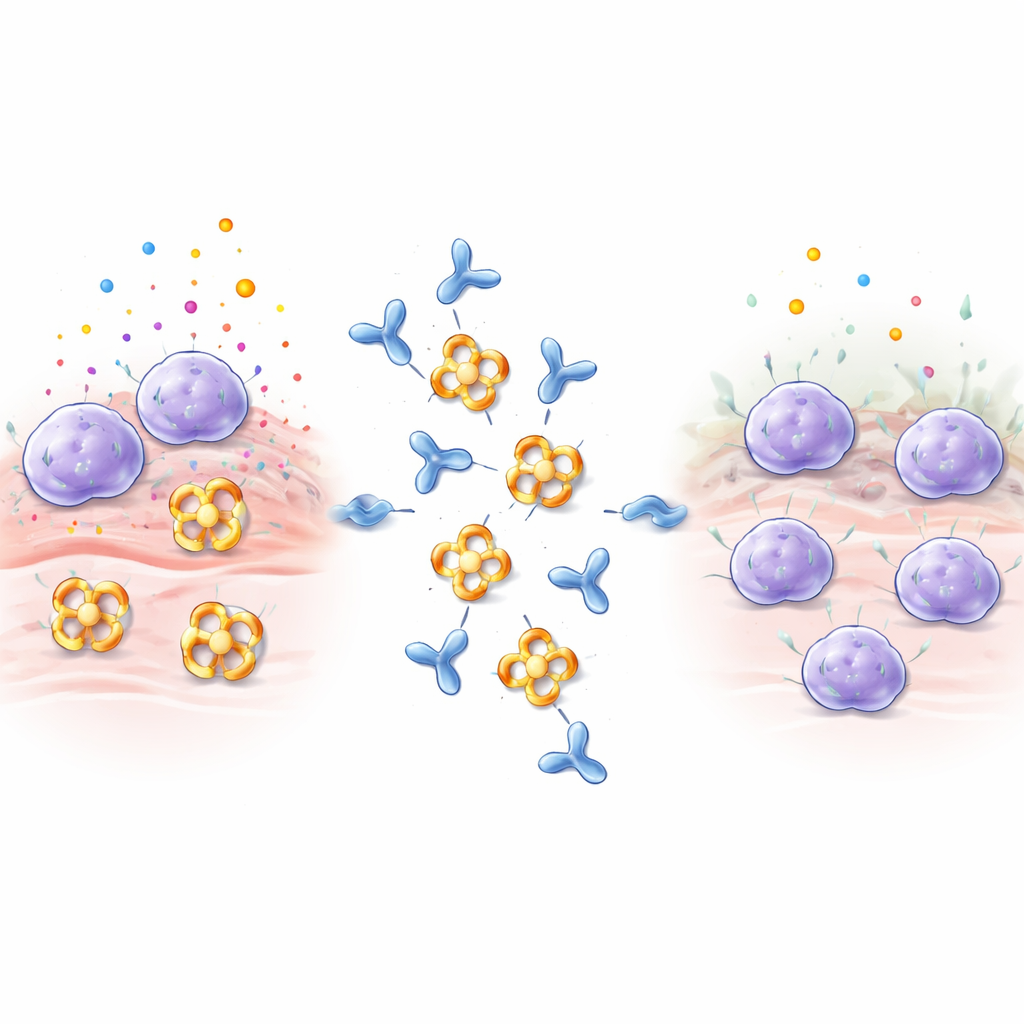
肥満細胞は肺、腸、皮膚などの組織で見張り役を務めます。アレルゲン、毒、微生物を感知すると、ヒスタミン、シグナル伝達タンパク質、酵素を詰めた小胞を素早く放出します。β‑トリプターゼはこれらの酵素の中で最も多く、気道の狭窄、余分なコラーゲン産生、肺での平滑筋収縮を促進し、喘息や他の炎症性疾患を悪化させます。β‑トリプターゼは通常、四量体と呼ばれる4つの部分のリングを形成し、その活性部位は中央の孔に向いています。この構造は体内の多くの天然阻害因子から活性中心を隠すため、従来の薬ではβ‑トリプターゼを阻害するのが特に難しくなっています。
酵素を止める抗体の設計
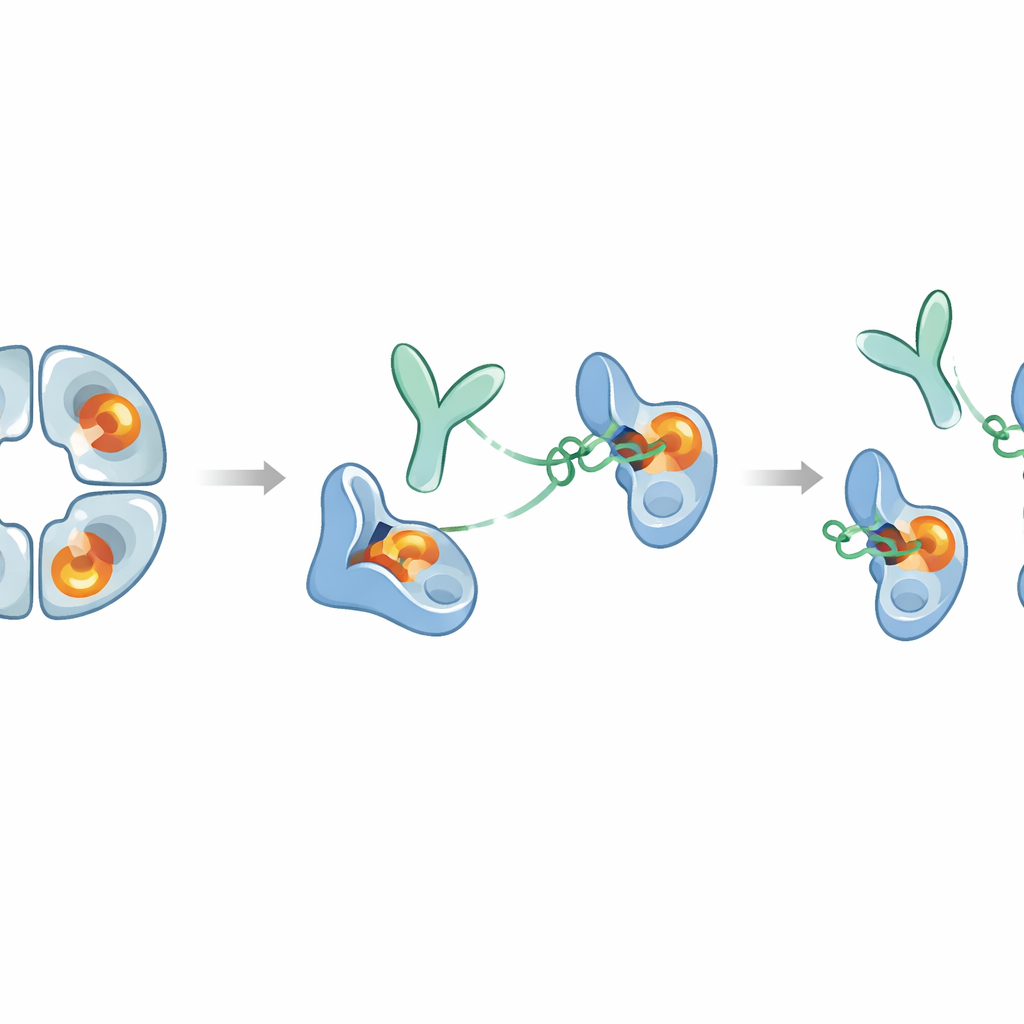
研究者らはヒトβ‑トリプターゼでウサギを免疫し、得られた抗体をスクリーニングして、E82.ASと呼ばれる1つに注目しました。これまでの部分的にしか酵素を無力化しない抗体とは異なり、E82.ASは通常強く活性を保つ条件下でもβ‑トリプターゼ活性を抑えることができました。詳細な結合試験は、全長抗体とその小さな断片(Fab)の両方がβ‑トリプターゼに非常に強く結合し、用量依存的に阻害することを示しました。研究チームがE82.ASを四量体酵素と混合して分離カラムに通すと、四量体が解離して抗体とともに移動する単量体になっていることが観察され、E82.ASがリングを壊して単量体化させることを示しました。
遠隔の把握がオフスイッチを切る
E82.ASがなぜこれほど効果的に働くのかを理解するために、科学者らは水素─重水素交換測定と高分解能クライオ電子顕微鏡を用いました。これらの手法は、抗体が酵素の中央の孔や触媒溝に結合するのではないことを明らかにしました。代わりに抗体は表面の“エキソサイト”(活性中心からかなり離れたパッチ)をつかみます。それでもこの遠隔の把握は、酵素の柔軟なループを介して活性部位に伝わる一連の形状変化を引き起こします。抗体結合型では、反応結合を保持する小さなポケットや塩基性アミノ酸を引き寄せる重要な負電荷といった切断反応を安定化する構造的要素が歪んだり移動したりします。その結果、活性部位は天然のタンパク質基質や大型のタンパク質ベースの阻害剤のいずれも収容できなくなります。
原子レベルの一つの調整の力
最も注目すべき発見の一つは、抗体の単一アミノ酸の変化が結合と機能を切り離し得ることです。チームは抗体の軽鎖の一残基を変え、93位のアスパラギン酸をグリシンに置換しました。この小さな修飾は抗体のβ‑トリプターゼへの結合力をほとんど弱めませんでしたが、四量体を解離させたり酵素活性を阻害したりする能力を完全に失わせました。構造解析は、元のアスパラギン酸側鎖がβ‑トリプターゼのループに押し当てられて近傍残基を軽く動かし、ジスルフィド結合を介して歪みを活性部位の中心へ伝えていることを示します。その側鎖を取り除くと機械的な押しが失われ、抗体が結合していても酵素は組み立てられたまま活性を保ちます。逆に、重鎖の二つの位置に正電荷を付加することで、酵素の負に帯電したパッチへの静電的引力が強化され、阻害効果が最大でほぼ5倍に向上しました。
将来の治療にとって何を意味するか
総じて、本研究は活性中心を塞ぐのではなく遠隔部位を引っ張ることで、薬剤化が難しい酵素を完全に沈黙させる稀な抗体の例を示しています。E82.ASはβ‑トリプターゼ四量体をこじ開けると同時に、各単量体を補助分子ヘパリンが存在して活性を高める状況でも“ジモーゲン様”の不活性な形に固定します。抗体断片だけでもこれを実現できるため、炎症を起こした気道に届きやすいより小さなバージョンを設計することが可能かもしれません。一方で、β‑トリプターゼは免疫シグナルの調節など有益な役割も持つため、治療では有害な過剰活性を抑える一方で有用な機能を長期間にわたり抑えすぎないバランスを取る必要があります。本研究はそのバランスのための詳細な分子設計図を提供し、同様のアロステリック戦略が他の疾患関連酵素に対して高選択的な阻害剤を設計するために応用できることを示唆しています。
引用: Maun, H.R., Azumaya, C.M., Walters, B.T. et al. Complete inhibition of β-tryptase by tetramer dissociation and active site allostery due to a single antibody residue. Nat Commun 17, 3393 (2026). https://doi.org/10.1038/s41467-026-70491-3
キーワード: 肥満細胞, β-トリプターゼ, アロステリック抗体, 喘息, 酵素阻害