Clear Sky Science · zh
致癌性的 CCDC6-RET 融合蛋白是一种同时依赖 ATP 和 ADP 的激酶
这项癌症研究为何重要
肺和甲状腺的某些癌症常由称为激酶的细胞通讯蛋白的异常变体驱动。其中一种常见变体——CCDC6‑RET 融合蛋白——在乳头状甲状腺癌和部分肺癌中频繁出现,尤其与辐射暴露后相关。本研究揭示了该融合蛋白如何自我激活,以及为何它可能特别适应肿瘤内部那种应激、能量匮乏的环境,为针对性治疗提供了新的思路。
助长肿瘤的基因拼接
在健康细胞中,RET 蛋白位于细胞膜上,帮助传递增长信号。在许多甲状腺癌以及一部分肺癌中,DNA 断裂并在错误位置重新连接,产生将 CCDC6 蛋白的一部分与 RET 的功能端融合的混合基因。产生的 CCDC6‑RET 成为一个独立的信号发动机,不再依赖正常的外部刺激。作者使用昆虫细胞大量表达了该融合蛋白,并显示它在溶液中形成非常稳定的二聚体。这些二聚体具有高度活性,自我发生多位点磷酸化,并对已知的 RET 抑制药有强烈响应,证明实验室制备的蛋白表现与临床驱癌体相似。
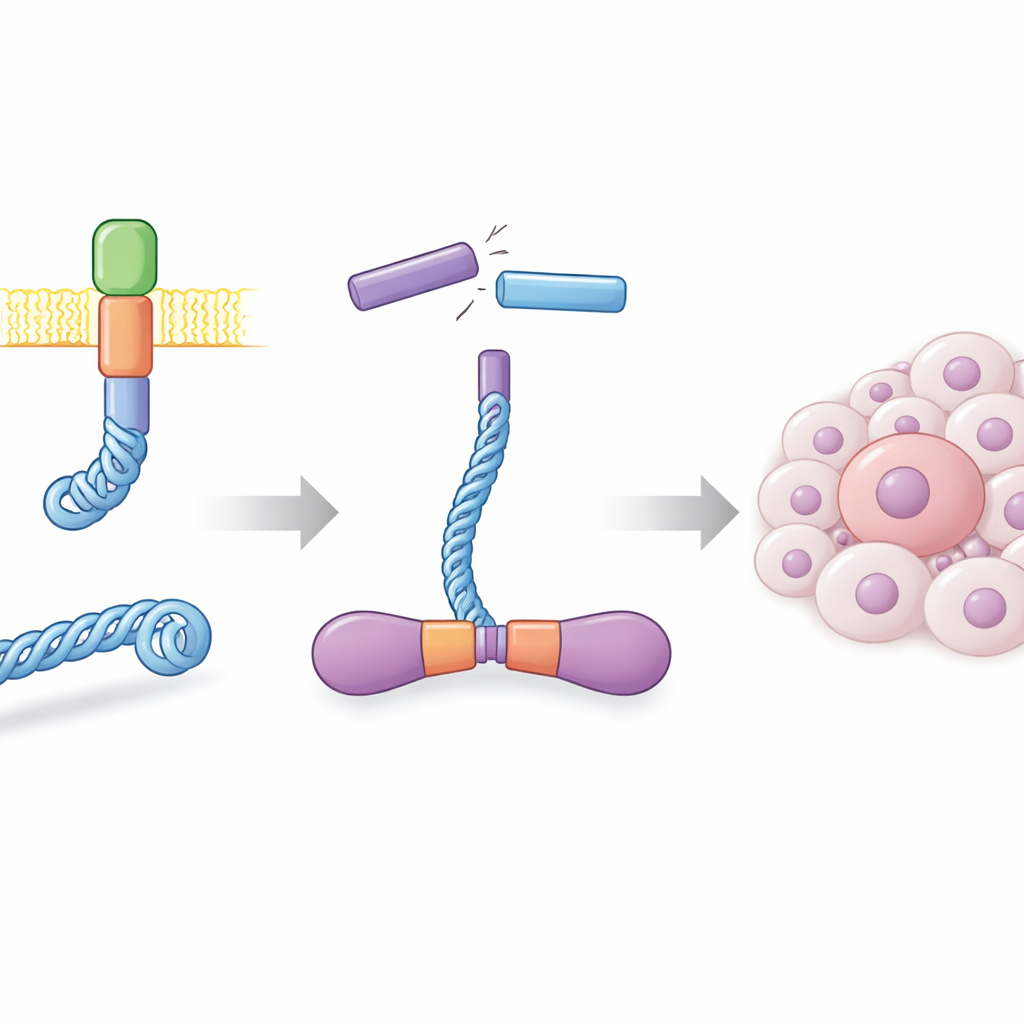
一种以两种燃料运行的激酶
大多数激酶使用 ATP 作为其反应的磷酸供体。当作者用生化测定和时间分辨质谱分析 CCDC6‑RET 的活性时,发现了一个令人惊讶的现象:该蛋白的磷酸化不仅随 ATP 增加,也随 ADP——ATP 消耗后的低能产物——增加。随后的实验证明 CCDC6‑RET 可结合两种核苷酸并可将任一者作为磷酸供体,尽管用 ATP 时反应更快。在中等 ADP 水平下,融合蛋白仍然保持活性,但非常高的 ADP 浓度会开始干扰由 ATP 驱动的活性,表明 ADP 可根据其丰度既为这种致癌酶提供燃料又对其进行调控。
表面微调的控制开关
研究团队进一步绘制了 CCDC6‑RET 自我磷酸化的具体位点。他们发现多个位点不仅位于 RET 的催化核心区,也分布在 CCDC6 片段中,其中包括此前未知的位点。位于一个称为激活环的柔性片段上的两个相邻酪氨酸发挥不同作用。一个位点(Tyr 900)对融合蛋白的正确折叠和稳定性至关重要,而另一个(Tyr 905)对高效磷酸化其他蛋白是必需的。突变 Tyr 905 在很大程度上保留了蛋白自我修饰的能力,但严重削弱了其对外加肽底物的作用,表明“自我激活”和“向外传递信号”在一定程度上是分离控制的。这种细微的调控可能帮助融合蛋白持续开启而不丧失结构完整性。
以三维显示蛋白的可动部分
为理解这些化学变化如何与构象相关,研究者结合预测性人工智能模型、电子显微镜、小角 X 射线散射和交联质谱重建了三维图景。在静止状态下,CCDC6‑RET 二聚体呈“面对面”构型:两个激酶结构域在由 CCDC6 段形成的共同缠绕螺旋柄底部紧密相邻,其激活环彼此接触。结合 ATP 或 ADP 后,这些激酶叶片像筷子尖端一样分开。计算机模拟表明,在这种更开放的状态下,每个激酶都可以“就位”并磷酸化自身的激活环(“就位内”),为二聚体对其他细胞靶标的快速信号传递做好准备。
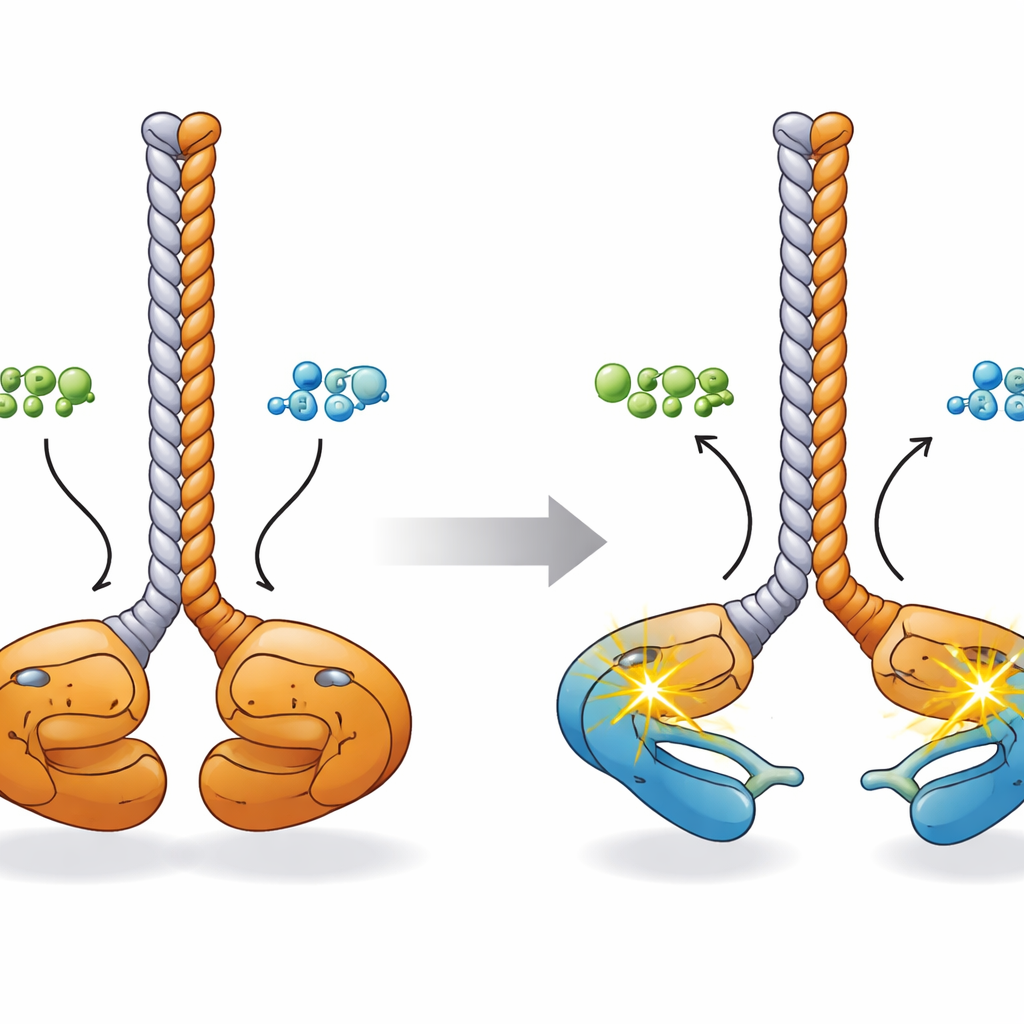
对癌症及未来疗法的意义
肿瘤细胞常处于能量危机边缘,ATP 降低而 ADP 升高。能够用 ATP 或 ADP 运行的融合激酶——甚至在 ADP 富集条件下改变其底物偏好——因此可能在固体肿瘤的严苛微环境中具有生存优势。通过阐明 CCDC6‑RET 的构建方式、二聚化机制、如何利用两种细胞燃料以及哪些磷酸化位点最为关键,这项工作为设计新一代药物提供了详细蓝图。这类药物不仅可以瞄准活性位点,还可以旨在破坏二聚体、干扰激活环的切换,或利用该酶对细胞能量平衡的非同寻常依赖性。
引用: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
关键词: RET 融合, 乳头状甲状腺癌, 肺腺癌, 蛋白激酶激活, ATP ADP 代谢