Clear Sky Science · es
La proteína de fusión oncogénica CCDC6-RET es una quinasa dependiente tanto de ATP como de ADP
Por qué importa este estudio sobre el cáncer
Los cánceres de pulmón y tiroides suelen estar impulsados por versiones defectuosas de proteínas de comunicación celular llamadas quinasas. Una de esas versiones defectuosas, la proteína de fusión CCDC6-RET, aparece con frecuencia en el cáncer papilar de tiroides y en algunos cánceres de pulmón, especialmente tras la exposición a radiación. Este estudio revela cómo esa proteína de fusión se activa y por qué puede estar excepcionalmente adaptada al entorno estresado y pobre en energía dentro de los tumores, abriendo nuevas vías para tratamientos dirigidos.
Un empalme genético que alimenta tumores
En células sanas, la proteína RET se sitúa en la membrana celular y ayuda a transmitir señales de crecimiento. En muchos cánceres de tiroides, y en un subconjunto de cánceres de pulmón, el ADN se rompe y vuelve a unirse en lugares incorrectos, creando un gen híbrido que fusiona parte de la proteína CCDC6 con el dominio funcional de RET. El resultado, llamado CCDC6-RET, es un motor de señalización autónomo que ya no necesita señales externas normales. Los autores produjeron esta proteína de fusión en gran cantidad usando células de insecto y demostraron que forma pares muy estables, o dímeros, en solución. Estos dímeros eran altamente activos, se auto-fosforilaban en muchos sitios y respondían con fuerza a fármacos conocidos que bloquean RET, confirmando que la proteína producida en laboratorio se comporta como su homóloga que impulsa el cáncer.
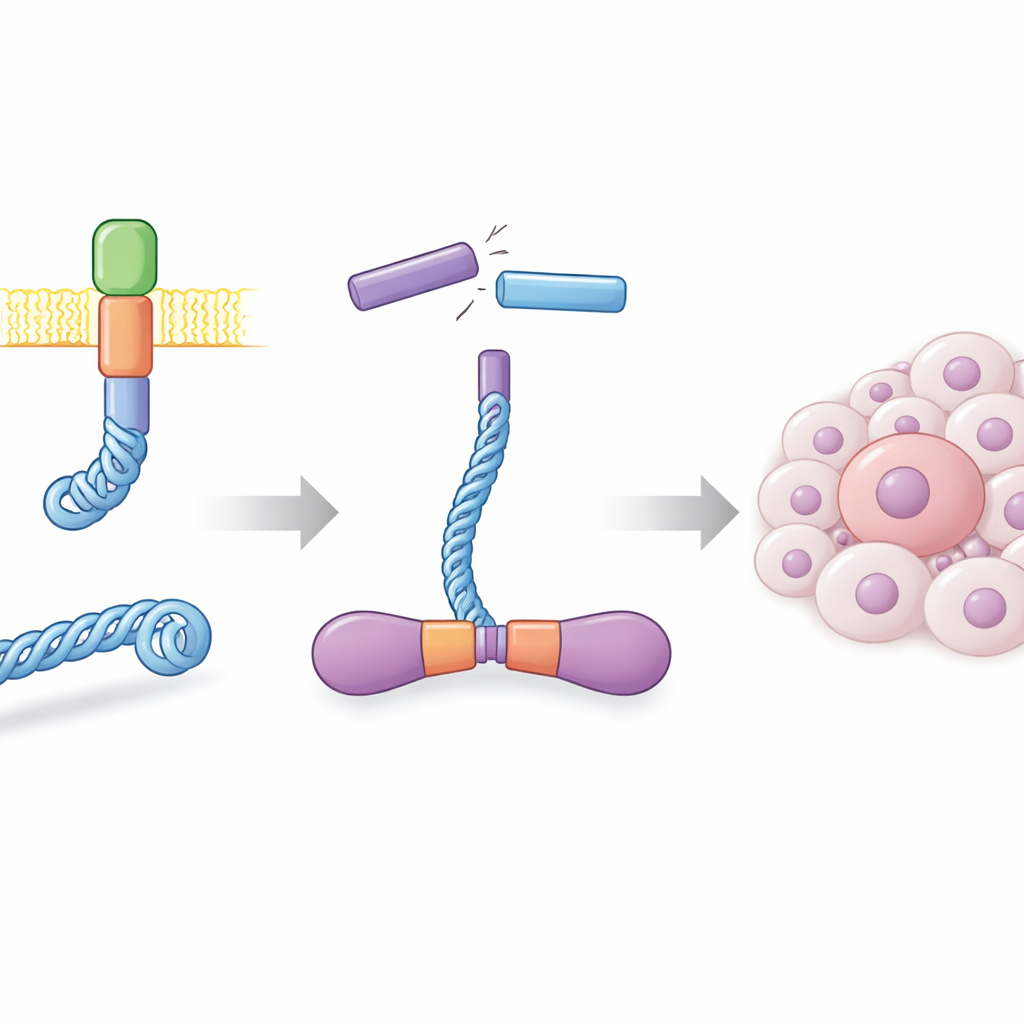
Una quinasa que funciona con dos tipos de combustible
La mayoría de las quinasas utilizan ATP, la principal moneda energética de la célula, como fuente de fosfato para sus reacciones. Cuando los autores analizaron la actividad de CCDC6-RET mediante ensayos bioquímicos y espectrometría de masas resolviendo el tiempo, observaron algo sorprendente: la fosforilación de la proteína aumentaba no solo con ATP sino también con ADP, el producto de menor energía que queda tras el gasto de ATP. Experimentos de seguimiento mostraron que CCDC6-RET se une a ambos nucleótidos y puede usar cualquiera de los dos como donante de fosfato, aunque funciona más rápido con ATP. A niveles moderados de ADP la fusión permanece activa, pero concentraciones muy altas de ADP empiezan a interferir con la actividad impulsada por ATP, lo que sugiere que el ADP puede tanto alimentar como regular esta enzima cancerígena según su abundancia.
Interruptores finamente ajustados en la superficie de la proteína
El equipo continuó mapeando exactamente dónde CCDC6-RET se fosforila a sí misma. Encontraron múltiples sitios no solo en el núcleo catalítico de RET sino también en la porción CCDC6, incluidos sitios desconocidos hasta ahora. Dos tirosinas vecinas en un segmento flexible llamado bucle de activación desempeñaron papeles distintos. Un sitio (Tyr 900) parece crucial para el plegamiento y la estabilidad adecuados de la proteína de fusión, mientras que la otra (Tyr 905) es esencial para la fosforilación eficiente de otras proteínas. La mutación de Tyr 905 apenas afectó la capacidad de la proteína para auto-modificarse pero dejó muy limitada su capacidad para actuar sobre un péptido sustrato añadido, revelando que la “auto-activación” y la “señalización hacia afuera” están controladas de forma algo separada. Este control matizado puede ayudar a que la proteína de fusión permanezca activa sin perder integridad estructural.
Revelando las partes móviles de la proteína en 3D
Para comprender cómo estos cambios químicos se relacionan con la forma, los investigadores montaron una imagen tridimensional usando modelos predictivos de inteligencia artificial, microscopía electrónica, dispersión de rayos X a ángulo pequeño y espectrometría de masas con entrecruzamiento. En su estado de reposo, el dímero CCDC6-RET adopta una configuración “cara a cara”: los dos dominios quinasa se sitúan cerca uno del otro en la base de un tallo de coiled-coil compartido formado por los segmentos CCDC6, con sus bucles de activación tocándose. Al unirse ATP o ADP, esos lóbulos quinasa se separan como las puntas de un par de palillos. Simulaciones por ordenador sugieren que en este estado más abierto cada quinasa puede alcanzar y fosforilar su propio bucle de activación (“in cis”), preparando el dímero para una señalización rápida hacia otros objetivos celulares.
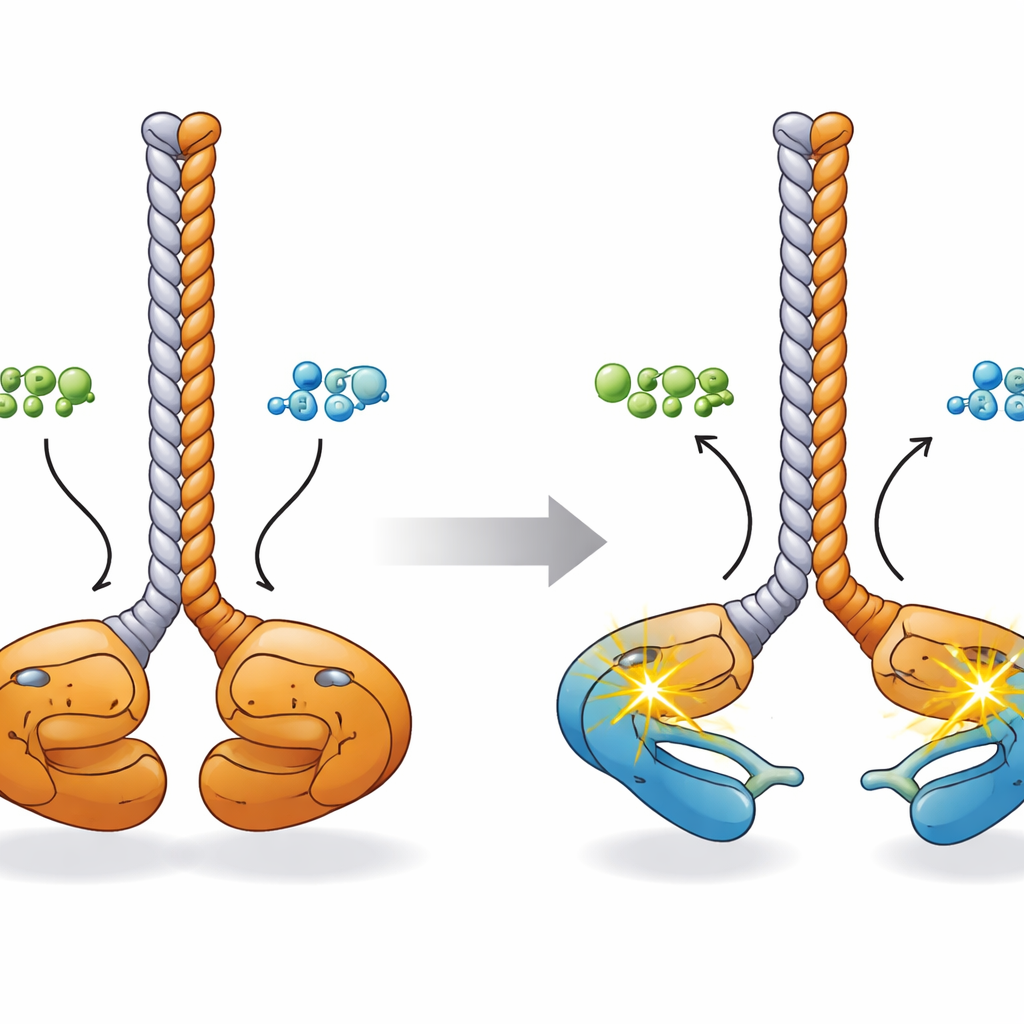
Qué significa esto para el cáncer y futuras terapias
Las células tumorales a menudo viven al borde de una crisis energética, con niveles de ATP más bajos y de ADP más altos que las células sanas. Una quinasa de fusión que puede funcionar con ATP o ADP—e incluso cambiar su preferencia de diana hacia diferentes aminoácidos en condiciones ricas en ADP—podría por tanto tener una ventaja de supervivencia en los microambientes hostiles de los tumores sólidos. Al aclarar cómo se construye CCDC6-RET, cómo se dimeriza, cómo usa ambas formas de combustible celular y qué sitios de fosforilación son los más importantes, este trabajo ofrece un plano detallado para diseñar fármacos de nueva generación. Tales fármacos podrían no solo bloquear el sitio activo, sino también interrumpir el dímero, interferir con el cambio del bucle de activación o explotar la inusual dependencia de la enzima del balance energético celular.
Cita: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
Palabras clave: fusión RET, cáncer papilar de tiroides, adenocarcinoma de pulmón, activación de quinasas, metabolismo ATP ADP