Clear Sky Science · nl
Het oncogene CCDC6-RET-fusie-eiwit is een kinase die afhankelijk is van zowel ATP als ADP
Waarom deze kankerstudie ertoe doet
Kankers van de long en schildklier worden vaak aangedreven door defecte versies van celcommunicatie-eiwitten die kinases heten. Een van die foutieve versies, het CCDC6-RET-fusie-eiwit, komt veel voor bij papillaire schildklierkanker en in sommige longkankers, vooral na bestraling. Deze studie onthult hoe dat fusie-eiwit zichzelf activeert en waarom het mogelijk uitzonderlijk goed is aangepast aan de gestreste, energiearme omgeving binnen tumoren, wat nieuwe invalshoeken voor gerichte behandeling opent.
Een genetische mix die tumoren voedt
In gezonde cellen zit het RET-eiwit in het celmembraan en helpt het groeisignalen doorgeven. In veel schildklierkankers, en in een subset van longkankers, breekt en sluit DNA op de verkeerde plaatsen weer aan elkaar, waardoor een hybride gen ontstaat dat een deel van CCDC6 fuseert met het werkende deel van RET. Het resultaat, genoemd CCDC6-RET, is een zelfstandig signaleringsapparaat dat niet langer normale externe aanwijzingen nodig heeft. De auteurs produceerden dit fusie-eiwit in grote hoeveelheden met insectencellen en toonden aan dat het in oplossing zeer stabiele paren, of dimeren, vormt. Deze dimeren waren sterk actief, voegden op veel plekken fosfaatgroepen aan zichzelf toe en reageerden sterk op bekende RET-remmers, wat bevestigt dat het in het laboratorium gemaakte eiwit zich gedraagt als zijn kankerveroorzakende tegenhanger.
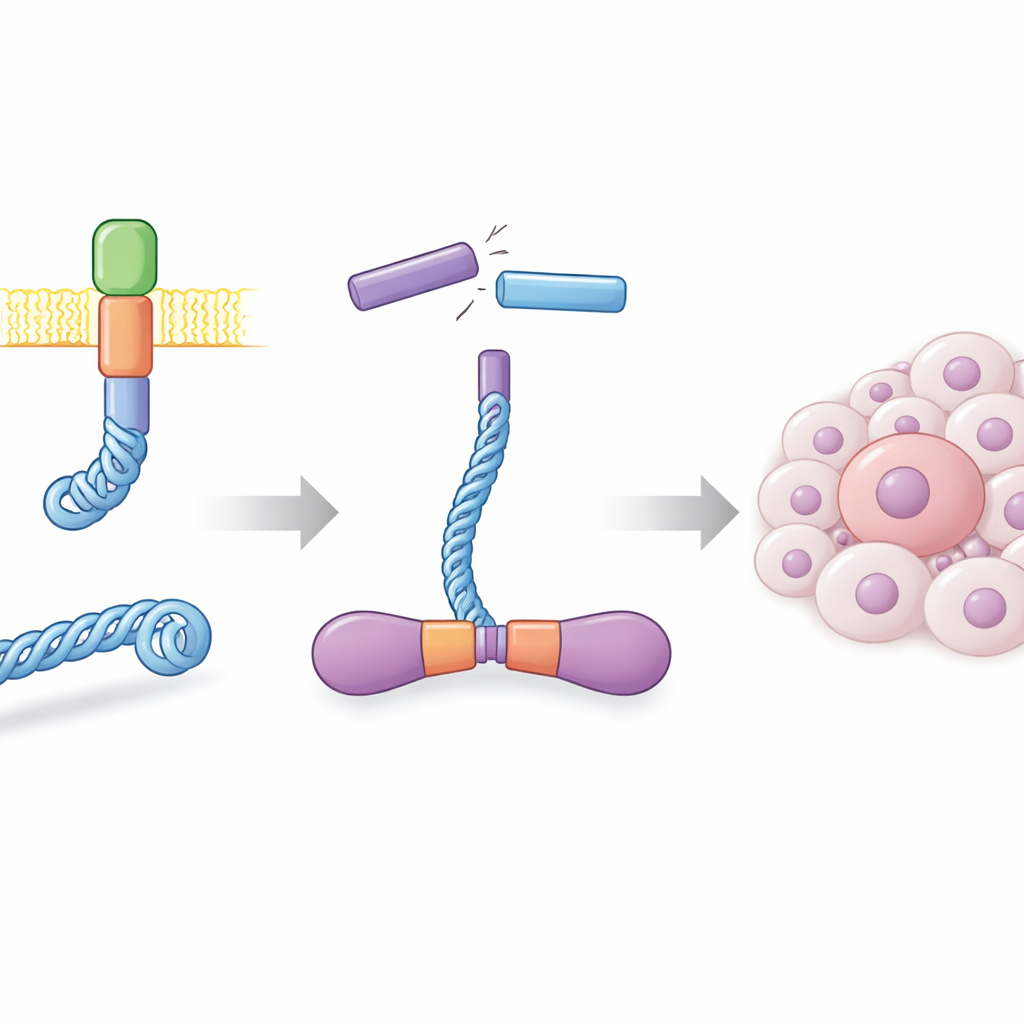
Een kinase die op twee soorten brandstof draait
De meeste kinases gebruiken ATP, de belangrijkste energie-eenheid van de cel, als fosfaatbron voor hun reacties. Toen de auteurs de activiteit van CCDC6-RET analyseerden met biochemische assays en tijdsgeresolveerde massaspectrometrie, viel iets verrassends op: de fosforylering van het eiwit nam niet alleen toe met ATP maar ook met ADP, het energielagere product dat overblijft nadat ATP is verbruikt. vervolgexperimenten toonden aan dat CCDC6-RET beide nucleotiden kan binden en elk van beide als fosfaatdonor kan gebruiken, hoewel het sneller werkt met ATP. Bij matige ADP-niveaus blijft de fusie actief, maar zeer hoge ADP-concentraties beginnen de ATP-gedreven activiteit te verstoren, wat suggereert dat ADP deze kankerenzyme zowel kan voeden als reguleren afhankelijk van de hoeveelheid.
Fijn afgestelde schakelaars op het eiwitoppervlak
Het team bracht vervolgens precies in kaart waar CCDC6-RET zichzelf fosforyleert. Ze vonden meerdere sites niet alleen in de catalytische kern van RET maar ook in het CCDC6-gedeelte, inclusief eerder onbekende locaties. Twee naburige tyrosines in een flexibele segment dat de activatielus heet, vervulden verschillende rollen. Eén site (Tyr 900) blijkt cruciaal voor de juiste vouwing en stabiliteit van het fusie-eiwit, terwijl de andere (Tyr 905) essentieel is voor efficiënte fosforylering van andere eiwitten. Het muteren van Tyr 905 liet grotendeels de mogelijkheid van het eiwit om zichzelf te modificeren intact, maar belemmerde sterk zijn vermogen om een toegevoegd peptide-substraat te bewerken, wat onthult dat “zelfactivatie” en “naar buiten signaleren” enigszins afzonderlijk worden gereguleerd. Deze genuanceerde controle kan het fusie-eiwit helpen actief te blijven zonder structurele integriteit te verliezen.
De bewegende delen van het eiwit in 3D onthuld
Om te begrijpen hoe deze chemische veranderingen verband houden met vorm, stelden de onderzoekers een driedimensionaal beeld samen met behulp van voorspellende kunstmatige-intelligentie-modellen, elektronenmicroscopie, small-angle X-ray scattering en crosslinking-massaspectrometrie. In rust neemt het CCDC6-RET-dimeer een “face-to-face”-configuratie aan: de twee kinasedomains liggen dicht bij elkaar aan de basis van een gedeelde coiled-coil-stengel gevormd door de CCDC6-segmenten, met hun activatielussen die elkaar raken. Bij binding van ATP of ADP zwaaien die kinaselobbia uit elkaar als de uiteinden van een stel eetstokjes. Computersimulaties suggereren dat in deze meer open toestand elke kinase in staat is om in cis zijn eigen activatielus te fosforyleren, waarmee het dimeer wordt klaargemaakt voor snelle signalering naar andere cellulaire doelen.
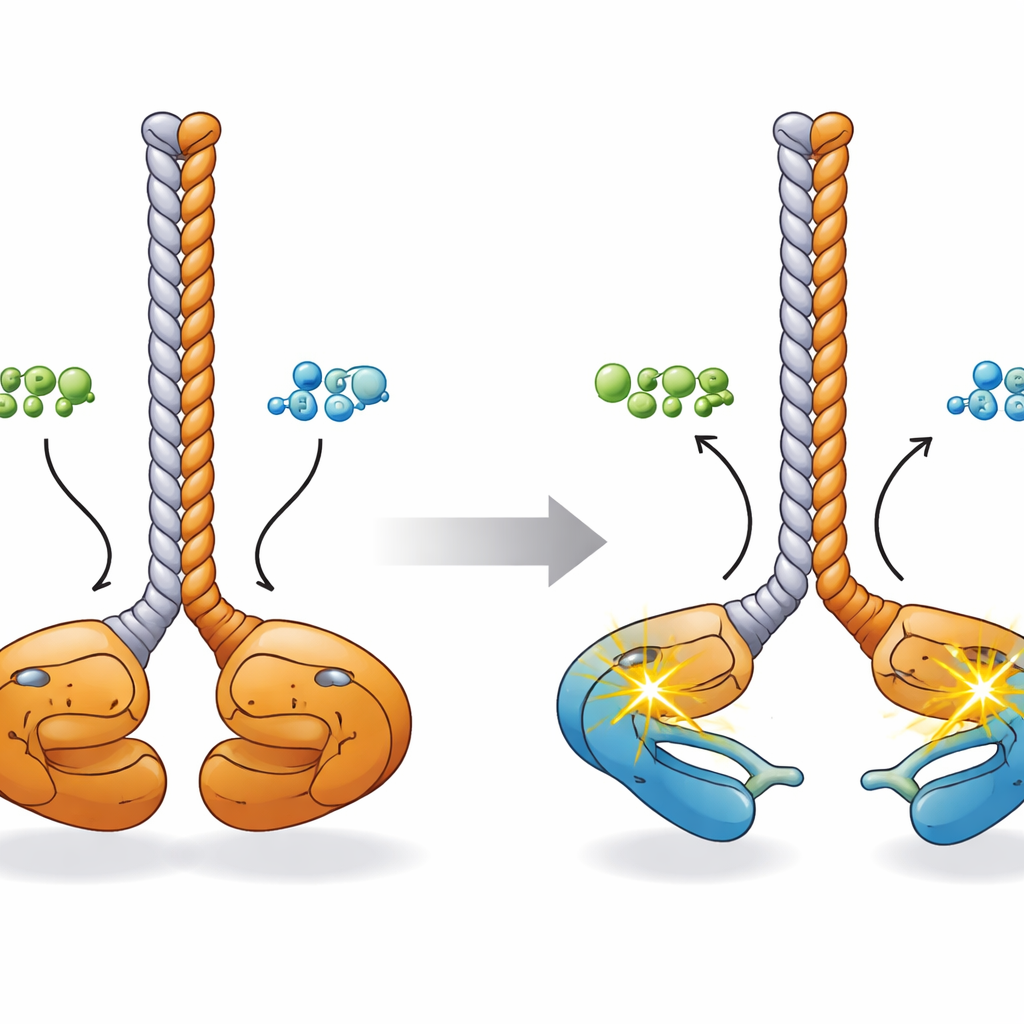
Wat dit betekent voor kanker en toekomstige therapieën
Tumorcellen leven vaak op de rand van een energiecrisis, met lagere ATP- en hogere ADP-niveaus dan gezonde cellen. Een fusie-kinase die met ATP of ADP kan functioneren — en zelfs zijn doelvoorkeur kan verleggen naar verschillende aminozuren onder ADP-rijke omstandigheden — kan daarom een overlevingsvoordeel hebben in de harde micro-omgevingen van solide tumoren. Door te verduidelijken hoe CCDC6-RET is opgebouwd, hoe het dimeriseert, hoe het beide vormen van cellulaire brandstof gebruikt en welke fosforyleringssites het meest van belang zijn, biedt dit werk een gedetailleerde blauwdruk voor het ontwerpen van volgende-generatie medicijnen. Dergelijke geneesmiddelen zouden niet alleen de actieve plaats kunnen blokkeren, maar ook het dimeer kunnen verstoren, het omschakelen van de activatielus kunnen belemmeren of de ongebruikelijke afhankelijkheid van het enzym van de energiebalans van de cel kunnen uitbuiten.
Bronvermelding: Martín-Hurtado, A., Contreras, J., Sánchez-Wandelmer, J. et al. The oncogenic CCDC6-RET fusion protein is a dual ATP- and ADP-dependent kinase. Nat Commun 17, 3595 (2026). https://doi.org/10.1038/s41467-026-69833-y
Trefwoorden: RET-fusie, papillaire schildklierkanker, longadenocarcinoom, activatie van proteïnekinasen, ATP- en ADP-metabolisme